Hémochromatose génétique

TOME 137
|
N° 4
|
AVRIL 2015
LE CONCOURS MÉDICAL
|
279
Pr Yves Deugnier
Hôpital Pontchaillou
CHU de Rennes
Conseiller scientifique
Hémochromatose
génétique
Intégré tôt et à vie, le parcours mène à une vie normale
PARCOURS DE SOINS
DR
Dossier coordonné par Brigitte Némirovsky
280. Nous avons les moyens d’éviter la surcharge
en fer et ses complications
Pr Yves Deugnier
281. Dépistage et diagnostic précoce :
deux circonstances, deux dosages
Pr Philippe Sogni
284. Diagnostic différentiel : clinique, biologie,
parfois IRM
Pr Marc Ruivard
286. Sensibiliser pour un diagnostic précoce :
priorité absolue
Entretien avec Brigitte Pineau
1
étape
290. Bilan rhumatologique et osseux : prérequis
pour préserver la qualité de vie
Pr Pascal Guggenbuhl
2
suite
{
300. Ne rien laisser au hasard pour permettre
une vie normale
Entretien avec Joël Demares
302. Bien que codifiée, la prise en charge reste
hétérogène
Entretien avec le Dr Edouard Bardou-Jacquet
{
292. Du simple suivi pour les formes débutantes
au traitement par saignées
Pr Véronique Loustaud-Ratti, Dr Paul Carrier
297. L’enquête familiale : un pilier de la prise en charge
Dr Edouard Bardou-Jacquet
3
étape
287. Bilan préthérapeutique à adapter
au cas par cas
Pr Domnique Guyader
2
étape
Tous droits reservés - Le Concours médical

280
|
LE CONCOURS MÉDICAL
TOME 137
|
N° 4
|
AVRIL 2015
Hémochromatose génétique
{
PARCOURS DE SOINS
Rôle majeur du généraliste, collaboration
régulière, intervenants multiples
Les articles de ce dossier du Concours médical
soulignent le rôle majeur du médecin généraliste à
toutes les étapes d’une longue histoire :
– diagnostic initial face à des symp-
tômes souvent peu spécifiques
(asthénie chronique, arthropathie,
modeste cytolyse hépatique non
expliquée…) ;
– dépistage familial, auquel il faut savoir faire adhérer
le patient ;
– bilan initial à adapter en fonction du stade auquel la
maladie est diagnostiquée, saignées à vie impliquant
rigueur et soutien ;
– enfin, vigilance sur de longues années avec implé-
mentation d’un dépistage échographique semestriel
du carcinome hépatocellulaire si une cirrhose a été
repérée au moment du diagnostic.
Une telle prise en charge implique une collabo-
ration régulière avec des partenaires variés (spé-
cialistes et centres de référence et de compétence,
infirmiers, associations de patients) et la tenue d’un
carnet de suivi par le patient sous le contrôle de son
médecin généraliste.
Plus de moyens pour une prise en charge
plus précoce
Au cours des quarante dernières années, le
visage de la maladie s’est considérablement
modifié.
L’avènement de moyens diagnostiques perfor-
mants (IRM hépatique, test génétique) permet un
diagnostic de plus en plus précoce : les formes
d’expression purement biologique et les formes
monosymptomatiques (asthénie, ostéo-arthropa-
thie) ont remplacé le tableau classique de cirrhose
bronzée avec diabète.
Le traitement, de mieux en mieux codifié,
apporte une espérance de vie améliorée si la fer-
ritinémie initiale est inférieure à 1 000 μg/L et
normalisée si celle-ci est comprise entre 1 000 et
2 000 μg/L. Seules les formes sévères avec fer-
ritinémie initiale supérieure à 2 000 μg/L voient
leur espérance de vie amputée, essentiellement
par le diabète et le carcinome hépatocellulaire.
Tous les outils sont à présent en place pour
permettre une prise en charge toujours plus
précoce. Le temps diagnostique est donc à
l’information des médecins, des patients et de
leur famille. Le temps thérapeutique reste à la
saignée en attendant que les mini-hepcidines,
les agonistes de BMP6 (bone morphogenetic
protein 6) et autres inhibiteurs de TMPRSS6
(transmembrane protease, serine 6) viennent
remplacer cette thérapie certes désuète mais ô
combien efficace dès lors qu’elle est correcte-
ment menée.
Bonne lecture ! •
Nous avons les moyens d’éviter
la surcharge en fer et ses complications
Pr Yves Deugnier ([email protected]), service des maladies du foie, centre de référence des surcharges génétiques en fer rares
et centre de dépistage familial de l’hémochromatose, hôpital Pontchaillou, CHU de Rennes
Les hémochromatoses génétiques (HG) sont largement dominées par
l’hémochromatose HFE – aussi dénommée HFE-1 – qui représente en
France plus de 95 % des surcharges en fer héréditaires et concerne
une personne sur 300. Ce dossier du Concours médical aborde de
façon pragmatique la prise en charge du patient hémochromatosique,
laquelle a beaucoup évolué au cours des dernières décennies.
L’homozygotie C282Y, condition nécessaire mais pas suffisante
L’hémochromatose génétique HFE-1 est une maladie autosomique récessive liée à une
mutation majeure, C282Y, à l’origine d’une perturbation de la synthèse d’hepcidine,
hormone de régulation de l’absorption digestive et de la sortie macrophagique du fer.
L’homozygotie C282Y conduit à un décit en hepcidine, lequel aboutit à une augmentation
du fer systémique à l’origine d’une élévation de la saturation de la transferrine, signe biolo-
gique cardinal de l’affection, puis secondairement à la constitution d’un excès viscéral de
fer dont témoigne l’élévation progressive de la ferritinémie. Les autres génotypes HFE-1
(hétérozygotie C282Y, hétérozygotie dite composite C282Y/mutation mineure, homozygotie
pour une mutation mineure) ne sont pas responsables de surcharges en fer signicatives.
L’homozygotie C282Y est une condition nécessaire mais non sufsante au développement
de la surcharge en fer HFE-1. L’excès de fer et ses potentielles complications ostéo-
articulaires, hépatiques, endocriniennes et cardiaques sont modulés par d’autres facteurs
génétiques encore mal cernés et par des facteurs d’environnement (alimentation, alcool,
syndrome métabolique, tabac…).
L’auteur déclare n’avoir aucun lien d’intérêts.
Tous droits reservés - Le Concours médical

TOME 137
|
N° 4
|
AVRIL 2015
LE CONCOURS MÉDICAL
|
281
Hémochromatose génétique
2
3
1
Devant quels signes évoquer le diagnostic ?
Les deux signes cliniques d’appel principaux
sont une asthénie physique ou psychique anor-
male et des manifestations articulaires à type
de douleurs prédominant au niveau métacarpo-
phalangien ou de crises de chondrocalcinose(1, 2).
Les autres manifestations sont soit moins évo-
catrices, soit plus tardives (tableau p. 282). L’ex-
pression phénotypique de la maladie est variable
suivant les personnes, que ce soit en intensité ou
en localisation.
L’atteinte articulaire est le principal respon-
sable de l’altération de la qualité de vie des per-
sonnes atteintes d’hémochromatose(2). L’atteinte
hépatique est le principal responsable de la
morbi-mortalité de l’hémochromatose, suivie par
les complications du diabète et l’atteinte car-
diaque. Les données récentes de mortalité chez
les patients atteints d’hémochromatose montrent
qu’il persiste une surmortalité d’origine hépatique
chez les patients avec une surcharge en fer ini-
tiale massive et qu’en revanche ceux avec une
surcharge en fer initiale modérée ont une dimi-
nution de la mortalité cardiovasculaire et par
cancers extra-hépatiques due au traitement par
saignées(3).
Comment affirmer le diagnostic ?
La présence de symptômes liés à l’hémochro-
matose traduit la présence d’une surcharge en fer
et donc d’anomalies du bilan martial.
Le taux de ferritinémie est à interpréter en fonc-
tion du sexe et, chez la femme, en fonction de
l’âge (avant ou après la ménopause). Il n’est pas
Dépistage et diagnostic précoce :
deux circonstances, deux dosages clés
Pr Philippe Sogni ([email protected]), université Paris-Descartes, INSERM U-1016, Assistance publique–Hôpitaux de Paris, service d’hépatologie,
hôpital Cochin, Paris
L’hémochromatose de type 1 est une maladie autosomale récessive de l’adulte de pénétrance incomplète
pouvant entraîner une surcharge en fer de l’organisme, responsable d’une altération de la qualité de vie et
d’une augmentation de la morbi-mortalité (figure 1). Le diagnostic se fait dans deux circonstances : soit il
existe des anomalies biologiques ou des symptômes qui doivent le faire évoquer, soit le diagnostic se fait
dans le cadre d’une enquête familiale. Plus le diagnostic est fait à un stade précoce de la maladie, plus le
traitement par les saignées est efficace et prévient les complications(1).
1
étape
influencé par le jeûne. En revanche, il pourrait
être influencé par l’origine ethnique, avec des
limites supérieures plus élevées chez les per-
sonnes d’origine asiatique(4, 5). L’hyperferritiné-
mie est un motif de consultation très fréquent
(voir article p. 284). Dans plus de 90 % des cas,
elle est liée à d’autres causes que l’hémochroma-
tose : consommation excessive d’alcool, syndrome
inflammatoire, pathologie tumorale, syndrome
métabolique, syndrome de lyse cellulaire(1). Dans
ces cas, le coefficient de saturation de la transfer-
rine est le plus souvent normal.
Le coefficient de saturation de la transferrine est
utile pour le dépistage de l’hémochromatose à
l’échelle d’une population mais doit être inter-
prété avec prudence à l’échelon individuel. En
effet, la variabilité de ce test est importante pour
Figure 1. Les différents stades de l’hémochromatose
Âge
Stades Maladie
grave
SymptômesAnomalies du
bilan martial
Anomalie
génétique
IV + + + +
++
+
– – –
– –
–
+
+
+
III
II
I
Tous droits reservés - Le Concours médical

282
|
LE CONCOURS MÉDICAL
TOME 137
|
N° 4
|
AVRIL 2015
Hémochromatose génétique
{
PARCOURS DE SOINS
un même individu, et la réalisation du test à jeun
ne semble pas augmenter ses performances(6). En
pratique, il est donc important de confirmer l’élé-
vation du coefficient de saturation de la transfer-
rine par un deuxième dosage avant de demander
un test génétique(1).
En cas d’association d’une hyperferritinémie
et d’une augmentation du coefficient de satura-
tion de la transferrine sur deux prélèvements,
le diagnostic d’hémochromatose est fortement
évoqué, et il est donc nécessaire de proposer un
test génétique pour le confirmer (figure 2). En
effet, dans cette situation, il a été rapporté que
l’homozygotie C282Y était présente chez environ
90 % des hommes et 75 % des femmes(7).
Le test génétique à réaliser de première inten-
tion est la recherche de la mutation C282Y sur
le gène HFE. Ce test réalisé sur tube EDTA est
inscrit à la nomenclature (B180) et est rem-
boursé depuis 2007. Comme pour tout test
génétique, une information claire et adaptée doit
être donnée à la personne avant le prélèvement.
Celle-ci doit signer une notice d’information et
de consentement en triple exemplaire, pour la
personne elle-même, pour le dossier médical et
pour le laboratoire réalisant ce test. Le résultat
du test sera renvoyé au médecin prescripteur,
à charge pour lui de l’expliquer au patient au
cours d’une consultation aboutissant à un conseil
génétique.
Les autres recherches de mutations, que ce
soit dans le gène HFE ou dans d’autres gènes
impliqués, n’ont d’intérêt qu’en cas de surcharge
en fer prouvée sans autre cause retrouvée et
sans mutation C282Y homozygote ; elles ne sont
à envisager que dans le cadre d’une consultation
spécialisée.
L’IRM avec mesure de la concentration hépatique en
fer (CHF) n’est pas nécessaire pour le diagnostic
ni pour le suivi du traitement d’un patient atteint
d’une hémochromatose C282Y homozygote(8).
Dans cette situation clinique, il existe en effet
un parallélisme entre le taux de ferritine et la
CHF à l’IRM. En revanche, l’IRM s’avère néces-
saire pour affirmer ou éliminer une surcharge en
fer chez un patient avec une hyperferritinémie
et un test génétique de recherche de mutation
C282Y négatif (figure 2). En l’absence de mutation
C282Y à l’état homozygote, le seuil d’hyperferri-
tinémie à partir duquel une IRM avec mesure du
CHF est pertinente n’est pas défini (probablement
pour des valeurs supérieures à 750-1 000 μg/L)[8].
Elle peut être également utile en cas d’étiologies
multiples suspectées, par exemple une hyper-
ferritinémie avec un syndrome métabolique, une
homozygotie C282Y et un coefficient de saturation
de la transferrine limite.
Tableau. Principales manifestations cliniques et biologiques
de l’hémochromatose
Manifestations Précoces Tardives
Générales Asthénie physique ou psychique
Douleurs abdominales Altération de l’état général
Articulaires
Atteinte
métacarpo-phalangienne
Chondrocalcinose
Atteintes articulaires multiples
Ostéopathie sous-chondrale
Ostéoporose
Cutanéo-phanériennes –
Mélanodermie, ichtyose,
koïlonychie, hypopilosité,
Porphyrie cutanée tardive
Hépatiques Élévation modérée des
transaminases
Hépatomégalie
Cirrhose
Carcinome hépatocellulaire
Endocriniennes Dysfonction sexuelle
Diabète
Impuissance
Stérilité et troubles de l’ovulation
Aménorrhée secondaire
Ménopause précoce
Cardiaques –
Troubles du rythme
Cardiomyopathie non obstructive
Complications cardiovasculaires
du diabète
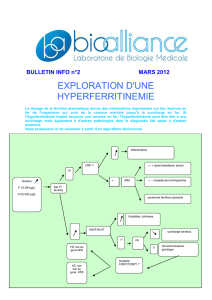
Hyperferritinémie
Coefficient de saturation
de la transferrine
> 45 % x 2
Hémochromatose probable à confirmer par
recherche de C282Y
C282Y homozygote Pas de mutation ou C282Y hétérozygote
IRM du foie / poursuite analyse génétique
– hémochromatose génétique autre
– maladie hépatique évoluée
– dysmyélopoïèse
Hémochromatose confirmée
Élimner :
– alcool
– syndrome inammatoire
– lyse cellulaire
– pathologie tumorale
– syndrome métabolique
Figure 2. Algorithme de décision en cas d’hyperferritinémie associée
à une augmentation du coefficient de saturation de la transferrine
Tous droits reservés - Le Concours médical

 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
1
/
24
100%