Dystrophies musculaires du gène à la pathologie

Matecki stefan
Laboratoire de Physiologie des interations, EA 701, Montpellier, France.
Dystrophies musculaires du gène à
la pathologie

Maladies génétiques hétérogènes
Perte intégrité de la Fibre musculaire
Perte de la force de contraction et de l ’endurance
Introduction

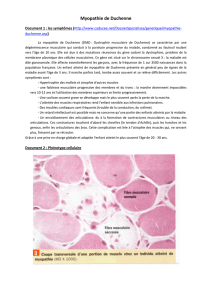
Variation de calibre
Infiltration de cellules inflammatoires, TC et tissu adipeux
Noyaux centro-nucléaires

normal Peu évoluée
Très évoluée
Fragilisation de la membrane
Nécrose
Perte tissu musculaire

actine Tropomyosine
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
1
/
21
100%