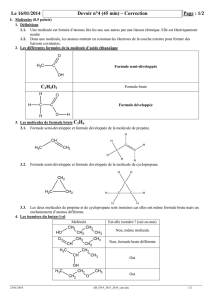
Principe

En chimie organique, la fonction ester désigne un groupement caractéristique formé d'un atome de carbone lié
simultanément à un atome d'oxygène par une double liaison et à un groupement alkoxy du type -O-R'. Les esters
sont des dérivés des acides carboxyliques, ils résultent très généralement de l'action d'un alcool sur ces acides avec
élimination d'eau. Les fonctions esters se retrouvent dans de nombreuses molécules biologiques, notamment les
triglycérides (huiles, matière grasse). Les esters ont souvent une odeur agréable et entrent dans la composition de
certains arômes naturels (fruits, fleurs). Ils sont aussi beaucoup utilisés pour les arômes de synthèse et dans la
parfumerie.
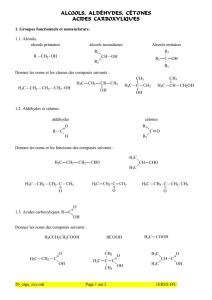
L’acétate d’isoamyle est un ester de l’acide acétique et de l'alcool isoamylique se
présentant sous la forme d'un liquide transparent incolore, à l'odeur de banane
ou encore d'« arlequin ». Il est présent dans les pommes mûres. Il est utilisé
dans la fabrication de peintures, ou comme agent de saveur. C'est aussi une des
phéromones d'alarme de l'abeille.
Principe
La synthèse de l’acétate d’isoamyle se réalise par une réaction d’estérification : action lente et limitée d’un alcool sur
un acide carboxylique pour donner un ester et de l’eau.
Q1. Entourer le groupe fonctionnel ester sur la formule topologique précédente.
Q2. Donner les formules topologiques et les noms de l’acide et de l’alcool à utiliser pour cette réaction.
Tableau de données utiles :
Alcool isoamylique
Anhydride acétique
Acétate d’isoamyle
Acide acétique
Densité
0,81
1,08
0,87
1,05
Température
d’ébullition (1 bar)
132 °C
139,5 °C
142 °C
117,9 °C
Solubilité dans l'eau
Assez faible
Très soluble
Très faible
Très soluble
Solubilité dans l’eau
salée
Faible
Très soluble
Quasi-nulle
Soluble
Compétences travaillées : Réaliser un montage expérimental
Respecter les règles de sécurité
Ecrire le résultat d’une mesure
Analyser un résultat expérimental
Communiquer et argumenter en utilisant un vocabulaire scientifique adapté

Propriétés des réactifs utilisés
Substances
chimiques
Phrases danger et prudence et
pictogramme
Masse Molaire,
données
Alcool isoamylique
C5H12O
H226 : liquide et vapeurs inflammables
H332 : nocif par inhalation
H335 : Peut irriter les voies respiratoires
M = 88,1 g.mol-1
Tfus = - 117 °C
Téb = 132 °C
d = 0,81
Acide acétique
CH3COOH
H226 : liquide et vapeurs inflammables
H314 : provoque de graves brûlures de la peau et
des lésions oculaires
M = 60,0 g.mol-1
Téb=117,9°C
d = 1,05
Acétate d’isoamyle
CH3COOC5H11
H226 : liquide et vapeurs inflammables
EUH066 : L'exposition répétée peut provoquer
dessèchement ou gerçures de la peau
M = 130,2 g.mol-1
Téb =142 °C
d = 0,87
Acide sulfurique
concentré
H2SO4
H290 : Peut être corrosif pour les métaux
H314 : Provoque de graves brûlures de la peau et
des lésions oculaires
M = 98,0 g.mol-1
Téb = 337 °C
d = 1,83
Hydrogénocarbonate
de sodium
NaHCO3
M = 84,0 g.mol-1
Tfus = 50 °C
d = 2,22
Consignes de sécurité: comme on manipule des acides purs et des alcools nocifs, le port des lunettes de protection
et des gants est obligatoire. Ne pas jeter les produits à l'évier mais dans le conteneur à produits organiques.
E3. Sous la hotte, dans un ballon de 250 mL bien sec, introduire environ 10 mL d’alcool isoamylique et environ 15 mL
d’acide acétique pur (dit : « glacial »).
E4. Ajouter environ 1 mL d’acide sulfurique concentré, qques grains de pierre ponce et chauffer à reflux pendant 30
minutes.
Q5. Ecrire l’équation de la réaction de synthèse.
Q6. Calculer les quantités de matière initiales des réactifs, dresser un tableau d’évolution, déterminer l’avancement
maximal xmax et montrer que le l’alcool isoamylique est le réactif limitant de cette synthèse.
Q7. Quel est l’intérêt d’utiliser un excès d’acide acétique ?
Q8. Pourquoi ajoute-t-on de l’acide sulfurique ?
Q9. Légender le schéma du montage ci-dessous.
Q10. Quel est l’intérêt de ce dispositif ?
Q11. Peut-on inverser les branchements des numéros 4 et 5 du montage ?

Q12. Quel est l’avantage d’un réfrigérant à boules par rapport à un réfrigérant droit ?
Q13. Quel est le rôle de la pierre ponce ?
Q14. Pourquoi le réfrigérant doit-il resté ouvert à son extrémité supérieure ?
Principe :
Après avoir bien séparé les phases aqueuses et organiques par relargage, il s’agit d’éliminer l’acide acétique resté en
phase organique en le faisant réagir avec de l’hydrogénocarbonate de sodium. Il se forme du dioxyde de carbone et
un autre produit très soluble dans l’eau. Enfin, les traces d’eau sont éliminées par séchage.
E15. Arrêter le chauffage et laisser refroidir le ballon à l’air libre pendant 5 minutes.
E16. Achever le refroidissement à l’aide d’un cristallisoir rempli d’eau. Une fois les vapeurs recondensées, arrêter la
circulation d’eau et retirer le ballon du montage.
E17. Rajouter environ 50 mL d’une solution de chlorure de sodium Na+ (aq) + Cl- (aq) saturée et transvaser le contenu
dans une ampoule à décanter (sans y mettre la pierre ponce !).
E18. Laisser décanter et éliminer la phase aqueuse.
E19. Traiter la phase organique dans l’ampoule en ajoutant 25 mL de solution d'hydrogénocarbonate de sodium Na+
(aq), HCO3
- (aq) (attendre que le dégagement gazeux soit fini avant de boucher l’ampoule à décanter et procéder
ensuite avec précaution car le dégagement gazeux peut être important).
E20. Poursuivre l’extraction jusqu’à ce qu’il n’y ait plus de dégagement gazeux puis laisser décanter.
E21. Eliminer la phase aqueuse et récupérer la phase organique dans un erlenmeyer propre et sec.
E22. Peser un autre erlenmeyer bien sec et noter sa masse : mi = . . . . . . g.
E23. Sécher enfin sur sulfate de magnésium anhydre et filtrer dans l’erlenmeyer précédent. Peser l’erlenmeyer
après récupération : mf = . . . . . . . g.
Q24. A quoi sert l’ajout d’eau salée ? On parle de relargage de l’ester.
Q25. Ecrire l’équation de la réaction acido-basique qui se produit lors de l’ajout
d’hydrogénocarbonate de sodium (des ions H+ sont échangés comme des électrons sont
échangés au cours d’une équation redox). Expliquer comment on élimine ainsi l’acide
acétique restant en phase organique. On parle de lavage de la phase organique.
Données : couples acide / base : CH3CO2H / CH3CO2
- ; CO2, H2O / HCO3
-
Q26. Légender le schéma du montage et préciser, en justifiant, la position et la
composition des deux phases.
Q27. Quel est le rôle du sulfate de magnésium anhydre ?
-
-
-
-
-
-
-

Q28. Déterminer la quantité de matière d’ester réellement formée nf et en déduire le rendement de la synthèse :
𝑟 = 𝑛𝑓
𝑥𝑓
(dans certains énoncés, le rendement est noté ou , à vous de vous adapter).
La phase organique obtenue ainsi que l’alcool de départ sont analysés par spectroscopie infra-rouge en phase liquide.
Les deux spectres sont donnés ci-dessous. On donne également une frise des bandes d’absorption IR de quelques
liaisons caractéristiques.
Q29. Retrouver le spectre de chacune des molécules.

Le mécanisme de la réaction d’estérification peut être décomposé en six étapes principales. Il reste valable pour les
alcools primaires et secondaires.
Etape 1 :
CH3C
OH
O+H+CH3C
OH
O+H
Etape 2 :
CH3C
OH
O+H
CH3CH
CH2CH2
CH3
OH
CH3C
OH
OH
O+
CH2CH2
CH CH3
CH3
H
+
Etape 3 :
CH3C
OH
OH
O+
CH2CH2
CH CH3
CH3
H
CH3C
OH
OH
O
CH2CH2
CH CH3
CH3
+H+
Etape 4 :
CH3C
OH
OH
O
CH2CH2
CH CH3
CH3
+H+CH3C
O+
OH
O
CH2CH2
CH CH3
CH3
H H
Etape 5 :
CH3C
O+
OH
O
CH2CH2
CH CH3
CH3
H H
CH3C
O+O
CH2CH2
CH CH3
CH3
H
+OH2
 6
6
1
/
6
100%