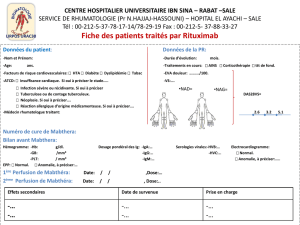
1 B. NOTICE

1
B. NOTICE

2
NOTICE
(MABTHERA flacons à 100 mg)
Veuillez lire attentivement l'intégralité de cette notice avant de prendre ce médicament.
- Gardez cette notice, vous pourriez avoir besoin de la lire à nouveau.
- Si vous avez d'autres questions, adressez-vous à votre médecin ou votre pharmacien.
- Ce médicament vous a été personnellement prescrit. Ne le donnez à personne d'autre. Vous
risqueriez de lui causer du tort, même si elle présente les mêmes symptômes que vous.
Dans cette notice:
1. Qu'est-ce que MABTHERA et dans quel cas est-il utilisé ?
2. Informations nécessaires avant de prendre MABTHERA
3. Comment prendre MABTHERA?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver MABTHERA ?
Dénomination du médicament
MABTHERA 100 mg
Rituximab
Liste complète des substances actives et des excipients
Le principe actif de MABTHERA est le rituximab. Un flacon de 10 ml contient 100 mg de rituximab.
Le flacon contient également les excipients (constituants supplémentaires) suivants : citrate de
sodium, polysorbate 80, chlorure de sodium, acide chlorhydrique, hydroxyde de sodium et eau pour
préparations injectables.
Nom et adresse du titulaire de l’autorisation de mise sur le marché et du titulaire de l’autorisation de
fabrication responsable de la libération des lots, si différent
Titulaire de l'autorisation de mise sur le marché
Le titulaire de l'autorisation de mise sur le marché est Roche Registration Limited, 40 Broadwater
road, Welwyn Garden City, Hertfordshire, AL7 3AY, Royaume-Uni.
Titulaire de l’autorisation de fabrication responsable de la libération des lots, et importateur
Hoffmann-La Roche AG, Postfach 1270, 79630 Grenzach-Wyhlen, Allemagne
1. QU'EST-CE QUE MABTHERA ET DANS QUEL CAS EST-IL UTILISÉ ?
Forme pharmaceutique et contenu; classe pharmacothérapeutique
MABTHERA est présenté sous forme d’une solution à diluer pour perfusion. Il est disponible en
flacon de 10 ml par boîte de 2 flacons. Cette solution doit être diluée avant la perfusion.
Rituximab est un anticorps monoclonal. Les anticorps monoclonaux sont des protéines qui
reconnaissent et se lient spécifiquement à une autre sorte de protéine appelée antigène. Rituximab se
lie à un antigène présent à la surface de certains globules blancs du sang, appelés lymphocytes B,
bloquant ainsi la multiplication pathologique de ces cellules.
Indications thérapeutiques
MABTHERA est utilisé pour le traitement d’un certain type de maladie affectant le système
lymphatique. Il est particulièrement utilisé en cas d’échec des autres traitements.

3
2. INFORMATIONS NÉCESSAIRES AVANT DE PRENDRE MABTHERA
Liste des informations nécessaires avant la prise du médicament
Contre-indications
Ne pas prendre Mabthera :
- s’il est connu que vous êtes allergique au rituximab ou à l'un des composants contenus dans ce
flacon ou à des protéines d'origine semblable. Votre médecin vous fournira les informations
nécessaires.
Précautions d’emploi; mises en garde spéciales
Prendre des précautions particulières avec MABTHERA :
Lorsque vous êtes traité par MABTHERA, des réactions telles que des difficultés à respirer, de la
fièvre, des frissons, des rashs et une baisse de la pression artérielle peuvent survenir. Ces effets
surviennent principalement lors de la première perfusion. Pendant les perfusions, vous serez surveillé
par le personnel médical. En cas de survenue d’une réaction, votre médecin ralentira la perfusion ou
l’arrêtera et vous donnera le traitement nécessaire. Après amélioration des symptômes, la perfusion
pourra être poursuivie. En cas de réaction grave, notamment en cas de graves difficultés respiratoires,
votre médecin arrêtera la perfusion, fera pratiquer des analyses de sang et une radiographie
pulmonaire. La perfusion ne sera pas reprise tant que votre médecin ne sera pas assuré de la
disparition complète de la réaction.
Du fait de la diminution possible de la pression artérielle au début de la perfusion, les patients prenant
des médicaments contre l’hypertension artérielle pourront être informés par leur médecin de ne pas les
prendre pendant les douze heures précédant la perfusion de MABTHERA. Si vous avez des
antécédents de maladie cardiaque (par exemple une angine de poitrine, des troubles du rythme
cardiaque ou une insuffisance cardiaque congestive) ou des antécédents de problèmes respiratoires,
votre médecin assurera une surveillance particulière tout au long du traitement par MABTHERA.
Le traitement par MABTHERA peut provoquer des anomalies du sang. De ce fait, votre médecin
procédera à des analyses de sang avant, pendant et après le traitement à intervalles réguliers.
Utilisation chez l’enfant
Actuellement, les données sont insuffisantes pour recommander l'utilisation de MABTHERA chez
l'enfant.
Utilisation pendant la grossesse et l'allaitement
Grossesse
Si vous êtes enceinte, si vous pensez être enceinte ou si vous envisagez de l’être, vous devez en parler
à votre médecin. Il discutera avec vous des risques et du bénéfice liés à la prise de MABTHERA
pendant la grossesse.
Si vous êtes une femme en âge d’avoir des enfants, vous devez prendre des mesures de contraception
efficaces pendant toute la durée du traitement par MABTHERA et pendant 12 mois après la fin du
traitement.
Allaitement
Vous ne devez pas allaiter votre enfant pendant toute la durée du traitement par MABTHERA, le
passage de ce produit dans le lait maternel n’étant pas connu.
Effets sur l’aptitude à conduire des véhicules ou à utiliser des machines
Conduite de véhicules et utilisation de machines:

4
L’effet de MABTHERA sur la capacité à conduire un véhicule ou à utiliser des machines n’est pas
connu.
Interaction avec d'autres médicaments
Prise d'autres médicaments :
Avant le début du traitement, informez votre médecin de tous les autres médicaments que vous prenez
(y compris ceux qui n’ont pas été prescrits par un médecin).
Cela est extrêmement important, car l'utilisation de plusieurs médicaments à la fois peut diminuer ou
augmenter l'effet de chaque médicament. Ainsi, MABTHERA ne doit pas être associé à d'autres
médicaments sans l'accord de votre médecin. Si, après un traitement par MABTHERA, vous êtes
traité par d’autres médicaments contenant des anticorps monoclonaux, il est possible que vous ayiez
une réaction allergique.
3. COMMENT PRENDRE MABTHERA
Instructions pour un bon usage
Posologie
Votre médecin vous prescrira avant chaque perfusion de MABTHERA, un médicament pour prévenir
et réduire douleur et/ou fièvre et allergie.
Il déterminera la dose appropriée de MABTHERA qui vous sera administrée sous forme d'une
perfusion chaque semaine pendant quatre semaines. Cette dose est fonction de votre poids et de votre
taille. Le traitement standard comprend au total 4 perfusions. Toutefois, en fonction des
caractéristiques de votre maladie ou de la réponse au traitement, votre médecin pourra modifier la
dose et/ou le nombre de perfusions.
Des traitements répétés avec MABTHERA sont possibles.
Mode et/ou voie(s) d’administration
MABTHERA est administré en perfusion intraveineuse après dilution, par du personnel médical.
Des solutions apyrogènes de sérum physiologique à 0,9% ou de sérum glucosé à 5% peuvent être
utilisées pour la dilution. La concentration finale après dilution doit être de 1 à 4 mg de rituximab par
ml de solution à perfuser.
Durée du traitement
La durée d’une cure est habituellement de 22 jours.
Utilisation de la solution après dilution.
La solution diluée de MABTHERA pour perfusion doit être utilisée immédiatement après dilution ;
elle est stable 12 heures à température ambiante. Si nécessaire, la solution diluée peut être conservée
au réfrigérateur (entre +2 °C et +8 °C) ; elle est chimiquement stable pendant 24 heures.
MABTHERA ne comporte aucun conservateur antimicrobien, ni agent bactériostatique ; aussi, toutes
les précautions nécessaires doivent être prises pour assurer la stérilité de la solution diluée.
4. QUELS SONT LES EFFETS INDÉSIRABLES ÉVENTUELS ?
Description des effets indésirables
En plus des effets recherchés, un médicament peut provoquer des effets indésirables. Plus
particulièrement durant les deux premières heures de la première perfusion, vous pouvez avoir de la
fièvre, des frissons et des tremblements. Les autres effets liés à la perfusion sont : urticaire et
démangeaison de la peau, mal au coeur, fatigue, maux de tête, , difficultés respiratoires, sensation de

5
gonflement de la langue ou de la gorge, démangeaisons, nez qui coule, vomissements, rougeur,
battements du coeur irréguliers et douleurs au niveau de la tumeur. Des problèmes cardiaques pré-
existants comme une angine de poitrine ou une insuffisance cardiaque congestive peuvent s’aggraver.
Ces réactions sont moins fréquentes lors des perfusions suivantes. MABTHERA peut aussi provoquer
des anomalies du sang et modifier la fonction hépatique. Des infections ont été observées durant et
après le traitement.
Des événements cardiaques sévères, incluant insuffisance cardiaque et infarctus du myocarde ont été
observés principalement chez les patients présentant des antécédents cardiaques et/ou ayant reçu une
chimiothérapie cardiotoxique. Ils étaient le plus souvent associés aux réactions liées à la perfusion.
Les effets indésirables suivants peuvent aussi survenir de façon rare : douleurs en particulier au niveau
de l’abdomen, du dos, du thorax, des muscles et des articulations et au point de perfusion, sensation
de malaise, gonflement abdominal, modification de la pression artérielle, modification des battements
du coeur, diarrhée, dyspepsie (digestion difficile), anorexie, anémie et troubles du système
lymphatique, pancytopénie, trouble de la coagulation sanguine, augmentation du tonus musculaire,
étourdissements, anxiété, paresthésie (une sensation anormale au niveau des extrémités telle qu’une
brûlure, une piqûre, un chatouillement, un fourmillement), hypoesthésie (diminution de la sensibilité
de la peau), agitation, insomnie (difficultés d’endormissement), nervosité, augmentation d’une toux,
sinusite (inflammation des sinus), bronchite (inflammation des poumons), herpès (infection virale),
zona (infection virale), transpiration, trouble de la sécrétion lacrymale (larmes anormales),
conjonctivites (inflammation de la surface de l’oeil), modification du goût.
Quelques cas de réactions sévères, notamment des difficultés respiratoires sévères, ainsi que des
réactions cutanées bulleuses sévères, ont été fatals. Votre médecin va donc assurer une surveillance
étroite de votre traitement et il est important que vous l’avertissiez immédiatement si vous présentez
la moindre difficulté respiratoire ou tout type de réaction cutanée.
Si vous présentez un ou plusieurs de ces effets et en particulier si vous souffrez d’un effet inattendu ne
figurant pas sur la notice, parlez-en immédiatement à votre médecin ou à votre pharmacien.
5. COMMENT CONSERVER MABTHERA ?
Conditions de conservation et date de péremption
Conservez toujours les flacons dans l'emballage d’origine et à une température comprise entre +2°C et
+8°C (au réfrigérateur).
Ne laissez ni à la portée ni à la vue des enfants.
N’utilisez pas ce produit après la date limite d’utilisation figurant sur l’emballage extérieur et sur
l’étiquette du flacon.
La dernière date à laquelle cette notice a été approuvée est le
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%