Actualités et Thérapie cellulaire dans la SEP, Pr Sandra Vukusic

Actualités thérapeutiques
et mise au point
sur les cellules souches
Pr. Sandra VUKUSIC
Service de Neurologie A et Fondation Eugène Devic EDMUS sur la Sclérose en Plaques
Observatoire Français de la Sclérose en Plaques (OFSEP)
Hôpital Neurologique Pierre Wertheimer – Hospices Civils de Lyon – France
Université Claude Bernard Lyon 1
Centre de Recherche en Neurosciences de Lyon - INSERM 1028 et CNRS UMR5292
Réseau Rhône-Alpes SEP – Journée des patients
8 octobre 2016

Déclaration Publique d’Intérêts
Sandra VUKUSIC
volontairement ci-dessous mes intérêts éventuels (au cours des 2 dernières années)*
►Activité donnant lieu à une rémunération personnelle occasionnelle
(rapport expertise, intervention ponctuelle, consultant, conférence, etc.)
Honoraires comme consultant ou pour des conférences de Biogen Idec, Geneuro, Genzyme, Merck Serono,
Novartis, Roche, Sanofi Aventis et Teva Pharma;
►Activité donnant lieu à un versement au budget d’une institution
Soutien à l’activité de recherche de Biogen Idec, Genzyme, Merck Serono, Novartis, Roche, Sanofi Aventis et
Teva Pharma.
Je soussigné :
Déclare pour la présente communication
© 2016.10.08 Actualités, Thérapie cellulaire et SEP – S. VUKUSIC

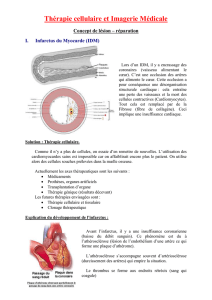
Inflammation
multifocale
aigüe, récurrente
Activité IRM
< 1/10
Poussées
> 24 heures
> 1 mois
Progression
du Handicap Irréversible
> 6 mois
Seuil Clinique
Dégénérescence
diffuse
précoce, chronique,
progressive
"SBAN"
Atrophie
RIS CIS SEP
Inflammation Dégénérescence
Une troisième composante :
l’inflammation microgliale
Evolution générale de la SEP
© 2016.10.08 Actualités, Thérapie cellulaire et SEP – S. VUKUSIC

Les formes évolutives de la SEP – Ancienne classification
Forme rémittente
Forme secondairement
progressive
Forme progressive
d’emblée
85%
15%
© 2016.10.08 Actualités, Thérapie cellulaire et SEP – S. VUKUSIC

La phase de poussées
2013 – La nouvelle classification de Lublin
La phase progressive
© 2016.10.08 Actualités, Thérapie cellulaire et SEP – S. VUKUSIC
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
1
/
32
100%