Metformine :nouvelles données pour une ancienne molécule

M. Sanduloviciu
F. R. Jornayvaz
introduction
Le traitement du diabète de type 2 a pour but de corriger l’hy-
perglycémie, de diminuer les risques de complications micro
et/ou macrovasculaires ainsi que la mortalité. Le choix du trai-
tement médicamenteux est à individualiser en fonction des
caractéristiques du patient (notamment âge, poids, comorbidités, degré d’hyper-
glycémie, adhésion au traitement) et du médicament (efficacité glycémique,
risque d’hypoglycémie, effets secondaires, bénéfice à long terme, coûts).1,2
La metformine, un biguanide excrété par le rein, est une molécule antidiabéti-
que utilisée depuis de nombreuses années, étant actuellement considérée comme
le premier choix en monothérapie selon les guidelines des sociétés européenne
et américaine du diabète, publiées en 20121 et modifiées en 2015.2
mécanisme d’action
La metformine diminue la résistance à l’insuline et n’induit pas d’hypoglycé-
mies. Elle augmente l’utilisation du glucose dans les tissus périphériques (foie et
muscle squelettique). La metformine diminue la production hépatique de glucose.3
En effet, contrairement aux sulfamides hypoglycémiants, les biguanides n’ont
aucune action insulinosécrétrice, ce qui fait que cette molécule agit indépendam-
ment de l’insuline.
In vivo, la metformine agit essentiellement au niveau du foie et du tissu mus-
culaire squelettique en augmentant l’insulinosensibilité de ces organes.
Le mécanisme d’action de la metformine est resté mal connu jusqu’ici. En effet,
l’hypothèse principale était qu’elle activait l’
AMP-actived proteine kinase
(AMPK).
Cependant, une équipe de chercheurs de l’Université de Yale a récemment mis
en évidence le mécanisme d’action de cette ancienne molécule. La metformine
inhibe l’isoforme mitochondriale de la glycérophosphate déshydrogénase
(mGPD), une enzyme qui catalyse la conversion de glycérophosphate (G3P) en
dihydroxyacétone phosphate (DHAP), avec en conséquence une réduction de la
conversion de lactate en pyruvate.4 Ainsi, l’utilisation du glycérol et du lactate
Metformin : new data for an old molecule
Metformin is the first-line oral agent for the
treatment of type 2 diabetes according to the
guidelines. Metformin decreases hepatic glu-
cose production, does not induce weight gain
and does not increase the risk of hypoglyce-
mia. However, decades after its introduction,
its mode of action has been only recently high-
lighted. The side effects of metformin are
well known and consist primarily of digestive
problems. Although rare, the dreaded com-
plication is lactic acidosis, which can develop
in patients with severe renal insufficiency or in
conditions of low perfusion. The purpose of
this article is to review the indications, risks
and benefits of this drug, but also to discuss
new evidence related to its mechanism of ac-
tion and the conditions that increase the risk
of lactic acidosis.
Rev Med Suisse 2015 ; 11 : 1222-6
La metformine est l’agent oral de première intention pour le trai-
tement du diabète de type 2 selon les guidelines. La metformine
diminue la production hépatique de glucose, n’induit pas de
prise de poids et n’augmente pas le risque d’hypoglycémie.
Cependant, plusieurs décennies après son introduction, son
mode d’action n’a été que très récemment mis en évidence.
Les effets secondaires de la metformine sont bien connus et
consistent essentiellement en des problèmes digestifs. Bien
que rare, la complication redoutée est l’acidose lactique, qui
peut apparaître notamment en cas d’insuffisance rénale sévère
ou dans des conditions d’hypoperfusion. Le but de cet article
est de revoir les indications thérapeutiques, les risques et bé-
néfices de ce médicament antidiabétique, mais aussi de discu-
ter de nouvelles évidences en lien avec son mécanisme d’action
et des conditions augmentant le risque d’acidose lactique.
Metformine : nouvelles données
pour une ancienne molécule
mise au point
1222 Revue Médicale Suisse
–
www.revmed.ch
–
3 juin 2015
Drs Maria Sanduloviciu
et François R. Jornayvaz
Service d’endocrinologie,
diabétologie et métabolisme
CHUV, 1011 Lausanne
06_10_38623.indd 1 28.05.15 09:31

Revue Médicale Suisse
–
www.revmed.ch
–
3 juin 2015 1223
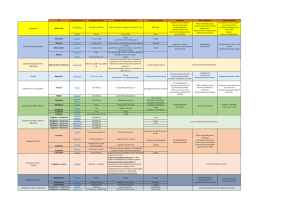
comme substrats pour la néoglucogenèse diminue et la
concentration de glycérol et lactate augmente dans le plas-
ma (figure 1).4,5
indications thérapeutiques et action
de la metformine
Selon le
Compendium suisse des médicaments
, la metformine
est indiquée dans le traitement du diabète de type 2,
lorsque le régime alimentaire et l’activité physique ne suf-
fisent pas à normaliser la glycémie. En pratique, il est fré-
quent d’introduire directement un antidiabétique oral en
complément aux mesures hygiénodiététiques, car rares sont
les patients suffisamment motivés pour être traités par ces
mesures seules. Cela dépend bien entendu aussi de l’HbA1c
de base.
Une autre indication de la metformine, moins connue, est
son ajout en complément d’une insulinothérapie dans le
diabète de type 1, notamment en présence d’une résistan ce
à l’insuline. Cependant, cette approche a fait l’objet de peu
d’études et cette indication ne devrait être posée qu’avec
prudence après avis spécialisé.
De manière similaire, l’emploi de la metformine dans le
diabète gestationnel doit faire l’objet d’une évaluation spé-
cialisée et d’une décision partagée. Pour un groupe de pa-
tientes bien sélectionnées, la metformine est une alterna-
tive intéressante à l’insuline (injectable et qui peut parfois
engendrer une prise pondérale et un risque accru d’hypo-
glycémie). Toutefois, il faut avertir du passage transplacen-
taire de la metformine dont l’impact sur le développement
fœtal et les effets à long terme ne sont pas connus.
effets sur la glycémie
La metformine peut être utilisée en monothérapie ou
avec d’autres antidiabétiques oraux ou l’insuline. En mono-
thérapie, la metformine permet une baisse de la glycémie
à jeun d’environ 20% et une réduction de l’HbA1c de 1 à 2%,
ce qui est similaire à l’efficacité des sulfonylurées.6,7 Pour
atteindre un contrôle glycémique optimal, il est possible
de l’associer avec d’autres antidiabétiques tels que les
sulfonylurées, les glinides, les inhibiteurs de l’alphagluco-
sidase, la pioglitazone, les inhibiteurs du sodium-glucose
cotransporteur 2 (SGLT2), les agonistes du récepteur au
glucagonlike peptide-1 (GLP-1), les inhibiteurs de la dipep-
tidyl-peptidase IV (DPP4 ; gliptines), ou l’insuline.
Le risque d’hypoglycémie est quasi nul chez le patient
qui prend seulement la metformine dans des circonstan-
ces normales, mais l’hypoglycémie peut survenir si l’apport
énergétique est insuffisant, si le patient se livre à des exer-
cices intenses sans s’assurer d’un apport calorique supplé-
mentaire ou s’il prend simultanément un autre agent anti-
diabétique ou de l’alcool.
effet sur le poids
Chez les obèses, la metformine favorise une réduction
pondérale modeste ou une stabilisation pondérale, con-
Figure 1. Mécanisme d’action de la metformine
(Adaptée de réf.5).
mGPD: glycérol-phosphate déshydrogénase isoforme mitochondriale ; cGPD : glycérol-phosphate déshydrogénase isoforme cytoplasmique ; G3P : glycérol-
3-phosphate ; LDH : lactate déshydrogénase ; DHAP : dihydroxycétone phosphate ; NAD : nicotinamide adénine dinucléotide ; NADH : forme réduite de la
nicotinamide adénine dinucléotide.
mGPD
QDHAP QDHAP
QGlucose
Amino acides Alanine Lactate
Plasma
LDH
qLactate
QNAD
QPyruvate
cGPD
qG3P qG3P
qNADH
Glycérol
06_10_38623.indd 2 28.05.15 09:31

trairement au gain pondéral associé à l’insuline ou au trai-
tement par sulfonylurées.7
effets sur l’incidence de cancers
La littérature médicale rapporte régulièrement une as-
sociation entre le diabète, en particulier de type 2, et le
cancer, principalement sur la base d’études observationnel-
les.8,9 Les hypothèses proposées pour cette relation entre
diabète et cancers sont l’hyperglycémie clinique et/ou l’in-
sulinorésistance et l’hyperinsulinémie compensatoire.8 En
même temps, les données convergent pour suggérer que
l’utilisation de la metformine diminue l’incidence de diffé-
rents cancers, probablement en réduisant l’hyperglycémie
et surtout l’hyperinsulinémie.8
D’autre part, la metformine agit sur les voies de signa-
lisation cellulaires comme l’AMPK qui est connue pour
stimuler des suppresseurs de tumeur comme le LKB1, ou
pour inhiber la protéine mTOR
(mammalian Target of rapa-
mycin)
qui est un puissant facteur de croissance et de pro-
lifération.9
Des méta-analyses portant principalement sur des études
cas-témoin et de cohorte effectuées chez des patients at-
teints de diabète de type 2 montrent que l’utilisation de la
metformine (comparativement à une absence de traitement
ou à d’autres traitements antidiabétiques) est associée à un
risque réduit de survenue de tous cancers confondus et de
mortalité par cancer.8,9 Cependant, ces effets restent con-
troversés et des études prospectives manquent.
effets cardiovasculaires
La possibilité que la metformine puisse réduire le ris-
que cardiovasculaire (CV) a été mise en évidence par l’étude
prospective conduite au Royaume-Uni sur le diabète de
type 2 (UK Prospective Diabetes Study, UKPDS), qui a mon-
tré une réduction du risque d’infarctus du myocarde et de
la mortalité toutes causes confondues.10 Des analyses épi-
démiologiques ultérieures ont confirmé un avantage cardio-
vasculaire, mais les données cliniques ne sont cependant
pas très solides.
Ainsi, en raison de ces différentes propriétés, la metfor-
mine a été choisie pour être le pilier pharmacologique du
traitement du diabète de type 2, même si l’évidence der-
rière ce choix n’est pas des plus solides. Les sociétés euro-
péenne et américaine du diabète ont donc sorti des re-
commandations dans ce sens en 2012, qui ont été mises à
jour en 2015. Ces dernières sont présentées dans le ta-
bleau 1.
effets indésirables
Effets secondaires digestifs
L’inconvénient principal de la metformine est sa relati-
vement mauvaise tolérance digestive (nausées, crampes
épigastriques, inconfort abdominal, diarrhées) que l’on peut
réduire si l’on tient compte des recommandations suivan tes :
• commencer par un ou deux comprimés à 500 mg par jour
et augmenter progressivement (après environ une semaine)
à 1000 mg deux fois par jour (matin et soir) ;
• conseiller au patient de prendre les comprimés pendant
ou à la fin du repas.
La dose efficace habituelle est de 1500 à 2000 mg par
jour. La dose maximale de 3000 mg par jour (1000 mg trois
fois par jour) ne permet pas d’améliorer significativement le
contrôle glycémique mais augmente les effets secondaires
gastro-intestinaux. Actuellement, on dispose de comprimés
à libération prolongée (XR) (mais uniquement sous forme
combinée avec une gliptine sur le marché suisse), ce qui
permet de réduire les effets digestifs.11
Risque d’acidose lactique
L’acidose lactique est une complication métabolique rare,
mais grave, qui résulte d’une accumulation d’acide lacti que
consécutive à l’administration de metformine en présence
de tout état caractérisé par une hypoperfusion et une hy-
poxémie tissulaires notables. La mortalité de l’acidose lac-
tique peut atteindre 50%.
Les symptômes et les signes incluent, dans les cas
graves, des nausées et des vomissements, une léthargie et
une polypnée. Le diagnostic est clinique et biologique. Sur
le plan biologique, l’acidose lactique se définit par l’éléva-
tion de la concentration sanguine de lactate (L 5 mmol/l),
la diminution du pH sanguin, le déséquilibre électrolytique
comportant une augmentation de la valeur du trou anioni-
que, et l’élévation du rapport lactate/pyruvate.12 Cependant,
en cas de traitement par metformine, la présence d’une
concentration plasmatique de lactate à jeun supérieure à
5 mmol/l ne témoigne pas nécessairement d’une acidose
lactique imminente et peut être imputable à d’autres cau-
ses, notamment au mauvais équilibre du diabète, à l’obé-
sité, à une activité physique vigoureuse, ou à des problè-
mes techniques relatifs au dosage du lactate. En l’absence
de signes d’acidocétose (cétonurie ou cétonémie), la pré-
sence d’une acidose métabolique chez tout patient diabé-
tique sous metformine doit faire soupçonner celle d’une
acidose lactique.
Chez les patients sous metformine, la fréquence décla-
rée d’acidose lactique est très faible (environ 0,03 cas pour
1000 patients-année, et environ 0,015 décès pour 1000 pa-
tients-année).13
Le risque d’acidose lactique augmente surtout avec la
gravité de la dysfonction rénale et l’âge du patient. Une ré-
cente revue systématique a montré que les données dis-
ponibles étaient limitées pour évaluer le risque d’acidose
lactique chez des patients insuffisants rénaux chroniques
traités par metformine, et qu’aucune étude randomisée con-
trôlée n’avait été conduite pour évaluer la sécurité de la
metformine dans l’insuffisance rénale.13 Des données obser-
vationnelles étayent un potentiel bénéfique de la met-
formine sur les complications macrovasculaires, même chez
les patients avec insuffisance rénale avancée. Ainsi, l’éviden-
ce disponible supporte l’utilisation de la metformine dans
l’insuffisance rénale légère et modérée.13 Une réduction
des doses de metformine est à préconiser en fonction du
déclin de la fonction rénale (tableau 2).
Le risque d’acidose lactique est aussi plus élevé chez
les patients souffrant de maladie hépatique, ainsi que dans
des conditions entraînant un risque d’hypoperfusion ou
d’hypoxémie (insuffisance cardiaque, sepsis, décompensa-
1224 Revue Médicale Suisse
–
www.revmed.ch
–
3 juin 2015
06_10_38623.indd 3 28.05.15 09:31

Revue Médicale Suisse
–
www.revmed.ch
–
3 juin 2015 1225
tion respiratoire, déshydratation). Le principe de précaution
veut donc que le traitement de metformine soit interrompu
sans délai en cas d’hypoxémie, sepsis et bien entendu
d’insuffisance rénale aiguë consécutive ou non à une dés-
hydratation. De plus, il faut conseiller aux patients traités
par metformine d’éviter toute consommation excessive
d’alcool, car la prise d’alcool entraîne la potentialisation du
métabolisme du lactate.
Risque de déficit en vitamine B12
Des troubles de l’absorption de la vitamine B12 ont été
mis en évidence chez 10 à 30% des patients traités par
metformine.14 Cependant, cette carence ne cause que très
rarement une anémie et se corrige rapidement à l’arrêt du
traitement ou à la prise de suppléments de vitamine B12.
Par contre, ce déficit peut causer une neuropathie périphé-
rique d’ailleurs très similaire à la neuropathie périphéri que
due au diabète lui-même. Par conséquent, le dosage séri-
que de la vitamine B12 est conseillé chez les patients sous
metformine au long cours, probablement tous les ans. Il
n’existe à l’heure actuelle pas de recommandation spéci-
fique concernant le dépistage et la correction du déficit en
vitamine B12 chez les patients sous metformine au long
cours, il convient donc d’appliquer les recommandations
habituelles de subsitution en cas de déficit en vitamine
B12.14
metformine et produits de contraste
Il faut suspendre temporairement le traitement de met-
formine avant tout examen radiologique comportant une
injection de produit de contraste. Le risque est la survenue
d’une acidose lactique en cas d’insuffisance rénale induite
par le produit de contraste. Dans ce cas, bien que les re-
Tableau 1. Guidelines ADA/EASD pour la prise en charge médicamenteuse du diabète de type 2
(Adapté de réf.2).
1re étape Modification du style de vie r monothérapie : metformine
• Efficacité • Elevée
• Risque d’hypoglycémie • Faible
• Effet sur poids • Neutre/perte pondérale
• Effets indésirables • Gastro-intestinaux/acidose lactique
• Coût • Faible
Si HbA1c cible n’est pas atteinte après 3 mois passer à l’étape 2 (bithérapie)
2e étape Modification du style de vie r bithérapie : metformine r
Sulfonylurée Inhibiteur SGLT2 Inhibiteur DDP4 Analogue GLP1 Thiazolidinedione Insuline
• Efficacité • Elevée • Intermédiaire • Intermédiaire • Elevée • Elevée • La plus élevée
• Risque d’hypoglycémie • Haut • Faible • Faible • Faible • Faible • Haut
• Effet sur poids • Prise pondérale • Perte pondérale • Neutre • Perte pondérale • Prise pondérale • Prise pondérale
• Effets indésirables • Hypoglycémie • Infection génito- • Rares • Gastro-intestinaux, • œdème/insuffisance • Hypoglycémie
urinaire/ nausées cardiaque/fractures
déshydratation
• Coût • Faible • Elevé • Elevé • Elevé • Faible • Variable
Si HbA1c cible n’est pas atteinte après 3 mois passer à l’étape 3 (trithérapie)
3e étape Modification du style de vie r trithérapie : bithérapie r
Inhibiteur Inhibiteur Analogue Thiazolidine- Insuline Sulfonylurée
SGLT2 ou DDP4 ou GLP1 ou dione ou ou
Si HbA1c cible n’est pas atteinte après 3 mois passer à l’étape 4
4e étape Modification du style de vie r metformine r multiples injections :
Insuline basale Insuline aux repas Analogue GLP1
Stade de eGFR (ml/min Posologie journalière Remarques
l’atteinte rénale pour 1,73 m2) maximale en mg
(classification
KDIGO 2012)
G1 L 90 3000 L 2000 mg peu d’efficacité supplémentaire par rapport aux effets indésirables digestifs
G2 60-l90 3000
G3a 45-l60 1500 Surveillance de la fonction rénale. Arrêter si risque de péjoration de la fonction
rénale
G3b 30-l45 Arrêter Selon guidelines suisses
G4 30-15 Ne pas utiliser
G5 l15 Ne pas utiliser
Tableau 2. Adaptation de la posologie de metformine selon la fonction rénale (recommandations suisses)
Adapté de réf.16).
06_10_38623.indd 4 28.05.15 09:31

commandations diffèrent selon les sociétés savantes, on
préconise de suspendre la metformine le jour de l’examen
(la veille si forme XR de metformine), et de reprendre la
metformine 48 heures plus tard si la fonction rénale le per-
met.15
conclusion
En l’absence de contre-indications, la metformine re-
présente donc le premier choix thérapeutique dans le trai-
tement du diabète de type 2, en raison de son efficacité
élevée (diminution de l’HbA1c), de son faible risque
d’hypoglycémie, de son effet neutre sur le poids, de son
potentiel bénéfice sur la réduction des risques cardiovas-
culaires, et de son faible coût.
1226 Revue Médicale Suisse
–
www.revmed.ch
–
3 juin 2015
Les auteurs n’ont déclaré aucun conflit d’intérêts en relation avec
cet article.
Implications pratiques
La metformine peut être instaurée en première intention
au moment du diagnostic de diabète de type 2, en parallèle
aux recommandations de modifications du style de vie
La metformine devrait être titrée en débutant par 500 mg
une à deux fois par jour jusqu’à la dose efficace maximale
tolérée, soit généralement 2000 mg par jour, à prendre
lors des repas. La forme retard est une alternative pour les
patients avec des symptômes digestifs importants. Si les
objectifs glycémiques ne sont pas remplis, la metformine
peut être combinée avec d’autres traitements antidiabé-
tiques selon les recommandations de l’ADA/EASD
Il convient de suspendre la metformine le jour d’un examen
avec produit de contraste et de la reprendre 48 heures
plus tard si la fonction rénale le permet
La metformine a un très faible risque d’hypoglycémie. Ce-
pendant, cet effet indésirable peut toutefois se produire en
cas d’apport alimentaire insuffisant, surtout associé à une con-
sommation d’alcool ou en cas d’activité physique intense et
prolongée, ou en cas d’association avec d’autres antidiabé-
tiques oraux
L’acidose lactique reste rare et est en principe liée à des
facteurs de risque tels qu’insuffisance rénale, insuffisance
cardiaque, insuffisance hépatique, insuffisance respiratoire et
alcoolisme
En cas d’insuffisance rénale, il convient de réduire les doses
de metformine lorsque la clairance de la créatinine passe en
dessous des 60 ml/min, et d’arrêter la metformine si elle
est inférieure à 45 ml/min
>
>
>
>
>
>
1 Inzucchi SE, Bergenstal RM, Buse JB, et al. Manage-
ment of hyperglycemia in type 2 diabetes : A patient-
centered approach: Position statement of the Ameri-
can Diabetes Association (ADA) and the European As-
sociation for the Study of Diabetes (EASD). Diabetes
Care 2012;35:1364.
2 ** Inzucchi SE, Bergenstal RM, Buse JB, et al. Ma-
nagement of hyperglycemia in type 2 diabetes, 2015 : A
patient-centered approach : Update to a position sta-
tement of the American Diabetes Association and the
European Association for the Study of Diabetes. Dia-
betes Care 2015;38:140-9.
3 McIntyre HD, Ma A, Bird DM, et al. Metformin in-
creases insulin sensitivity and basal glucose clearance in
type 2 (non-insulin dependent) diabetes mellitus. Aust
N Z J Med 1991;21:714.
4 * Madiraju AK, Erion DM, Rahimi Y, et al. Metfor-
min suppresses gluconeogenesis by inhibiting mitochon-
drial glycerophosphate dehydrogenase. Nature 2014;
510:542.
5 Ferrannini E. The target of metformin in type 2 dia-
betes. N Engl J Med 2014;371:1547.
6 Hermann LS, Scherstén B, Bitzén PO, et al. Thera-
peutic comparison of metformin and sulfonylurea,
alone and in various combinations. A double-blind
controlled study. Diabetes Care 1994;17:1100.
7 * Hemmingsen B, Schroll JB, Wetterslev J, et al.
Sulfonylurea versus metformin monotherapy in patients
with type 2 diabetes : A Cochrane systematic review
and meta-analysis of randomized clinical trials and trial
sequential analysis. CMAJ Open 2014;2:E162.
8 Libby G, Donnelly LA, Donnan PT, et al. New users
of metformin are at low risk of incident cancer : A cohort
study among people with type 2 diabetes. Diabetes
Care 2009;32:1620.
9 Landman GW, Kleefstra N, van Hateren KJ, et al.
Metformin associated with lower cancer mortality in
type 2 diabetes : ZODIAC-16. Diabetes Care 2010;33:
322.
10 United Kingdom Prospective Diabetes Study
(UKPDS). Effect of intensive blood-glucose control with
metformin on complications in overweight patients
with type 2 diabetes (UKPDS 34). Lancet 1998;352:854.
11 Neutel JM1, Zhao C, Karyekar CS. Adding saxa-
gliptin to metformin extended release (XR) or uptitration
of metformin XR : Efficacy on daily glucose measures.
Diabetes Ther 2013;4:269-83.
12 Lalau JD. Lactic acidosis induced by metformin : In-
cidence, management and prevention. Drug Saf 2010;
33:727.
13 * Inzucchi SE, Lipska KJ, Mayo H, et al. Metformin
in patients with type 2 diabetes and kidney disease : A
systematic review. JAMA 2014;312:2668.
14 de Jager J, Kooy A, Lehert P, et al. Long term treat-
ment with metformin in patients with type 2 diabetes
and risk of vitamin B-12 deficiency : Randomised placebo
controlled trial. BMJ 2010;340:c2181.
15 Goergen SK, Rumbold G, Compton G, Harris C.
Systematic review of current guidelines, and their evi-
dence base, on risk of lactic acidosis after administra-
tion of contrast medium for patients receiving metfor-
min. Radiology 2010;254:261.
16 * Zanchi A, Lehmann R, Philippe J. Antidiabetic
drugs and kidney disease-recommendations of the Swiss
Society for Endocrinology and Diabetology. Swiss Med
Wkly 2012;142:w13629.
* à lire
** à lire absolument
Bibliographie
06_10_38623.indd 5 28.05.15 09:31
1
/
5
100%