Microsoft PowerPoint - UE 2.1-Master_IADE_4 [Mode de compatibilit

Approfondissement des
connaissances en biologie
moléculaire
Master IADE – Année 2013-2014

Plan du cours
•Rappels de biologie moléculaire et de biologie
cellulaire
–Les molécules du vivant
–Le support de l’information génétique et son décodage
–L’organisation de la cellule animale
•Les outils et les approches expérimentales utilisées
par les chercheurs
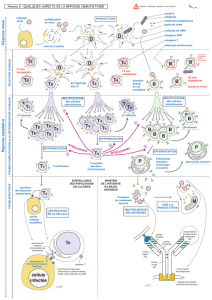
•Les mécanismes qui permettent aux cellules de
communiquer entre elles

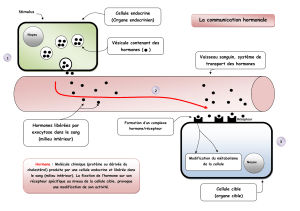
Les mécanismes qui permettent aux
cellules de communiquer entre elles
Master IADE – Année 2013-2014

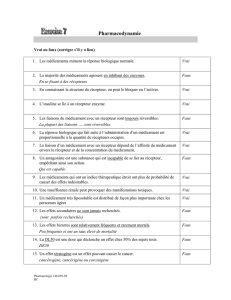
Pourquoi cela concerne votre pratique : les
médicaments utilisés en anesthésie
•Gaz et halogènes: N20, isoflurane,...
•Hypnotiques: Etomidate, Propofol,...
•Benzodiazépines: Diazépam, Midazolam, Dormicum, Hypnovel
•Morphinomimétiques agonistes: Morphine, Sufentanil,....
•Morphinomimétiques antagonistes: Naloxone,...
•Myorelaxants: Iodure de suxaméthium, curares
•Anesthésiques locaux: Lidocaine,...
•Sympathomimétiques: Epinéphrine, Nicardipine,...

Les cibles des médicaments utilisés en
anesthésie
•Récepteurs αet βadrénergique : sympathomimétiques
•Récepteur de l’acide γ amino butytirique (GABA):
benzodiazépines, barbituriques, anesthésiques volatils,
anesthésiques intraveineux
•Récepteur du glutamate (NMDA) : kétamine
•Récepteur nicotinique de l’acétylcholine (NMDA) : curares
•Récepteurs des opiacés : morphinomimétiques
•Récepteur des glucocorticoïdes: dexaméthasone
•Canaux sodium dépendants du voltage: lidocaine
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
1
/
30
100%