Les effets secondaires des nouveaux traitements anti

Les effets secondaires des nouveaux traitements anti-cancéreux.
Dr Jean-Pierre Delord
Institut Claudius Regaud
Laboratoire de pharmacologie clinique et expérimentale des médicaments anti-cancéreux.
Toulouse
Les progrès réalisés dans la connaissance fondamentale des processus de l’oncogénèse se
traduisent actuellement par l’apparition de nouvelles classes thérapeutiques en cancérologie. Ces
nouveaux médicaments sont appelés « thérapeutiques ciblées ».
Ce terme « thérapeutique ciblée » désigne des molécules dirigées contre des cibles moléculaires
présentes et jouant un rôle dans la transformation néoplasique de la cellule cancéreuse. Il ne s’agit
pas d’un concept nouveau en oncologie. Les traitements hormonaux des cancers du sein et de la
prostate par exemple correspondent à des thérapeutiques ciblées selon cette définition, et sont
étudiés depuis longtemps. Cependant, de très nombreux traitements innovants deviennent utilisables
en clinique. Ils peuvent avoir comme cible :
- une néo-protéine résultant d’une anomalie moléculaire causale, directement responsable
de la transformation néoplasique
- un oncogène impliqué dans progression tumorale
- une ou plusieurs cibles du micro-environnement tumoral
Pour obtenir l’inhibition pharmacologique d’une ou plusieurs cibles, deux grandes classes de
molécules sont utilisées :
- les anticorps monoclonaux, en partie ou totalement humanisés
- les « petites molécules »
Exemples :
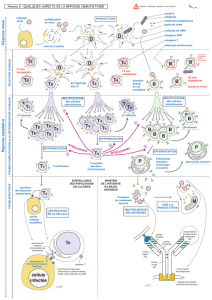
Figure 1 : transduction du signal de prolifération à partir d’un oncogène membranaire (récepteur à un
signal de croissance)

Figure 2 : représentation schématique des classes thérapeutiques inhibant ce récepteur
Ces médicaments interagissent avec les protéines tumorales en bloquant leur activité « kinase ».
Les effets secondaires de ces molécules sont donc très différents de la chimiothérapie cytotoxique
traditionnelle. En particulier, les risques de toxicité hématologique et de leuco-neutropénie sont
souvent presque inexistants.
Globalement les effets secondaires attendus dépendent désormais :
- de la classe pharmacologique : les anticorps monoclonaux partiellement humanisés
(injectables) font courir aux patient un risque immédiat de réaction anaphylactique et de
fièvre. Les petites molécules (administrées par voie orale) ont des effets secondaires que
nous pouvons qualifier de non spécifique (essentiellement mucite et diahhée)
- surtout, du mécanisme d’action de la molécule : voici quelques exemples
1. les inhibiteur de la protéine EGF-R (Epidermal Growth Factor : facteur de croissance des
épidermes) ont essentiellement des effets secondaires cutanés (cette protéine étant
exprimée anormalement dans certains cancers, mais présente de façon physiologique
dans les couches basales de l’épiderme). Il convient de connaître ces effets secondaires
s’exprimant souvent sous la forme d’une réaction érythémateuse maculo-pustulo-
papulaire du visage qui n’est ni une allergie ni de l’acné. Le traitement de ces anomalies
repose essentiellement sur une hydratation de la peau et les anti-inflammatoires cutanés.
2. les inhibiteurs de HER-2 (récepteur de la famille des EGFR) sur-exprimé dans certaines
cancers du sein. L’inhibition pharmacologique de ce récepteur n’a quasiment aucun effet
secondaire immédiat dans la mesure où ce récepteur est très peu exprimé dans les tissus
sains chez l’adulte. Par contre, HER2 est impliqué dans l’organogénèse, en particulier
cardiaque. Les inhibiteurs de HER2 nécessitent donc une surveillance cardiaque
particulière car ils peuvent accentuer les effets secondaires liés à la chimiothérapie sur la
fonction cardiaque.
3. les inhibiteurs de l’angiogénèse tumorale. Ces traitement ont un effet anti-tumoral par une
destruction plus ou moins complète des vaisseaux sanguins tumoraux. Ces molécules

interagissent avec de grands mécanismes physiologiques de l’homéostasie vasculaire. Ils
peuvent donc être responsables de l’apparition :
o d’hypertension artérielle nécessitant une prise en charge symptomatique
o de protéinurie souvent asymptomatique
o d’un risque plus élevé de phénomènes thrombotiques et hémorragiques
o d’effet secondaire multiples dont la physiopathologie n’est pas élucidée : asthénie,
troubles des phanères, hypothyroïdie, etc.
Il est vraiment rare que ces nouveaux traitement soient à l’origine d’effets secondaires exposant les
patients à un risque vital (comme par exemple la neutropénie). Ces traitements exposent plutôt les
patients à des effets secondaires apparaissant comme des toxicités « chroniques ». Leur prise en
charge dépend donc du contexte clinique, du bénéfice thérapeutique attendu et de l’avis des patients,
souvent important pour des effets secondaires cutanés par exemple. La gestion de ces toxicités
chroniques impliquera nécessairement plus les médecins de famille.
1
/
3
100%