CM2_Poly2_TP Géométrie des Molécules

CH7/CM2
CH7/CM2 CH7/CM2
CH7/CM2
–
––
–
T
TT
TP
P P
P
–
––
–
Géométrie des Molécules
Géométrie des MoléculesGéométrie des Molécules
Géométrie des Molécules
–
––
– 1/2
1/2 1/2
1/2
Qu’est
Qu’estQu’est
Qu’est-
--
-ce qu’un
ce qu’unce qu’un
ce qu’une molécule
e moléculee molécule
e molécule
?
??
?
Assemblage chimique électriquement neutre de plusieurs atomes
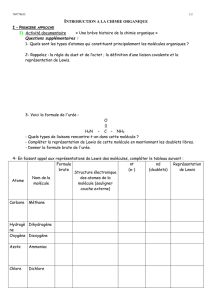
L’objectif de cette application est de trouver la représentation de Lewis, ainsi que la géométrie de quelques molécules
Quelques exemples qui nous entourent
Quelques exemples qui nous entourentQuelques exemples qui nous entourent
Quelques exemples qui nous entourent
:
::
:
P
PP
Premières questions
remières questionsremières questions
remières questions
:
::
:
Vous disposez d’une boîte avec des boules de différentes couleurs, présentant différentes géométries de trous.
1. Reproduire les molécules présentées ci-dessus, et commenter leur géométrie.
2. Pourquoi la molécule de CO
2
est-elle linéaire, alors que la molécule de H
2
O est coudée ?
3. Quelle est la différence de géométrie entre le dioxygène O
2
et le diazote N
2
?
4. Justifier la disposition des trous sur les boules de la boîte.
Etab
EtabEtab
Etablir la formule de Lewis
lir la formule de Lewislir la formule de Lewis
lir la formule de Lewis
?
??
?
Comment établir la formule de Lewis d’une molécule : On illustre la méthode sur un exemple simple
On cherche la formule de Lewis de l’éthanol C
2
H
5
OH
Etapes
EtapesEtapes
Etapes
:
::
:
Exemple
ExempleExemple
Exemple
:
::
:
Partir de la formule brute
2 6
C H O
, ou
3 2
CH CH OH
(plus d’info)
Représenter chaque atome avec sa couche de valence
(voir chapitre précédent – structure de l’atome)
En déduire la covalence de chaque atome
(nombre de liaisons qu’ils peuvent faire) C = 4 / H = 1 / O = 2
Compter le nombre total d’électrons
(Attention aux ions Ajouter ou soustraire la charge)
2 4 6 1 1 6 20
n
= × + × + × =
Associer les atomes en respectant la covalence
(c'est-à-dire en respectant la règle de l’octet)
Vérifier le nombre total d’électrons 10 doublets 20 électrons
Calculer la charge formelle de chaque atome
(Comparer la charge de l’atome seul / dans la molécule) Ici, pas de charges formelles (voir TD)
H
HH
H
C
CC
C
O
OO
O
H
HH
H
C
CC
C
O
OO
O
H
HH
H
H
HH
H
C
CC
C
H
HH
H
H
HH
H
H
HH
H
Dioxyde de
Carbone CO
2
L’eau H
2
O
Méthane
C
H
4
Dioxygène O
2
Diazote N
2

CH7/CM2
CH7/CM2 CH7/CM2
CH7/CM2
–
––
–
T
TT
TP
P P
P
–
––
–
Géométrie des Molécules
Géométrie des MoléculesGéométrie des Molécules
Géométrie des Molécules
–
––
– 2
2 2
2/2
/2/2
/2
En déduire la géométrie de la molécule
En déduire la géométrie de la moléculeEn déduire la géométrie de la molécule
En déduire la géométrie de la molécule
?
??
?
Selon le nombre de liaisons qui entourent les atomes
Reproduire cette molécule…
Application à d’autres exemples
Application à d’autres exemplesApplication à d’autres exemples
Application à d’autres exemples
5. Pour chacune des molécules suivantes
Donner sa représentation de Lewis
Préciser la géométrie des atomes de Carbone, d’azote et d’oxygène
Réaliser la molécule avec les modèles
Avec des liaisons simples uniquement :
a. L’éthane : C
2
H
6
(un gaz naturel)
b. Le propane : C
3
H
8
(un autre gaz naturel)
c. Le méthanol : CH
4
O (un alcool)
Avec des liaisons doubles :
d. L’acide méthanoïque : HCOOH (un acide)
e. L’acide éthanoïque : CH
3
COOH (un autre acide)
f. L’éthylène : C
2
H
4
g. Le propylène : C
3
H
6
h. Un autre acide :
HCONH
2
Avec des liaisons triples :
i. L’éthyne : C
2
H
2
j. Le propyne : C
3
H
4
Autres molécules :
k. Le chlorure de Carbonyle : COCl
2
l. Le chlorure de vinyle : C
2
H
3
Cl
m. Le méthylamine : CH
3
NH
2
H
HH
H
C
CC
C
O
OO
O
H
HH
H
H
HH
H
C
CC
C
H
HH
H
H
HH
H
H
HH
H
Entouré de 4 doublets
Structure tétraédrique
Entouré de 4 doublets
Structure tétraédrique
Entouré de 4 doublets
Structure tétraédrique
1
/
2
100%