étude cinétique d`une réaction ( 7,5 points)

étude cinétique d'une réaction ( 7,5 points)
On considère la réaction entre un ester et l'ion hydroxyde, qui conduit à
la formtion d'un alcool et d'un ion
carboxylate.
1. Etude de la réaction : l'équation générale de la réaction est : ester + HO-=
alcool + ion carboxylate
- De quelle réaction s'agit-il ?
- Est-elle totale/ limitée ?
- Est-elle lente / rapide ?
- Ecrire l'équation entre l'éthanoate d'éthyle et l'hydroxyde de sodium. Nommer les produits.
- Donner le mécanisme de la réaction.
- Citer une application industrielle de la saponification.
2. Cinétique de la réaction :
- Exprimer la vitesse de disparition de l'ester en fonction des concentrations des ré
actifs. On note k, la
constante de vitesse, a : l'ordre partiel par rapport à l'ester; b : l'ordre partiel par rapport à
l'ion hydroxyde.
- Afin de dé
terminer l'ordre a, on fixe le pH de la solution en utilisant des ions polyphosphates. Le pH reste
constant pendant l'étude cinétique. Que peut-on dire de la concentration des ions HO-
au cours du temps ?
Réécrire l'expression de la vitesse de disparition de l'ester en notant k' la constante apparente.
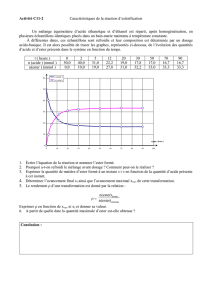
- On obtient les résultats suivants :
Vérifier que ln(ester) est une fonction affine du temps. Que peut-on en dé
duire sur la valeur de a
Déterminer graphiquement k'.
Définir le temps de demi-réaction et déterminer sa valeur.
Comment varie le temps de demi-réaction si on refait l'expérience à 60°C ?
corrigé
saponification, lente, totale
CH3COO-C2H5+ NaOH = CH3COONa + C2H5OH
les produits sont l'alcool éthylique et l'éthanoate de sodium
mécanisme : attaque du nucléophile HO-sur le carbone du groupe ester ( étape lente dé
terminante).
puis rapidement il se forme un acide caboxylique et un ion alcoolate
enfin on passe rapidement à l'ion carboxylate et à l'alcool
application industrielle : fabrication des savons.
vitesse v = -d[ester]/dt = -k[ester]a[HO-]b.
si le pH reste constant alors [HO-]= 10-14 / [H3O+]= 10-14 / 10-pH = constante.
vitesse v = -d[ester]/dt = -k'[ester]a.
T en h 0 2 5 10 20 30 40
[ester] mmol/L 10 8,7 7,1 5 2,5 1,25 0,6
T en h 0 2 5 10 20 30 40
Corrig
é
BTS Analyses Biologiques 2004 Sciences Physiques
-
http://www.chimix.com
-
CHIMIX
T
é
l
é
charg
é
sur http://www.aidexam.com

Le temps de demi-réaction est la durée au bout de laquelle le taux d'avancement final est égale à
0,5. Dans ce cas,
c'est la durée au bout de laquelle la moitié du réactif limitant, l'ester, a disparu. D'aprè
s le tableau on trouve 10
heures.
La vitesse de la réaction croît avec la température ; en conséquence le temps de demi-ré
action diminue si la
température augmente.
[ester] mol/L 10 10-3 8,7 10-3 7,1 10-3 5 10-3 2,5 10-3 1,25 10-3 0,6 10-3
ln[ester] - 4,6 - 4,74 - 4,95 - 5,3 -6 - 6,68 - 7,42
www.be
-
mev.com
Commentaires
étude thermodynamique de la complexation des ions Cu(II)
(4 points)
Le but de cet exercice est de déterminer par une étude thermodynamique la constante globale
4
de l'
formation de l'ion complexe tétrammine cuivre II suivant la réaction : Cu2+ + 4 NH3= Cu(NH3)42+.
1. Calculer l'enthalpie standart de la réaction de formation de l'ioncomplexe
rH°.
2. Calculer l'entropie standart de la réaction
rS°.
3. Calculer à 25°C, l'enthalpie libre standart de la réaction
rG°.
4. Commenter le signe de
rH°,
rS°,
rG°.
5. En déduire la constante
4. Commenter sa valeur.
R= 8,314 J K-1 mol-1.
Cu2+ NH3Cu(NH3)42+
rH° kJ mol-1 65,8 -80,3 -349
rS° J K-1mol-1 -97,2 111 274
Corrig
é
BTS Analyses Biologiques 2004 Sciences Physiques
-
http://www.chimix.com
-
CHIMIX
T
é
l
é
charg
é
sur http://www.aidexam.com

corrigé
rH°=
rH°(complexe) - 4
rH°(NH3)-
rH°(Cu2+)
rH°= -349 - 4*(-80,3) -65,8 = -93,3 kJ mol-1
rS°=
rS°(complexe) - 4
rS°(NH3) -
rS°(Cu2+)
rS°= 274-4*111-(-97,2) = -72,8 J K-1mol-1
rG° =
rH° - T
rS°= -93,3 103- 298 *(-72,8) = -71,6 kJ mol-1.
rG° négatif : la réaction évolue spontanément vers la formation du complexe.
rH° négatif : réaction exothermique, chaleur cédée au milieu extérieur.
rG° = - RT ln
4; ln
4=
rG° /( RT)= 71600 / (8,314*298) = 28,9
4=3,56 1012.
Cette valeur est importante : le complexe est particulièrement stable.
maintenance de l'électronique d'un spectrophotomètre
(4,5 points)
L'électronique d'amplification d'un spectrophotomètre est réglée, par construction, pour fonctionner
à
température moyenne de 20°C. En ce mois de juin, une alarme s'est déclenchée sur le spectrophotom
è
température du laboratoire dépasse la valeur seuil. C'est l'étude de l'é
lectronique d'amplification qui est propos
L'amplificateur opérationnel est considéré comme parfait. i+= i-= 0 et ud=0 V.
1. Exprimer I1en fonction de UEet R1.
2. Exprimer I2en fonction de UE, USet R2.
Corrig
é
BTS Analyses Biologiques 2004 Sciences Physiques
-
http://www.chimix.com
-
CHIMIX
T
é
l
é
charg
é
sur http://www.aidexam.com

3. En déduire US= (1+R2/R1)UE.
4. Pour pouvoir réutiliser le spectrophotomètre, il suffit de règler le potentiomètre R2. A la temp
é
moyenne de 20 °C, le rapport US/UEvaut 10 ; sachant que R1= 2200
calculer la valeur de R
5. A la tempé
rature du laboratoire au mois de juin, il faut, selon le constructeur du spectrophotom
rapport US/UEà la valeur 9. Calculer la valeur à laquelle il faut régler R2.
corrigé
UE= - R1I1; I1= -UE/ R1
US+R2I2= UE; I2= (UE- US) / R2
or I1=I2car i+= 0
-UE/ R1=(UE- US) / R2; -UER2= (UE- US) R1
USR1= UE(R1+R2)
US= (1+R2/R1)UE.
à 20°C : US/UE= 10 = 1+R2/R1; 9 = R2/R1; R2= 9 R1= 19,8 k
.
à une température plus élevée : US/UE= 9 = 1+R2/R1; 8 = R2/R1; R2= 8 R1= 17,6 k
sédimentation (4 points)
On se propose d'étudier la sédimentation de la nuclé
ohistone en solution aqueuse, sous l'effet de la pesanteur.
1. Coefficient de frottement d'une particule supposée sphérique :
- La molécule de nucléohistone a une masse m= 3,5 10-21 kg. En supposant la molécule sphé
rique,
déterminer son rayon. Masse volumique de cette molécule
= 1520 kg m-3.
- En supposant toujours la molécule sphérique et à l'aide de la loi de Stockes dé
terminer la valeur du
coefficient de proportionnalité k = 6
R de la force de frottement à la vitesse. (viscosité
= 1,005 10
s)
- Ce coefficient vaut en réalité 4,35 10-10u SI ; la molécule est-elle sphé
rique ? Sinon proposer une forme
pour la molécule.
2. Sédimentation de la particule réelle :
- Faire le schéma de toutes les forces qui s'exercent sur cete molécule.
- Le mouvement de la molécule devient rapidement rectiligne uniforme. A l'aide du bilan préc
é
que la vitesse de sédimentation peut s'exprimer par la relation v = mg/k(1-
'
)où
et
' dé
signent
respectivement la masse volumique de la nuclé
ohistone et de l'eau. Calculer cette vitesse pour la mol
réelle.
- Quelle serait la durée nécessaire pour qu'elle sédimente sur 1 cm ?
- Quelle technique pourrait-on utiliser afin de réduire notablement cette durée ?
Corrig
é
BTS Analyses Biologiques 2004 Sciences Physiques
-
http://www.chimix.com
-
CHIMIX
T
é
l
é
charg
é
sur http://www.aidexam.com

corrigé
volume (m3) = masse (kg) / masse volumique (kg m-3) = 3,5 10-21 / 1520 = 2,3 10-24 m
3
volume d'une sphère V= 4/3
R3soit R3= 3V(4
)
R3= 2,3 10-24 * 3 / (4*3,14)= 5,5 10-25 ; R= 8,19 10-9 m.
k = 6
R = 6*3,14*1,005 10-3 * 8,19 10-9 = 1,55 10-10
valeur différente, trois fois plus faible, que la valeur réelle : la molécule n'est pas sphé
rique mais a une forme
assez éloignée de la sphère ( éllipse assez allongée ou cylindre).
La molécule est soumise à son poids, à la poussée d'Archimède et à
une force de frottement fluide.
lors d'un mouvement rectiligne uniforme : V
g = k vlimite + V
'g
vlimite = Vg/k (
-
') avec m = V
ou V = m/
vlimite = mg/k( 1-
'/
)
vlimite = 3,5 10-21 *9,81/ 4,35 10-10(1-1000/1520)= 2,7 10-11 m/s.
Durée nécessaire pour qu'elle sédimente sur 0,01 m : 0,01 / 2,7 10-11 = 3,7 108s.
technique pour réduire notablement cette durée : ultracentrifugation
Corrig
é
BTS Analyses Biologiques 2004 Sciences Physiques
-
http://www.chimix.com
-
CHIMIX
T
é
l
é
charg
é
sur http://www.aidexam.com
1
/
5
100%