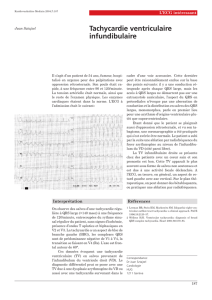
Stratification du risque Stratification du risque

HOLTER
AECG
(Ambulatory Electrocardiography)
HOLTER
AECG
(Ambulatory Electrocardiography)
Dr J. Sztajzel Colloque des internes du 01.12.2008

Références bibliographiques
Références bibliographiques
•ACC/AHA Guidelines for Ambulatory Electrocardiography
(AECG). Crawford et al. J Amer Coll Cardiol 1999; 34: 912-
948.
•ACC/AHA Clinical Competence on Electrocardiography
and Ambulatory Electrocardiography. Kadish et al.
Circulation 2001; 104: 3169-3178.

Indications
Indications
•1) Détermination de la relation entre symptômes et
troubles du rythme
•2) Monitorage de l’efficacité d’un traitement
médicamenteux ou non médicamenteux
•3) Evaluation de la fonction pacemaker et/ou défibrillateur
•4) Identification de patients, avec et sans symptômes, à
risque de présenter une arythmie (après infarctus du
myocarde, insuffisance cardiaque)
•5) Détection d’ischémie myocardique

Indications
Indications
–Quatre situations:
•1) symptômes-arythmie sur Holter
•2) symptômes-rien sur Holter
•3) pas de symptômes-arythmie sur Holter
•4) pas de symptômes-rien sur Holter

R-test (event loop recorders)
R-test (event loop recorders)
•Utilisation pour augmenter le temps d’enregistrement et
détecter mieux certaines arythmies
•R-test
–avec mémoire en boucle limitéeà20 minutes (R-Test Novacor)
–enregistrement continu de 7 jours (Lifecard Delmar Reynolds)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
1
/
45
100%