2de_Univers : Pourquoi Mars est

2de_Univers : Pourquoi Mars est-elle rouge ? M.HENRY
________________________________________________________________________________
I. Problématique
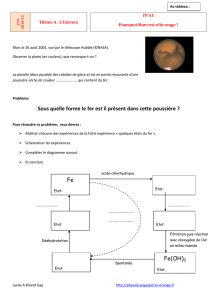
Mars le 26 août 2003, vue par le télescope Hubble (©NASA).
La planète Mars possède des calottes de glace et est en partie recouverte
d’une poussière sèche de couleur rouge qui contient du fer.
Sous quelle forme le fer est il présent dans cette poussière?
Comment s’est elle formée ?
Source : http://pedagogie.ac-toulouse.fr/sc_phy/site_php/spip.php?article508
________________________________________________________________________________
II. Données sur l'élément Fer :
Noms Fer Oxyde de fer
déshydraté
hydroxyde
de fer III
ion Fer II Oxyde de Fer
hydraté
hydroxyde
de fer II
Formules Fe Fe2O3Fe (OH) 3Fe2+ Fe2O3, H2O Fe (OH) 2
états Solide Métal Solide Poudre
Précipité
Ions en
solution
Solide Aspect
gélatineux
Précipité
couleurs Gris Rouge
marron
Rouille
Orangée
Verdâtre
( si concentré )
Marron
foncé
Vert
________________________________________________________________________________
III. Consignes / Expérimentation
•Réalisez chacune des expériences de la Fiche expérience « quelques états du fer ».
•Schématisez les expériences et décrivez vos observations sur votre compte rendu.
________________________________________________________________________________
Fiche expérience « quelques états du fer »
Expérience 1 : action de l'acide chlorhydrique
Dans un tube à essai, verser une spatule de poudre de fer puis, avec précaution, environ
5 mL d’acide chlorhydrique . Laisser la réaction se poursuivre durant 30 minutes
minimum Noter vos observations pendant que l’expérience se déroule.
Expérience 2 : action de la soude
Transvaser le liquide du tube à essai précédent dans un tube propre.
ajouter délicatement environ 3 mL d’une solution d’hydroxyde de sodium à 2,00 mol.L-1.
Noter vos observations.
Sous quelle forme se trouve maintenant l’élément fer ?
Expérience 3 : action de l’air
Filtrer le contenu du tube à essai et observer le contenu du papier filtre à la fin de la filtration.
Attendre quelques minutes. Noter l’aspect et la couleur de ce qu’il contient.
Sous quelle forme se trouve maintenant l’élément fer ?
Expérience 4 : action de l'étuve
Lorsque la filtration est terminée, poser votre papier filtre sur un autre papier filtre pour absorber le

liquide et étaler soigneusement le composé obtenu. Placer le précipité dans une étuve à 80°C.
Quelle est le rôle de l’étuve ?
Décrire le contenu du papier filtre
Sous quelle forme se trouve maintenant l’élément fer ?
Expérience 5 : aluminothermie
Un mélange de poudre d’oxyde de fer (III), tout à fait semblable à celle obtenue dans l’étuve et de
poudre d’aluminium, est placé sur une brique réfractaire.
La réaction entre ces deux composés est amorcée par la combustion d’un ruban de magnésium.
Il se forme un métal incandescent qui devient gris en refroidissant et qui est attiré par un aimant.
Vidéo : Lien http://youtu.be/kcb_5smmVoY
________________________________________________________________________________
IV- CONCLUSION:
1. En vous aidant des informations ci-dessus et des observations expérimentales précédentes
élaborer un cycle de l’élément fer en partant du métal fer, Fe . Indiquez à chaque étape, la formule
chimique du composé obtenu, son état (en solution, précipité, métal, poudre …) et sa couleur.
2. Lavoisier disait : « Rien ne se perd, rien ne se crée, tout se transforme ».
Que voulait il signifier par sa phrase ?
3. Quel est l’élément commun à tous les corps formés au cours des différentes étapes ?
4. A cause de quel composé Mars nous apparaît-elle rouge ?
V. Prolongement
5. Le composé trouvé est l’un des constituants de la rouille. En présence de quels réactifs la rouille
se forme-t-elle ?
Qu’en déduisez-vous sur la composition de Mars dans le passé ?
6. D’après vous, comment l’élément fer présent dans ce composé a-t-il pu arriver sur Mars ?
Acide
chlorhydrique
soude
Fe
Métal Fer
gris
air
étuve
aluminothermie
1
/
2
100%