Pourquoi Mars est rouge

582692157 C Bourvic
ACTIVITE N°3 Noms :
Pourquoi Mars est Rouge. Groupe N° :
Le télescope Hubble (©NASA) Le 26 août 2003 nous a fourni une vue de
Mars. Les observations montre que la planète Mars possède des calottes de
glace et qu’elle est en partie recouverte d’une poussière sèche de couleur
rouge qui contient du fer.
A partir d’expériences simples, nous allons chercher à répondre à la
question suivante :
Sous quelle forme le fer est il présent dans cette poussière?
1) Protocoles expérimentales.
Avant toutes expériences, il est important de lire la fiche de sécurité des réactifs utilisés.
Quelles sont les risques et les précautions que vous devez respecter en utilisant l'acide
chlorhydrique:
L’acide chlorhydrique est Corrosif et dangereux pour la santé. Peut provoquer de graves brûlures,
être irritant pour les yeux, les voies respiratoires, la peau. Est nocif par contact avec la peau,
ingestion et inhalation.
Mettre des gants, porter des lunettes, ne pas inhaler et ingérer.
Quelles sont les risques et les précautions que vous devez respecter en utilisant la soude:
La soude est Corrosive. Peut provoquer de graves brûlures, être irritant pour les yeux, les voies
respiratoires, la peau.
Mettre des gants, porter des lunettes.
Réalisez et schématisez chacune des expériences ci dessous :
Expérience 1 : action de l’acide chlorhydrique sur le fer
Dans un tube à essai, versez une spatule de limaille de fer puis environ 2mL d’acide chlorhydrique (de
concentration 1 mol.L-1).
Il se forme des ions fer (II) Fe2+.
FICHE DE SECURITE
Acide chlorhydrique
FICHE DE SECURITE
Soude (hydroxyde de sodium)

582692157 C Bourvic
Cette réaction est étudiée en troisième, il apparait un dégagement gazeux et une légère
couleur verdâtre, correspondant aux ions Fe2+t.
Expérience 2 : action de la soude sur les ions fer (II)
Transvaser le liquide du tube à essai précédent dans un tube propre.
Verser environ 1mL de soude (de concentration 2 mol.L-1 ) dans le liquide.
Il se forme de l’hydroxyde de fer (II) Fe(OH)2.
On obtient une suspension solide verdâtre ressemblant à des « flocs » que
l’on appelle un précipité..
Expérience 3 : action de l’air sur l’hydroxyde de fer (II)
Après filtration, étaler le précipité obtenu précédemment sur une coupelle.
Attendre quelques minutes. ( schématiser les deux partie de votre
expérience)
1ère partie la filtration:
2ème partie oxydation spontanée:
Il se forme dans un premier temps de l’hydroxyde de fer (III) Fe(OH)3 puis celui-ci se transforme
spontanément en oxyde de fer (III) hydraté Fe2O3,H2O. Ces deux composés ont la même couleur.
En quelques minutes, on observe un passage du vert à l’orangé.
erlenmeyer
Entonnoir et
papier filtre
filtrat
Mélange à filtrer

582692157 C Bourvic
Expérience 4 : déshydratation de l’oxyde de fer (III) hydraté
Placer la coupelle d’oxyde de fer (III) hydraté dans une étuve ou bien placer l’oxyde de fer (III) hydraté
dans un tube à essai et chauffer modérément à l’aide d’un bec électrique.
L’oxyde de fer (III) se déshydrate.
L’eau présent sur le filtre est éliminé par déshydratation. Ci-dessous deux résultats obtenus avec une
quantité de précipité plus ou moins importante
.
Expérience 5 : action de l’aluminium sur l’oxyde de fer (III) (prof)
Un mélange de poudre d’oxyde de fer et de poudre d’aluminium est placé sur une brique réfractaire ou
dans un creuset. La réaction est amorcée par la combustion d’un ruban de magnésium. Il se forme un
métal incandescent qui devient gris en refroidissant et qui est attiré par un aimant. C’est donc du
fer.
On constate une expérience vive qui fait apparaitre au fond du creuset de petites billes de fer. Celles-ci
sont attirés pas un aimant.
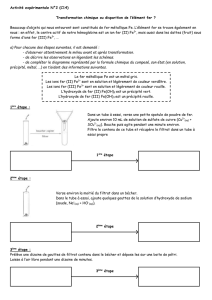
2) Bilan des expériences.
Complétez le diagramme sur cette fiche par la formule chimique du composé obtenu, son état
(en solution, précipité, métal, poudre …) et sa couleur.

582692157 C Bourvic
Conclure : Quel est la formule chimique du composé de fer qui donne sa couleur à Mars?
Les observations montrent que la planète Mars est en partie recouverte d’une poussière sèche de
couleur rouge qui contient du fer.
L’expérience 4 nous montre que l’oxyde de fer (III) déshydraté est plutôt rouge. C’est donc sous
cette forme que le fer est présent sur Mars
D’autre part en regardant le diagramme on constate que l’élément fer est conservé tout au long des
réactions chimiques. Il passe de la forme atome à la forme d’ion pour revenir à l’atome.
1
/
4
100%