Les prions - anne decoster

- JC Lemahieu et A. Decoster, ATNC, FLM, p. 1 -
LES "AGENTS" TRANSMISSIBLES NON CONVENTIONNELS (ATNC)
Cette dénomination s'applique à deux types d’agents transmissibles qui ne sont ni des bactéries, ni des virus :
- les viroïdes = information génétique sans protéine
- les prions = protéine sans information génétique ?
I - LES VIROÏDES
À ce jour, les viroïdes n'ont été observés que dans le règne végétal.
Un viroïde est un ARN monocaténaire circularisé de taille infime (200 à 400 nucléotides). L'appariement d'une
grande partie des nucléotides donne aux viroïdes l'apparence d'un ARN bicaténaire, compacté en bâtonnet.
L'ARN ne code aucune protéine. C'est dans le noyau de la cellule infectée que se situe la réplication des
viroïdes, effectuée par l'ARN polymérase cellulaire.
En perturbant la production des ARN-messagers et le fonctionnement des ribosomes, les viroïdes entraînent
d'importants désordres dans le métabolisme cellulaire.
Le premier viroïde, isolé en 1967, cause la maladie des tubercules fusiformes de la pomme de terre. Les
tubercules sont allongés, noueux et leur surface est sillonnée de profondes crevasses, ce qui les rend
impropres à la consommation.
De nombreuses espèces végétales sont infectées par des viroïdes; les dégâts qu'ils causent sont surtout
considérables dans les pays chauds.
les viroïdes sont essentiellement transmis
p
ar contact, en
p
articulier
p
ar les instruments de culture.
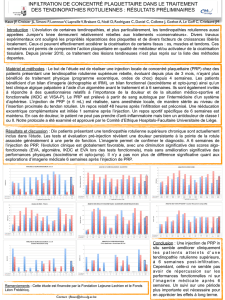
structure d'un viroïde
le rectangle de la région centrale correspond à une
séquence retrouvée chez tous les viroïdes
Le virus de l'hépatite delta (voir aussi le cours sur les virus des hépatites)
Le virus de l'hépatite delta (VHD), spécifique de l'homme, est le seul membre du genre Deltavirus.
Le VHD est un virus défectif, car il ne peut se multiplier qu'en présence du virus de l'hépatite B dont il "emprunte"
l'enveloppe.
Le génome du VHD est apparenté à celui des viroïdes :
c'est un ARN circulaire − (taille = 1,7 kb) compacté en bâtonnet, association d'un segment ressemblant à
celui des viroïdes avec un unique gène codant une protéine1 : l'antigène delta. (Ag δ).
L'antigène δ dirige la réplication, la morphogenèse et la libération des nouveaux virus.
L'ARN-polymérase cellulaire synthétise l'ARN-m de l'Ag δ. et réplique le génome. Le complexe ARN − / Ag δ quitte
le noyau et acquiert l'enveloppe du VHB au niveau du réticulum endoplasmique.
1 Le VHD est le seul virus dont le génome est un ARN circulaire.

- JC Lemahieu et A. Decoster, ATNC, FLM, p. 2 -
L'infection par le VHD dépend de l'infection par le VHB : cette double infection peut résulter soit d'une co-
infection (les deux virus pénètrent en même temps) ou de la surinfection d'un porteur chronique du VHB par
le VHD. Elle touche surtout les toxicomanes.
→ le VHD potentialise les effets pathogènes du VHB.
La recherche de l'antigène δ et des anticorps anti-δ (IgM et IgG) sont les examens les plus utiles pour
reconnaître une infection.
Le VHD étant recouvert par l'enveloppe du VHB, la vaccination contre l'hépatite B protège également de
l'hépatite D.
II – LES PRIONS, AGENTS DES ESST
Les prions sont les agents transmissibles non conventionnels responsables des encéphalopathies
spongiformes subaiguës transmissibles (ESST)
A – DEFINITION DES ESST
ESST - l'abréviation résume les points communs de ces maladies :
Encéphalopathie la cible principale est le cerveau
Spongiforme le cerveau s'altère et prend l'aspect d'une éponge
Subaiguë l'évolution de la maladie est intermédiaire entre l'état
aigu et l'état chronique
Transmissible d'un individu infecté à un individu sain
Les ESST sont des maladies neurodégénératives caractérisées par une longue période d'incubation
asymptomatique (parfois de plus de 40 ans chez l'homme) suivie par une maladie neurologique d'évolution
subaiguë, létale chez 100 % des sujets en quelques semaines à quelques mois.
l'incubation est généralement égale à la moitié de l'espérance de vie de l'espèce considérée.
Une ESST est caractérisée par :
1. une déperdition neuronale liée à la mort des neurones.
2. une spongiose1 : par suite de l'apparition de vacuoles dans le cytoplasme des neurones et les prolongements
dendritiques.
la vacuolisation des neurones infectés (absence de coloration) donne au tissu cérébral un aspect d'éponge
3. une gliose : prolifération d'autres cellules (hyperastrocytose).
4. la présence, inconstante, de « plaques » de formes variées.
De façon surprenante, on n'observe pas :
1. de production d'interféron
2. ni de réaction inflammatoire d'où le terme d'encéphalopathie et non d'encéphalite (comme l'encéphalite herpétique)
3. ni de réaction immunitaire (l'absence d'anticorps spécifiques de l'agent infectieux empêche le diagnostic sérologique).
il ne doit donc pas s'agir de virus
L'agent infectieux se "multiplie" pourtant d'abord dans le système immunitaire puis dans le système nerveux central, très
longtemps avant l'apparition des signes cliniques.
Toutes les ESST sont transmissibles : dans la même espèce et chez certains animaux de laboratoire, en
particulier la souris.
1 voir le petit lexique neurologique en fin du document

- JC Lemahieu et A. Decoster, ATNC, FLM, p. 3 -
B - CLASSIFICATION DES ESST
− les ESST animales
• la tremblante du mouton ou scrapie 1730
• l'encéphalopathie transmissible du vison 1947
• l'encéphalopathie spongiforme bovine (ESB) 1986
c'est la maladie des « vaches folles ».
− les ESST humaines
• la maladie de Creutzfeldt-Jakob (MCJ) 1920
• la maladie de Gertsmann-Sträussler-Sheinker (GSS) 1936
• le kuru 1957
• l'insomnie fatale familiale (IFF) 1986
• la nouvelle variante de MCJ (nv-MCJ) 1994
C - HISTOIRE DES ENCÉPHALOPATHIES SPONGIFORMES TRANSMISSIBLES
1°- La tremblante du mouton - XVIIème siècle
Cette maladie est bien connue des vétérinaires puisqu'elle sévit en Europe − au moins depuis 1730 − à l'état endémique.
Elle affecte maintenant les cinq continents.
En 1990, l'incidence de la tremblante était estimée à 1 mouton sur 100 en Angleterre où l'on compte environ 40 millions de
moutons.
endémique (en = sur, demos = peuple) : qui sévit en permanence.
En Angleterre, on l'appelle la scrapie (to scrape = se gratter) : les signes cliniques de la maladie étant le tremblement et le
prurit intense.
Dès 1936, deux vétérinaires français de l'école de Toulouse ont montré le caractère infectieux de la maladie. Ils
inoculent, par voie intra-oculaire, un broyat de cerveau d'un mouton malade à deux moutons sains. Ces derniers
développent la maladie en tous points identique à la tremblante, après 20 mois d'incubation.
L'agent infectieux est présent dans le cerveau, mais aussi dans la rate et dans le placenta.
→ Comment se transmet la tremblante ?
Le placenta expulsé par les brebis est mangé par les autres moutons. L'herbage et le sol contaminé conservent
longtemps une infectiosité significative.
En 1938, les mêmes auteurs démontrent expérimentalement la transmissibilité de la
tremblante du mouton à la chèvre.
Il n'existe pas d'argument épidémiologique pour penser que l'agent de la tremblante du mouton soit pathogène
pour l'homme.
2°- L'encéphalopathie spongiforme du vison - USA, 1947
Elle est due à l'alimentation de ces animaux en élevage par des carcasses de ruminants atteints d'ESST
(tremblante ou encéphalite spongiforme bovine).
Certains cas suggèrent en effet la transmission d'une ESB qui n'aurait pas été diagnostiquée chez les bovins.
La maladie du vison se maintient dans les élevages du fait du cannibalisme : les visons consommant leurs
congénères morts.

- JC Lemahieu et A. Decoster, ATNC, FLM, p. 4 -
3°- Le kuru - 1957
Un médecin australien de la Santé publique, nommé en Nouvelle-Guinée, Vincent Zigas, chargé de la santé des tribus du
nord-est de l'île (qui vivent encore à l'âge de pierre), constate une maladie curieuse : elle atteint spécifiquement une tribu,
les Fores, qui compte environ 15 000 membres, et qui appelle cette maladie le « kuru », ce qui signifie « trembler de
peur ».
La maladie atteint surtout les femmes et les enfants et se manifeste par des tremblements de la tête, du
tronc et des membres, des signes d’ataxie cérébelleuse (trouble de la coordination du mouvement volontaire),
d’où une démarche chancelante. Les symptômes s’amplifient progressivement. Des signes de démence
apparaissent. Le malade devient incapable de se mouvoir. En 3 à 6 mois, la mort est constante, liée aux
complications infectieuses du décubitus (le sujet devenant grabataire et incontinent).
L'analyse de cerveaux révèle une spongiose constituée de multiples vacuoles et une déperdition neuronale importante.
Pour l'anatomopathologiste, la seule autre maladie conduisant à des anomalies de ce type lui paraît être la maladie de
Creutzfeldt-Jakob. Il note la présence fréquente de plaques amyloïdes dans le cortex.
4°- Le kuru et la tremblante du mouton - 1959
À la fin de l'année 1957, Zigas et Gajdusek publient un article résumant ce qu'ils ont appris de cette maladie
obscure...
L'origine du kuru : (selon Gajdusek)
cette maladie étant inconnue avant 1930, un cas de MCJ sporadique est apparu dans la tribu
des Fore. La pratique du cannibalisme rituel des morts en a favorisé la dissémination de
famille en famille, créant ainsi une nouvelle maladie.
En 1959, un vétérinaire américain, William Hadlow, lit cet article et écrit au Lancet, pour attirer l’attention sur la
parenté clinique et neuropathologique entre le kuru et la tremblante du mouton.
Hadlow termine sa lettre en suggérant d’inoculer du cerveau de sujets décédés du kuru à des singes et d’attendre
longtemps pour voir si cette maladie est transmissible comme la tremblante.
Ce qu'entreprend Gajdusek en 1963. Il démontre que le kuru est transmissible au chimpanzé : on retrouve
chez l'animal les lésions du kuru 20 mois après l’inoculation intracérébrale.
Le kuru est donc une maladie infectieuse, liée au cannibalisme familial pratiqué par les Fore : le corps du défunt sert de
nourriture rituelle aux membres de la famille qui recueillent ainsi les vertus de leur parent.
Pour préparer le repas, les femmes doivent dépecer le défunt. Tandis que les hommes et les adolescents mangent les
muscles, symbole de force, les femmes et les enfants mangent les « abats » dont le cerveau, cuit à la vapeur...
Les femmes et les enfants se contaminent surtout par la voie cutanéo-muqueuse lors du dépeçage du défunt : muqueuses
nasales et oculaires ou via les abrasions de la peau et aussi, peut-être, par la voie orale.
Depuis l'interdiction du cannibalisme en 1957, la maladie a presque disparu.
Les très rares cas actuels font suite à des contaminations survenues il y a plus de 40 ans.
Gajdusek a obtenu le Prix Nobel de Médecine en 1976.
L'incubation de la maladie est variable : de 4 à 40 ans.
L’agent infectieux ne peut être isolé...
5°- La maladie de Creutzfeldt-Jakob (MCJ)
La maladie porte le nom des deux neurologues allemands qui l'on décrite en 1920.
La maladie de Creutzfeldt-Jakob est la plus fréquente des encéphalopathies spongiformes transmissibles
humaines.
En 1968, Gajdusek réussit la transmission de la MCJ au chimpanzé : un an après l’inoculation intracérébrale,
on retrouve chez l'animal les lésions caractéristiques.
L’agent infectieux ne peut être isolé...

- JC Lemahieu et A. Decoster, ATNC, FLM, p. 5 -
On décrit trois formes de MCJ :
1. la forme sporadique : 90 % des cas
De cause inconnue, c'est la forme la plus fréquente.
La répartition de cette forme est mondiale. L'incidence est de :
1 cas par 1.000.000 d'habitants et par an (60 cas annuels en France).
Elle touche également les deux sexes.
L'âge du début de la maladie se situe habituellement entre 55 et 75 ans (extrêmes : 16-83).
La durée totale de la maladie ne dépasse pas un an dans 90 % des cas (extrêmes : 1 à 30 mois).
2. la forme familiale : 5 à 6% des cas
D’origine génétique, ces formes familiales se transmettent d'une façon autosomale dominante.
L'âge du début de la maladie se situe entre 34 et 54 ans.
Ni la forme sporadique, ni la forme familiale ne paraissent liées à une quelconque influence
extérieure.
3. la forme infectieuse : 4 à 5% des cas
Elle est d'origine iatrogénique (provoquée par un acte médical)
La période de latence varie de 18 mois à 28 ans.
Sur environ 100 cas décrits, 90 % sont dus à un traitement par l'hormone de croissance extraite
d'hypophyses ou à une greffe de dure-mère ; les 10 % restants sont attribués à des interventions
diverses : greffes de cornée, interventions neurochirurgicales ou explorations avec du matériel
contaminé.
6°- La maladie de Gertsmann-Straüssler- Sheinker (GSS)
Décrite en 1936, c'est une ESST génétiquement transmise, dont moins de 100 cas ont été publiés, appartenant à une
vingtaine de familles.
L'âge moyen de début de la maladie est de 48 ans (extrêmes : 20 et 66 ans).
La durée totale de la maladie est en moyenne de 5 ans (extrêmes : 1 à 11 ans).
7°- L'insomnie fatale familiale (IFF)
Décrite en 1986, c'est une ESST génétiquement transmise, dont moins de 100 cas ont été publiés, appartenant à six
familles.
L'âge moyen de début de la maladie est de 49 ans (extrêmes : 25 et 62 ans).
La durée totale de la maladie est en moyenne d'un an (extrêmes : 7 à 32 mois).
Les trois formes de MCJ, GSS et IFF peuvent être transmises horizontalement.
La forme familiale de MCJ, GSS et IFF sont des maladies génétiques causées par une mutation dominante.
Ces maladies sont aussi des maladies infectieuses : l'inoculation d'un broyat de cerveau à un animal sensible
entraîne une encéphalopathie spongiforme.
8° - La tremblante et l’encéphalopathie spongiforme bovine (ESB)
Angleterre, novembre 1986...
Une nouvelle maladie, baptisée rapidement par les médias "maladie des vaches folles", apparaît
soudainement dans les élevages de vaches laitières (en moyenne 1 élevage sur 2). Elle frappe les vaches
âgées de plus de 5 ans. La mort survient 1 à 6 mois après le début des premiers symptômes, assez proches
de ceux de la tremblante du mouton.
En 1988, un vétérinaire anglais découvre l'origine de cette épidémie soudaine : les farines de viande et d'os –
les FVO, ajoutées à l'alimentation (à raison d'environ 8 %) pour accroître le rendement en lait.
Leur préparation a été modifiée en 1981-1982 :
• le recyclage industriel des carcasses d’animaux abattus par les fermiers ou refusées par les services vétérinaires des
abattoirs, fournit des protéines et des graisses (le suif).
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
1
/
11
100%