Les lésions blanches de la muqueuse buccale et autres lésions à

conférence en direct
10 JDN 2015 · 6 | 7 | 8 mai
n
Introduction
Le cancer est la première cause de mor-
talité en France (source INCA). En 2008, le
taux d’incidence annuel mondial des can-
cers de la cavité buccale et du pharynx
étaient de 484083[1–4]. La France occupe
l’une des premières places en Europe avec
une d’incidence en 2013 estimée à 11 240
nouveaux cas, et 3 758 décès[5, 6]. En France,
l’incidence des cancers de la cavité buccale
(KCB) diminue chez les hommes du fait de
la diminution de la consommation d’alcool
et de tabac. Chez les femmes, le nombre de
nouveaux cas augmente à cause de l’aug-
mentation du tabagisme[7]. Les facteurs de
risque connus sont la consommation ex-
cessive de tabac et d’alcool, ainsi que l’ex-
position chronique au soleil pour les can-
cers de la lèvre. L’alimentation riche en vi-
tamines et oligoéléments antioxydants a
un effet protecteur sur le développement
des KCB[8]. La survenue des KCB est égale-
ment favorisée par l’usage de la noix d’arec
dans les pays ou la chique de Betel est
consommée. Le papillomavirus (HPV)
transmit sexuellement est un facteur de
risque de développement des cancers de
l’oropharynx. La mauvaise hygiène bucco
dentaire et le traumatisme chronique ne
peuvent pas être considérés comme des
facteurs de risque du KCB car il n’existe pas
de preuve épidémiologique. Le taux de sur-
vie à 5 ans des KCB est d’environ 80 % au
stade I et de 20 % aux stades III/IV. La moi-
tié des patients consultent à un stade
avancé ce qui grève le pronostic[4]. Le dia-
gnostic est souvent tardif du fait du carac-
tère non spécifique des symptômes et de
leur méconnaissance par la population gé-
nérale. L’idéal serait de diagnostiquer le
cancer à un stade précoce avant qu’il ne de-
vienne invasif et risque de donner des mé-
tastases. En ce sens, l’odontologiste qui est
le premier maillon de la chaine diagnos-
tique a un rôle important à jouer, notam-
ment dans le diagnostic et la prise en
charge des lésions à potentiel malin. Les
quatre LPM les plus fréquentes en France
seront traitées dans cet article : les leuco-
plasies, l’érythroplasie, le lichen plan et la
chéilite actinique.
Les lésions à potentiel malin
Les lésions à potentiel malin (LPM) sont
des lésions qui peuvent se transformer en
cancer mais qui ne sont pas malignes au
moment de leur diagnostic. Une LPM est
une modification morphologique d’un
tissu présentant un risque accru de déve-
loppement d’un cancer[9]. Le suivi à long
terme des LPM est important car il permet
de diagnostiquer, en cas de transformation
maligne, le cancer en état initial et ainsi de
diminuer la morbidité et le taux de morta-
lité [1,4]. Les termes de lésion pré cancéreuse
et d’état précancéreux anciennement pré-
conisés par l’OMS en 1978 sont aujourd’hui
regroupés sous le terme de lésion à poten-
tiel malin[10–11]. Les LPM correspondent à
différentes affections (Tableau I).
La conduite à tenir devant une lésion à
potentiel malin est de réaliser une biopsie
pour préciser le diagnostic et rechercher
un trouble de la maturation et de la prolifé-
ration cellulaire appelé dysplasie épithé-
liale. La dysplasie est légère lorsque les al-
térations architecturales sont limitées au
tiers basal de l’épithélium, accompagnées
d’atypies cellulaires discrètes avec des mi-
toses normales. Elle est modérée lorsque
les altérations atteignent le tiers moyen de
l’épithélium, avec des atypies cellulaires
modérées et les mitoses normales ou anor-
males. La dysplasie est sévère lorsque les
altérations architecturales et cytologiques
dépassent les deux tiers de l’épithélium ou
lorsque les altérations cellulaires sont
abondantes. Le terme carcinome « in situ»
est réservé aux troubles touchant toute l’é-
paisseur épithéliale, où la transformation
maligne a eu lieu mais sans l’invasion des
tissus adjacents [3, 12]. Le potentiel malin, est
directement lié à la sévérité de la dyspla-
sie [13]. Toutes les dysplasies épithéliales
n’évoluent pas en carcinome et peuvent
même régresser[13].
Leucoplasies
La Leucoplasie est un terme clinique
qui n’a aucune spécificité histologique
(Fig. 1). C’est une kératose à risque discuta-
ble de cancérisation après exclusion de
toutes les autres lésions blanches n’ayant
pas un risque accru pour le cancer[10, 11]. La
prévalence de la lésion selon des études ré-
alisées dans plusieurs pays varie entre 1 et
5%[14], 5 % des lésions se transformeront
en cancer dans une période moyenne de
5 ans [15,16].
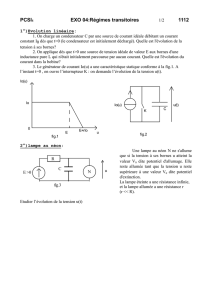
Les principales lésions à exclure sont le
white sponge naevus (Fig. 2), les kératoses
frictionnelles (Fig. 3), le lichen plan (Fig. 4),
les candidoses aigues et chroniques
(Fig. 5), la leucoplasie orale chevelue
(Fig. 6), la stomatite nicotinique (Fig. 7).
Les leucoplasies peuvent être homogè-
nes ou inhomogènes. La forme homogène
est la plus fréquente (Fig. 8). Ces leucopla-
–Date, heure
Vendredi 8 mai |9h00-12h30
–Président de séance
Dr Charles Savoldelli
–Responsable scientifique
Dr Jérôme Surmenian
–Objectifs
· Faire le point sur les connaissances de
la prise en charge odontologique des
patients traités pour un cancer
–Intervenant
Pr Jean-Christophe Fricain
Conférence- DELPHES 3 –
Les lésions blanches de la
muqueuse buccale et autres
lésions à potentiel malin
Les lésions blanches de la muqueuse buccale
et autres lésions à potentiel malin
Pr JC Fricain
5
Tableau I: les lésions à potentiel malin regroupent les
anciennes lésions précancéreuses et étatprécancé-
reux.
5
Fig. 2 : LEUCOPLASIE : diagnostics à exclure. White Sponge Naevus.
5
Fig. 3 : LEUCOPLASIE : diagnostics à exclure. Kératose frictionnelle (traumatique).
5
Fig. 4 : LEUCOPLASIE : diagnostics à exclure. a) Lichen Plan b) Réaction lichéno-
ide
5
Fig. 5 : LEUCOPLASIE : diagnostics à exclure. Pseudomembrane candidosique.
5
Fig. 6 : LEUCOPLASIE : diagnostics à exclure. Leucoplasie orale chevelue.
5
Fig. 7 : LEUCOPLASIE : diagnostics à exclure. Ouranite tabagique.
5
Fig. 8 :
LEUCOPLASIE : formes cliniques. Leucoplasie homogène.
5
Fig. 9 : LEUCOPLASIE : formes cliniques. Leucoplasie inhomogène.
5
Fig. 10: LEUCOPLASIE : formes cliniques. Leucoplasie proliférative verruqueuse =«carcinome verru-
queux ».
5
Fig. 11: LEUCOPLASIE : sevrage tabagique. b) 1 mois de sevrage. Martin JC, 97% rémission leucoplasie due tabac non fumé. (J Am Dent Assoc 1999)
5
Fig. 12 : LEUCOPLASIE : Conduite à tenir pour absence dysplasie/dysplasie
légère à modéré (taille <3cm2) : exérèse lame.
5
Fig. 13: LEUCOPLASIE : Conduite à tenir pour absence dysplasie/dysplasie légère à modéré (taille <3cm2) : exérèse laser diode.
2 3 4a 4b
5 6 7
8 9 10
11a 11b 12 13
5
Fig 1 : LEUCOPLASIE : plaque blanche kératosique
idiopathique ou associé à la consommation de tabac
et/ou noix d’arec. Diagnostic d’exclusion basé sur
l’examen clinique et la biopsie.
1

conférence en direct
11
JDN 2015 ·6|7|8 mai
sies ont un aspect de plaque blanche claire-
ment circonscrite, plane ou légèrement
surélevée, lisse ou uniformément ru-
gueuse, légèrement granulaire et ondulée,
parfois traversée par de fines crevasses ou
fissures sans érythème ou avec un éry-
thème discret et uniforme sans érosions[11].
Les leucoplasies inhomogènes (Fig. 9)
sont mal limitées, d’aspect érythémateux,
érosif, verruqueux ou nodulaire sur toute
leur surface ou par endroits. Leur surface
est irrégulière (aussi en épaisseur) présen-
tant des zones ulcérées ou érythropla-
siques [10]. Les types de leucoplasies inho-
mogènes sont : [11]
Plaque mixte (speckled leucoplakia),
blanche et rouge, mais ayant le blanc
comme couleur principale, a l’aspect d’une
plage érythémateuse mouchetée de kéra-
tose, appelée aussi érythroleucoplasie ;
• Leucoplasie verruqueuse : prolifération
exophytique verruqueuse avec parfois des
fissures dans une zone muqueuse hyperké-
ratosique blanche ;
• Leucoplasie nodulaire : surélevée, ar-
rondie avec des excroissances rougeâtres
ou blanchâtres qui se présentent comme
des grains ou des nodules ;
Les leucoplasies inhomogènes sont fré-
quemment associées aux dysplasies épi-
théliales et au carcinome « in situ» [10, 11, 17].
La leucoplasie verruqueuse proliféra-
tive ou PVL (proliferative verrucous leuco-
plakia) est la prolifération de multiples leu-
coplasies simultanées, homogènes ou in-
homogènes (Fig. 10). C’est une affection
multifocale, couvrant des larges surfa-
ces [10, 17–18].
Le traitement des leucoplasies repose
en première intention sur le sevrage taba-
gique (Fig. 11).
En l’absence de dysplasie ou en pré-
sence de dysplasie légère à modérée, le
traitement des leucoplasies repose sur
l’exérèse à la lame (Fig. 12) ou au laser
diode (Fig. 13) pour les lésions de petite
taille. Pour les lésions de grande taille une
vaporisation au laser CO2est préconisée
(Fig. 14). Pour les lésions de dysplasie sé-
vère l’exérèse à la lame avec des marges est
nécessaire (Fig. 15). Les leucoplasies proli-
fératives verruqueuses peuvent être trai-
tées par chimiothérapie (méthotrexate IV)
pour les formes étendues.
Erythroplasie
L’érythroplasie est la lésion ayant le po-
tentiel de transformation maligne le plus
important [19]. Elle est définie comme une
plage rouge brillant qui ne peut pas être
diagnostiquée comme aucune autre affec-
tion [11]. C’est une macule érythémateuse si-
tuée 0,1 à 0,2mm sous la muqueuse nor-
male (Fig. 16). Elle a un aspect velouté, le
plus souvent uniforme sans trace de kéra-
tinisation, souvent très étendue mais dont
la limite avec les tissus sains est nette[19–20].
Dans plus de 90 % de cas elle correspond
histologiquement à une dysplasie épithé-
liale sévère[19–22]. Elle atteint principale-
ment le palais mou, la muqueuse jugale et
le plancher buccal[21].
Les principaux diagnostics différentiels
devront être fait avec l’érythème friction-
nel, l’érythème des pathologies inflamma-
toires de la muqueuse et les érythèmes ca-
rentiels (Fig. 17). Le traitement repose sur
l’exérèse chirurgicale et l’analyse anato-
mopathologique de la pièce d’exérèse.
Le lichen Plan
Le lichen plan est une maladie inflamma-
toire caractérisée sur le plan clinique par
des papules cutanées et un réseau kérati-
nisé réticulé au niveau de la muqueuse buc-
cale[22]. L’aspect histologique typique est un
infiltrat inflammatoire lympho-plasmocy-
taire sous la membrane basale responsable
de la formation de corps apoptotiques. Cer-
tains médicaments ou des traumatismes lo-
caux peuvent induire des lésions lichénoï-
des proches sur le plan clinique et histolo-
gique du lichen plan (Fig. 19).
On peut classer les différentes formes
cliniques du lichen plan buccal en fonction
des lésions élémentaires. Les lésions mu-
queuses peuvent être isolées ou associées
à des lésions d’autres muqueuses: princi-
palement génitale mais aussi œsophage et
plus rarement conjonctive. Le
lichen plan buccal peut aussi être associé à
des lésions cutanées, des ongles ou du cuir
chevelu. Il existe aussi des formes cli-
niques associées à des maladies générales.
L’association lichen plan buccal hépatite c
a été démontrée dans les pays du pourtour
méditerranéen et au japon mais ne semble
pas évidente en France. Le siège de prédi-
lection du lichen plan buccal est les joues
en raison du phénomène de koebner mais
toutes les régions de la muqueuse buccale
peuvent être atteintes.[22–25]
Le lichen plan se présente sous différen-
tes formes cliniques[22-25] :
– Lichen plan buccal kératosique (Fig. 20) :
La forme la plus typique du lichen plan
est la forme kératosique. En fonction de
l’ancienneté du lichen il aura un aspect
en pointillé, réticulé avec les classiques
stries de Wickman, dendritique puis en
plaque évoquant une leucoplasie. A no-
ter sur la langue un aspect typique en
plaque. Le lichen plan kératosique est ra-
rement algique.
– Lichen plan buccal érythémateux
(Fig. 21):
L’aspect érythémateux du lichen plan
buccal est en général associé aux autres
lésions élémentaires du lichen. Une
forme clinique particulière où domine
l’érythème est la gingivite érosive ou des-
quamative. Cette forme de gingivite est
sans rapport avec une infection bacté-
rienne. Contrairement à cette dernière,
l’inflammation est souvent située à dis-
tance du collet des dents, respecte sou-
vent la papille et à tendance à s’étendre
vers la gencive kératinisée. Le lichen
plan érythémateux est généralement
douloureux.
– Lichen plan buccal érosif (Fig. 22):
Si l’appellation lichen plan buccal érosif
est commune, les véritables formes érosi-
ves sont rares. En effet l’infiltrat inflam-
matoire étant localisé au niveau de la
membrane basale, on observe le plus sou-
vent un décollement à ce niveau ce qui
laisse le conjonctif à nu et se traduit sur
le plan clinique par une ulcération. D’au-
tre part, l’érosion est souvent une lésion
fugace en bouche du fait des traumatis-
mes répétés qui induisent une ulcéra-
tion.
– Lichen plan buccal ulcéré (Fig. 23):
Les formes ulcérées de lichen plan buc-
cal sont douloureuses. Elles peuvent être
uniques ou multiples. Elles sont en géné-
ral associées à des formes kératosiques et
érythémateuses. Des granulomes secon-
daires peuvent se former sur les ulcéra-
tions.
– Lichen plan buccal bulleux :
La forme bulleuse du lichen plan buccal
est rare car les bulles éclatent rapide-
ment pour laisser place à une ulcération.
La forme la plus commune est l’atteinte
gingivale.
– Lichen plan buccal pigmenté (Fig. 24):
Une pigmentation de la muqueuse buc-
cal peut s’observer au cours du lichen
plan. La muqueuse prend une teinte va-
riant du brun clair au noir foncé. Cette
pigmentation est secondaire à une dé-
charge pigmentaire dans le chorion
superficiel sous l’effet de l’infiltrat lym-
phocytaire.
– Lichen plan buccal atrophique (Fig. 25) :
Caractérisé par un amincissement de l’é-
pithélium, la muqueuse apparait comme
5
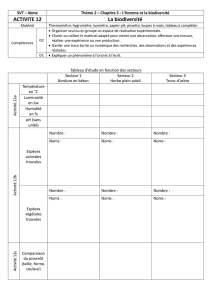
Fig. 14 : LEUCOPLASIE : Conduite à tenir pour absence dysplasie/dysplasie légère à modéré (taille >3cm2) : Vaporisation laser.
5
Fig. 15 : LEUCOPLASIE : Conduite à tenir pour dysplasie sévère: exérèse lame.
5
Fig. 16 : ERYTHROPLASIE :
tâche rouge bien limitée ne pouvant pas être ratachée à une autre pathologie. Diagnostic d’exclusion basé sur l’examen clinique et la biopsie.
5
Fig. 17: ERYTHROPLASIE : diagnostic à exclure. Erythème et érosion d’origine inflamma-
toire, autoimmune ou carentielle.
5
Figure 18 : ERYTHROPLASIE : conduite à tenir. Biopsie et éxérèse chirurgicale.
5
Fig. 19 : Lichen plan et réactions lichénoïdes : a) Lichen plan. b) Réaction lichénoide de contact.
5
Fig. 20 : Lichen plan :
formes cliniques : kératosique.
5
Fig. 21: Lichen plan: formes cliniques: Erythème.
5
Fig. 22 : Lichen plan: formes cliniques : Erosion.
5
Fig. 23 : Lichen plan : formes cliniques: Ulcération.
5
Fig. 24 : Lichen plan : formes cliniques: Pigmen-
tée.
5
Fig. 25: Lichen plan : formes cliniques : Atrophie.
5
Fig. 26: Lichen plan et réactions lichénoïdes : a) Dégénérescence lichen plan. Taux de transformation < 0,5 % (V der Wall, Oral Oncol 2010) Pas de traitement… b) Dégénérescence
réaction lichénoïde.
5
Fig. 27 : Cheilite actinique : lèvre inférieure ++++, homme 45–75 ans.
5
Fig. 28 : Traitement par vaporisation laser CO2d’une lésion de cheilite actinique.
14 15 16
17 18 19a 19b
21
22
26a 26b 27 28
23 24 25
20

lustrée. Parfois des bandes scléreuses
sont palpables notamment au niveau des
joues. Il peut s’y associer des lésions pig-
mentées. Le plus souvent la réaction in-
flammatoire a disparue et il s’agit d’un
état post-lichénien.
Environ 1 à 3 % des lésions de lichen plan
buccal seraient susceptibles de dégénérer
en carcinome épidermoïde (Fig. 26). Des
transformations en carcinome verruqueux
ont aussi été décrites (Fig. 26). Il n’y a pas de
traitement pour prévenir cette transforma-
tion. Une surveillance régulière (une à 2 fois
par an) est requise pour dépister des chan-
gements structuraux de la muqueuse évo-
cateurs d’un carcinome épidermoïde (néo-
formation tissulaire, ulcération persis-
tante, induration, adénopathie).
Le lichen plan buccal est une maladie
chronique, difficile voire impossible à éra-
diquer dans de nombreux cas. Une des ex-
plications pourrait résider dans la pré-
sence de processus irritatifs chroniques
liés à la flore, à la présence des dents, pro-
thèses, matériaux d’obturation dentaires
divers et à la mastication et phonation. A ti-
tre prophylactique, il conviendra donc sys-
tématiquement de minimiser au maxi-
mum les facteurs irritatifs locaux.
Le traitement du lichen plan est essen-
tiellement symptomatique et n’a le plus
souvent qu’un effet suspensif. Il dépend de
la lésion élémentaire et de sa distribution
dans la cavité buccale. En première ligne
thérapeutique on retiendra la corticothé-
rapie locale ou systémique et les inhibi-
teurs de la calcineurine en seconde inten-
tion. Des études anciennes ont montrés l’ef-
ficacité des rétinoïdes topiques sur le li-
chen plan buccal érosif et atrophique. Il
semble que ces traitements sont peu utili-
sés aujourd’hui en raison d’une intolé-
rance locale et dans notre expérience
d’une efficacité modérée. La Puvathérapie
est aujourd’hui contre indiquée en raison
du risque carcinogène.
Chéilites actiniques
Les chéilites actiniques (Fig. 27) sont des
affections touchant les lèvres. La kératose
actinique labiale est caractérisée par des
lésions atrophiques, érosives, blanches ou
des croutes brunâtres du bord vermillon
des lèvres. Elle est causée par une exposi-
tion aux ultra violets. Ces lésions et les can-
cers des lèvres sont plus fréquents chez les
gens qui travaillent à l’extérieur (marins,
agriculteurs, bergers…).
L’épithélium du vermillon peut être
hyperplasique ou atrophique et présente
des troubles de maturation, divers degrés
de kératinisation, des atypies cellulaires et
une importante activité mitotique[14]. Le
tissu conjonctif sous-jacent montre une dé-
générescence basophile du collagène et une
élastose. Le diagnostic clinique de présomp-
tion doit être confirmé par une biopsie[11, 12].
La suppression de l’exposition au soleil,
le conseil du port de vêtements couvrants,
un chapeau et l’utilisation de crèmes de
protection solaire doivent être conseillés.
Le traitement chirurgical par vaporisation
laser CO2(Fig. 28)ou une vermillonectomie
peuvent être nécessaire[26-27].
Conclusion
L’odontologiste est souvent en première
ligne diagnostique des lésions à potentiel
malin et des cancers de la cavité buccale. Il
a une obligation médico-légale de mettre
en œuvre les moyens diagnostics selon les
données acquises de la science. A ce titre
l’examen de la muqueuse buccale fait par-
tie de l’examen de la cavité buccale. L’odon-
tologiste doit repérer les lésions élémentai-
res et mettre en œuvre les moyens d’abou-
tir à un diagnostic et un traitement. Pour les
lésions à potentiel malin et les cancers l’en-
jeu est d’autant plus important que le pro-
nostic de vie du patient est en jeu.7
Bibliographie
[1] Warnakulasuriya S. Global epidemiology of oral and
oropharyngeal cancer. Oral Oncol 2009; 45:309–16.
[2] Ferlay J, Shin H, Bray F, Forman D, Mathers C, Parkin
D. GLOBOCAN 2008 v2.0, Cancer Incidence and Mor-
tality Worldwide: IARC CancerBase No. 10. Lyon, Fr
Int Agency Res Cancer 2010.
[3] Barnes L, Eveson JW, Reichart P, Sidransky D. World
Health Organization Classification of
Tumours. Pathology & Genetics. Head and Neck Tu-
mours. International Agency for Research on Cancer
(IARC). Lyon: 2005.
[4] Van der Waal I. Are we able to reduce the mortality
and morbidity of oral cancer; some considerations.
Med Oral Patol Oral Y Cir Bucal 2013:e33–e37.
[5] OMS. EUCAN – Centre international de Recherche
sur le Cancer n.d. http://eco.iarc.fr/EUCAN (acces-
sed May 16, 2013).
[6] Ferlay J, Steliarova-Foucher E, Lortet-Tieulent J,
Rosso S, Coebergh JWW, Comber H, et al. Cancer in-
cidence and mortality patterns in Europe: Estimates
for 40 countries in 2012. Eur J Cancer
2013;49:1374–403.
[7] Belot A, Velten M, Grosclaude P, Bossard N, Launoy
G, Remontet L, et al. Estimation nationale
de l’incidence et de la mortalité par cancer en France
entre 1980 et 2005. Institut de Veille Sanitaire; 2005.
[8] Maserejian NN, Joshipura KJ, Rosner BA, Giovan-
nucci E, Zavras AI. Prospective study of alcohol
consumption and risk of oral premalignant lesions in
men. Cancer Epidemiol Biomarkers Prev
2006;15:774–81.
[9] World Health Organization Collaborative Reference
Centre for Oral Precancerous Lesions. Application of
the international classification of diseases to Dentis-
try and stomatology. Geneva: WHO Publications
Center; 1978.
[10] Warnakulasuriya S, Johnson NW, van der Waal I. No-
menclature and classification of potentially mal-
ignant disorders of the oral mucosa. J Oral Pathol
Med 2007;36:575–80.
[11] Ben Slama L. [Potentially malignant disorders of the
oral mucosa: terminology and classification]. Rev
Stomatol Chir Maxillofac 2010;111:208–12.
[12] Warnakulasuriya S, Reibel J, Bouquot J, Dabelsteen
E. Oral epithelial dysplasia classification systems:
predictive value, utility, weaknesses and scope for
improvement. J Oral Pathol Med 2008;37:127–33.
[13] Pindborg JJ, Daftary DK, Mehta FS. A follow-up study
of sixty-one oral dysplastic precancerous lesions in
Indian villagers. Oral Surg Oral Med Oral Pathol
1977;43:383–90.
[14] Kleinman D V, Swango PA, Pindborg JJ, Gupta P. Ad-
vances in Dental Research 1993.
[15] Schepman KP, van der Meij EH, Smeele LE, van der
Waal I. Malignant transformation of oral leukopla-
kia: a follow-up study of a hospital-based population
of 166 patients with oral leukoplakia from The Ne-
therlands. Oral Oncol 1998; 34:270–5.
[16] Bouquot JE, Gorlin RJ. Leukoplakia, lichen planus,
and other oral keratoses in 23,616 white Americans
over the age of 35 years. Oral Surg Oral Med Oral Pa-
thol 1986;61:373–81.
[17] Waldron C, Shafer W. Leukoplakia revisited. Cancer
1975;36:1386–92.
[18] Carrard V, Brouns E, van der Waal I. Proliferative ver-
rucous leukoplakia; a critical appraisal of the dia-
gnostic criteria. Med Oral Patol Oral Y Cir Bucal
2013;18:e411–e413.
[19] Reichart P a, Philipsen HP. Oral erythroplakia--a re-
view. Oral Oncol 2005;41:551–61.
[20] Shafer WG, Waldron C a. Erythroplakia of the oral ca-
vity. Cancer 1975;36:1021–8.
[21] Bouquot JE, Weiland LH, Kurland LT. Leukoplakia
and carcinoma in situ synchronously associated
with invasive oral/oropharyngeal carcinoma in Ro-
chester, Minn., 1935-1984. Oral Surg Oral Med Oral
Pathol 1988;65:199–207.
[22] Van der Waal I. Potentially malignant disorders of
the oral and oropharyngeal mucosa; terminology,
classification and present concepts of management.
Oral Oncol 2009;45:317–23.
[23] Epstein JB, Wan LS, Gorsky M, Zhang L. Oral lichen
planus: progress in understanding its malignant po-
tential and the implications for clinical manage-
ment. Oral Surg Oral Med Oral Pathol Oral Radiol
Endod 2003;96:32–7.
[24] Meij EH Van Der, Waal I Van Der. Lack of clinicopa-
thologic correlation in the diagnosis of oral lichen
planus based on the presently available diagnostic
criteria and suggestions for modifications
2003:507–12.
[25] Patil S, Rao RS, Sanketh DS, Warnakulasuriya S. Li-
chenoid dysplasia revisited – evidence from a re-
view of Indian archives. J Oral Pathol Med 2014.
[26] Lodi G, Porter S. Management of potentially mal-
ignant disorders: evidence and critique. J Oral Pathol
Med 2008;37:63–9.
[27] Ishii J, Fujita K, Komori T. Laser surgery as a treat-
ment for oral leukoplakia. Oral Oncol
2003;39:759–69.
JDN 2015 · 6 | 7 | 8 mai
1
/
3
100%