Interférons

Interférons
L’interféron aété découvert en 1957 comme une subs-
tance inhibant la réplication d’un virus en présence d’un
autre virus. Depuis, on connaît deux types d’interféron.
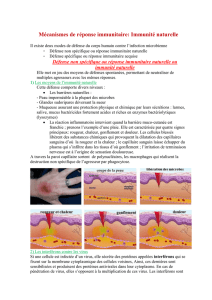
Ces molécules font partie des défenses antivirales non
spécifiques des cellules et des organismes. Produits au
tout début des infections, les interférons sont également
impliqués dans le réseau complexe des cytokines et
donc dans la réponse immunitaire :
•interférons de type I:les gènes des interférons de
classe Isont dépourvus d’introns et sont situés sur le
bras court du chromosome 9:
–les interférons α:18gènes sont connus et
20 espèces moléculaires sont décrites (IFNα1a pour
le produit du gène A1) ;
–l’interféron â:unseul gène connu et une seule pro-
téine de 166 acides aminés ;
–l’interféron Ù:six gènes connus et une espèce
moléculaire connue de 172 acides aminés.
•interféron de type II :ilsecompose uniquement de
l’interféron ã,codé par un gène unique, comprenant
trois introns, localisé sur le chromosome 12 ;l’espèce
moléculaire connue est formée de deux sous-unités
protéiques.
Les interférons αsont produits par les lymphocytes
non-T, non-B, portant des HLA-DR, par les cellules
dendritiques, par les monocytes, par les fibroblastes en
présence de certains virus comme le virus herpès sim-
plex, de certaines substances chimiques, comme des
oligonucléotides àsimple brin, les G-CSF et GM-CSF.
La synthèse des interférons âest induite dans les fibro-
blastes en présence d’ARN bicaténaire viral, celle des
interférons ãest produite par les lymphocytes TCD4
activés par des substances mitogènes ou par des lym-
phocytes TouNKenprésence d’interleukine 2ou12.
L’induction d’interféron après une infection virale va
durer plusieurs jours, puis s’arrêter. Les cellules
connaissent alors une période réfractaire avant d’être de
nouveau inductibles par une nouvelle infection virale.
Les interférons ont une spécificité d’espèce. Les interfé-
rons αet âreconnaissent les mêmes récepteurs spéci-
fiques. Le spectre d’activité antivirale des interférons
s’étend àtous les virus, indépendamment de leur acide
nucléique ARN ou ADN ;cependant, les cycles réplica-
tifs du virus de l’hépatite Coudelavaricelle sont plus
facilement bloqués que ceux d’autres virus.
Les dosages d’interférons αet ãsont praticables sur
sérum et sur liquide céphalo-rachidien par des tech-
niques biologiques, puis plus récemment par des tech-
niques de type Elisa.
Chez le sujet sain, les taux d’interférons αou ãsont
indétectables et sont normalement inférieurs au seuil de
sensibilité de la technique.
Les interférons αsont induits chez l’homme par les
infections virales, alors que les interférons ãpeuvent
être décelés dans des prélèvements pratiqués au cours
de maladies virales, bactériennes ou parasitaires.
Lors d’un syndrome infectieux, la présence de taux
significatifs d’interféron au niveau sérique ou rachidien
doit alerter si l’examen microbiologique est revenu
négatif.
Dosages dans le sérum
Au cours des infections aiguës, les taux sériques d’inter-
féron αaugmentent précocement au cours des 3à
10 premiers jours de l’infection selon les virus, les taux
étant d’autant plus élevés que les échantillons sont pré-
levés rapidement. Selon l’infection virale, les taux
peuvent être plus ou moins élevés :virus de la rougeole,
de l’herpès, arbovirus, rotavirus. L’interféronémie α
peut être absente lors de certaines virémies ou représen-
tée par des sous-types d’interférons αnon dosables par
les dosages actuels :ledosage de l’interféron ãpeut
alors s’avérer utile en deuxième intention car, en parti-
culier pour les virus de l’herpès, de la rougeole et les
entérovirus, l’élévation de l’interféron ãest concomi-
tante de celle des interférons α .
Au cours des infections virales persistantes, l’interféro-
némie n’est pas constante et dépend du virus. Au cours
de l’infection au VIH, les taux élevés d’interféron α
semblent plus corrélés àdes charges virales élevées.
Dosages dans le liquide céphalo-rachidien
Les taux élevés d’interféron retrouvés au niveau du
liquide céphalo-rachidien témoignent d’une production
locale d’interféron, par réplication intrathécale en rela-
tion avec un envahissement viral du système nerveux
central ou des méninges :les valeurs observées sont très
élevées dès le début des signes cliniques et s’annulent en
5à10jours pour les encéphalites et en 3à5jours pour
les méningites.
L’interféron αest synthétisé par le système nerveux
dans 95 %des cas d’encéphalite herpétique :chez
l’adulte, la production d’interféron αest uniquement
intrathécale et chez le jeune enfant, les taux sériques
sont généralement supérieurs aux taux rachidiens.
Le dosage de l’interféron dans le liquide céphalo-
rachidien est un bon marqueur de méningite virale,
mais n’est actuellement pas disponible en urgence.

Plus récemment, des taux élevés d’interféron αont été
décrits dans le liquide céphalo-rachidien au cours du
syndrome d’Aicardi-Goutières, encéphalopathie pro-
gressive caractérisée par un arrêt du développement
psychomoteur dans les premiers mois de vie (transmis-
sion autosomique récessive).
Interférons et thérapeutique
Par ailleurs, les interférons sont utilisés en thérapeu-
tique dans certaines indications, mais àcejour, les
dosages ne sont pas contributifs au suivi thérapeutique
des patients. Il s’agit d’interférons recombinants,
type α2a, α2b, â1a et â1b. De nombreux effets indé-
sirables sont notés :apparition d’anticorps anti-
interféron, syndromes pseudo-grippaux, nausées,
troubles hématologiques avec leucopénie, thrombo-
cytopénie, nécessitant une surveillance clinique et bio-
logique rapprochée :
•en cancérologie :l’interféron αaune autorisation de
mise sur le marché pour le traitement de la leucémie
àtricholeucocytes, des leucémies myéloïdes chro-
niques et du sarcome de Kaposi. Au cours des méla-
nomes, myélomes, lymphomes non hodgkiniens,
cancer du rein métastatique ou récidivant, l’interfé-
ron αest actif dans 5à65 %des cas avec ou sans
association àlachimiothérapie ;
•en infectiologie :principalement dans la prise en
charge des hépatites Cdepuis que la pégylation de
l’interféron àdupolyéthylène glycol (IFN-PEG) aper-
mis de multiplier la demi-vie de l’interféron par 40,
ce qui apermis d’obtenir des concentrations plus
stables et prolongées sur la semaine, et donc une tolé-
rance et une efficacité augmentées ;
•dans la sclérose en plaques :deux interférons â1a et
un interféron â1b sont disponibles pour la prise en
charge du traitement de fond.
☞Entérovirus, Hépatite C, Herpès simplex virus, TNF-
α
(DubosF,Lorrot M, Soulier M, RozenbergF,Lebon P, Gendrel D.
Production d’interféron alphadanslesérum destrès jeunes nourrissons
lorsd’infectionsvirales.
Méd MalInfect 2004 ;34:361-365.
Lebon P.
Interféronsetmaladiesinfectieuses.
EMC -Maladiesinfectieuses1997 ;8-006-I-10, 8p.
1
/
2
100%