Lymphome cardiaque primitif obstructif

Cas anatomoclinique
H´
ematologie 2012 ; 18 (4) : 250-2
Lymphome cardiaque primitif obstructif
Obstructive primary cardiac lymphoma
Thouraya Filali1
Dhaker Lahidheb1
Walid Ghodbene2
Wafa Fehri1
Slim Chenik2
Habib Haouala1
1Service de cardiologie,
hôpital militaire de Tunis,
Tunisie
2Service de chirurgie cardiaque,
hôpital militaire de Tunis,
Tunisie
Le lymphome cardiaque primitif (LCP) est la tumeur cardiaque pri-
mitive la plus rare (1,3 %) [1]. Cette entité exceptionnelle, parfois
même discutée, correspond à un lymphome confiné exclusivement
au cœur et/ou au péricarde, sans autre localisation extracardiaque
au moment où le diagnostic a été posé [2]. Le LCP est à distinguer
de l’extension cardiaque des lymphomes non hodgkiniens, plus commune et qui
complique9à27%deslymphomes disséminés [3]. En raison de symptômes car-
diaques peu spécifiques, le diagnostic de la localisation cardiaque est rarement fait
du vivant du malade [4, 5]. Le pronostic spontané à court terme est constamment
défavorable à cause d’une prolifération tumorale rapide d’où l’urgence diagnos-
tique et thérapeutique de cette affection [6]. Nous rapportons le cas d’une patiente
chez qui une insuffisance cardiaque droite subaiguë par obstacle intracardiaque
droit subocclusif et un trouble conductif ont été le mode de révélation d’un énorme
LCP.
Observation
Il s’agit d’une patiente de 30 ans sans antécédents pathologiques particuliers qui
a été hospitalisée pour exploration d’une dyspnée récente d’aggravation rapide
avec syncopes évoluant depuis trois semaines. À l’examen, on a noté un rythme
cardiaque irrégulier à 75 bpm, une TA à 90/60 mmHg ainsi que des signes francs
d’insuffisance cardiaque droite, le reste de l’examen étant sans anomalies. La
radiographie du thorax était sans particularités. L’électrocardiogramme a montré
un bloc auriculoventriculaire de 2edegré de type Mobitz II. L’échocardiographie
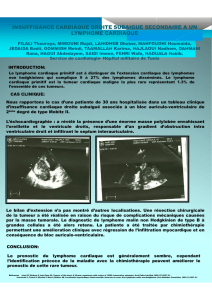
transthoracique (ETT) a mis en évidence une énorme masse d’échostructure hété-
rogène polylobée très mobile à large base d’implantation sur la paroi latérale de
l’oreillette droite (OD), mesurant 70 ×46 mm (figure 1). Cette masse s’enclavait à
travers l’orifice tricuspide pour passer dans le ventricule droit (VD), créant un obs-
tacle au remplissage du VD avec un gradient de pression moyen transtricuspide
à 9 mmHg. Il y avait aussi un épanchement péricardique rétro-auriculaire droit et
en regard du VD de 10 mm. La veine cave inférieure était dilatée non compliante.
À l’échographie transœsophagienne (ETO), on a noté un épaississement notable
du septum interauriculaire qui paraissait infiltré (figure 2). Le bilan d’extension
n’a pas révélé d’autres localisations. En raison du caractère obstructif de cette
grosse masse intracardiaque et du risque embolique majeur, mettant en jeu le
pronostic vital immédiat, la patiente a bénéficié en urgence d’une résection chirur-
gicale de la tumeur. L’examen macroscopique de la tumeur a montré qu’elle était
formée par une multitude de masses ovoïdes de couleur nacrée et de consistance
cérébroïde très friables, rassemblées en grappe de raisin (figure 3). L’examen ana-
tomopathologique a révélé qu’il s’agissait d’un lymphome malin non hodgkinien
de type B à grandes cellules. Une chimiothérapie a alors été entreprise en urgence
250
Tir´
es `
a part :
T. Filali
doi:10.1684/hma.2012.0729
H´
ematologie, vol. 18, n o4, juillet-août 2012
Pour citer cet article : Filali T, Lahidheb D, Ghodbene W, Fehri W, Chenik S, Haouala H. Lymphome cardiaque primitif obstructif. H´
ematologie 2012 ; 18 (4) :
250-2 doi:10.1684/hma.2012.0729
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

V
5
10
15
Figure 1. Grosse masse polylobée comblant l’OD et s’enclavant
à travers l’orifice tricuspide dans le VD (ETT coupe apicale quatre
cavités).
V
5
10
Figure 2. Masse tumorale comblant l’OD et s’enclavant à travers
l’orifice tricuspide dans le VD avec épaississement et infiltration du
septum interauriculaire (ETO).
permettant une évolution rapidement favorable avec régres-
sion de l’infiltration septale et affinement de cette paroi,
permettant la récupération d’une conduction auriculoventri-
culaire normale. La patiente est en rémission depuis dix mois.
Discussion
Le LCP a été décrit surtout dans la population de patients
immunodéprimés, particulièrement ceux atteints du syndrome
Figure 3. Aspect macroscopique de la tumeur intracardiaque.
d’immunodéficience acquis ou les patients transplantés – le
LCP chez les patients immunocompétents, comme notre
patiente, étant exceptionnel [2, 3]. Il s’agit habituellement de
lymphomes non hodgkiniens de type B à grandes cellules [7].
Le LCP touche plus le sexe masculin, avec un âge moyen de
découverte aux alentours de 62 ans [6, 8].
Les cavités droites, et essentiellement l’oreillette droite, consti-
tuent le siège de prédilection de la tumeur [7]. L’invasion
de la séreuse péricardique est aussi classique, alors que
l’atteinte des cavités gauches ou du septum est beaucoup
plus rare. Les manifestations cardiaques sont la conséquence
de l’envahissement et de l’effet de masse qu’engendre la
tumeur ; elles dépendent de la structure cardiaque atteinte. À
côté des manifestations inhérentes à la masse tumorale exu-
bérante, des complications liées à l’infiltration myocardique
ont été rapportées. Dans une mise au point récente recen-
sant la majorité des cas (une soixantaine) de LCP répertoriés
dans la littérature médicale, le mode de révélation paraît peu
spécifique, dominé par l’insuffisance cardiaque, les compli-
cations péricardiques, les troubles conductifs et plus rarement
les complications emboliques, les troubles du rythme, etc. [9].
Chez notre patiente, l’enclavement de la grosse tumeur à
travers l’orifice tricuspide était responsable d’une obstruction
partielle, à l’origine des symptômes d’insuffisance cardiaque
droite subaiguë. Le bloc auriculoventriculaire est vraisembla-
blement la conséquence de l’atteinte des voies de conduction
par l’infiltration septale.
Le diagnostic de masse intracardiaque est généralement
porté par l’ETT. L’ETO a permis de s’affranchir des limites
de l’ETT en permettant d’affiner davantage l’analyse de ces
masses. Le LCP se présente habituellement sous forme d’une
masse irrégulière inhomogène polylobée [4], associée par-
fois à une infiltration myocardique [10]. Dans notre cas, à
H´
ematologie, vol. 18, n o4, juillet-août 2012
251
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

côté de la grosse tumeur, l’aspect infiltré du septum à l’ETO
laissait déjà présager une étiologie maligne.
Les autres examens d’imagerie (scanner, PET-scanner, IRM)
permettent de bien quantifier la masse tumorale, de préci-
ser ses rapports ainsi que de réaliser un bilan d’extension
[6]. Toutefois, la sensibilité de l’IRM est meilleure que celle
du scanner [6, 7] et elle constitue actuellement l’examen
de référence dans le diagnostic des tumeurs cardiaques
[11]. Le diagnostic formel du LCP se fera par biopsie endo-
myocardique percutanée transveineuse, sinon chirurgicale
par médiastinoscopie ou par thoracotomie [6, 12]. En cas
d’atteinte péricardique [7], l’analyse cytologique du liquide
de ponction ou, mieux, la biopsie péricardique, seront une
alternative diagnostique.
Le traitement du LCP rejoint celui des lymphomes de haut
grade [6] et repose sur la chimiothérapie. Le traitement
chirurgical n’a habituellement pas de place dans la stratégie
thérapeutique, à l’exception de quelques cas rapportés [1],
comme le nôtre, où une résection chirurgicale urgente était
indispensable à cause du caractère obstructif de cette grosse
tumeur.
Il importe de souligner aussi la place de l’échocardiographie
dans le suivi des lymphomes sous chimiothérapie, permettant
de moduler le schéma thérapeutique pour en optimiser la
réponse [4, 5, 10]. Plus encore, l’ETO [5] a été utilisée afin
d’ajuster le protocole de chimiothérapie lorsqu’en début du
traitement, une réponse explosive, due à une nécrose mas-
sive de la tumeur, est constatée, car une telle réponse peut
être délétère de par le risque d’embolie massive [6, 10],
voire de perforation septale ou de rupture cardiaque
mortelle [3-5]. À côté de l’IRM, le PET-scanner constitue un
examen performant dans le suivi évolutif des patients traités
[6, 8].
La localisation cardiaque est un facteur de mauvais pronostic
avec une survie, en l’absence de traitement, ne dépassant
pas un mois [6]. Cependant, le pronostic du lymphome
cardiaque, considéré globalement comme sombre, semble
s’améliorer avec l’essor des nouveaux protocoles de chi-
miothérapie, et notamment avec l’adjonction du rituximab
au schéma thérapeutique [5], et certains auteurs rapportent
même des cas de survie prolongée [2]. Il n’en reste pas
moins que le pronostic à moyen et à long terme reste menacé
par la tendance classique de la maladie lymphomateuse aux
récidives et à la diffusion systémique [11].
En conclusion, le LCP est une tumeur rarissime dont la
pathogénie reste obscure [7]. La chimiothérapie représente
l’essentiel du traitement des lymphomes cardiaques et doit
être entreprise en urgence. L’option chirurgicale est à réser-
ver uniquement en cas de complication mécanique avec
répercussion hémodynamique.
RÉFÉRENCES
1.Mohamed A, Cherian S, El-Ashmawy A, et al. Unusual origin
and rare presentation of primary cardiac lymphoma. Tex Heart Inst J
2011 ; 38 : 415-7.
2.Bagwan IN, Desai S, Wotherspoon A, et al. Unusual presenta-
tion of primary cardiac lymphoma. Interact Cardiovasc Thorac Surg
2009;9:127-9.
3.Ban-Hoefen M, Bernstein SH, Bisognano JD, et al. Sympto-
matic intracardiac diffuse large B-cell lymphoma. Am J Hematol
2009 ; 84 : 683-5.
4.Trifunovic D, Vujisic-Tesic B, Vuckovic M, et al. Multimodality imaging
in the assessment of cardic lymphoma presented as new-onset atrial
fibrillation. Echocardiography 2010 ; 27 : 332-6.
5.Takaya T, Takeuchi Y, Nakajima H, et al. The usefulness of tran-
sesophageal echocardiographic observation during chemotherapy for
cardiac metastasis of non-hodgkin lymphoma complicated with left dias-
tolic collapse. J Cardiol 2009 ; 53 : 447-52.
6.Roubille F, Massin F, Cayla G, et al. Lymphome intracardiaque avec
insuffisance cardiaque droite: à propos de deux cas. Arch Mal Coeur
Vaiss 2007 ; 100(12) : 1025-9.
7.Faganello G, Belham M, Thaman R, et al. A case of primary cardiac
lymphoma: analysis of the role of echocardiography in early diagnosis.
Echocardiography 2007 ; 24 : 889-92.
8.Castelli JB, Alexandre L, Futuro G, et al. Primary cardiac lym-
phoma detected by 18F-FDG PET scan: a case report. J Nucl Cardiol
2011 ; 18 : 974-7.
9.Miguel CE, Bestetti RB. Primary cardiac lymphoma. Intern J Cardiol
2011 ; 149 : 358-63.
10.Gaspar A, Salomé N, Nabais S, et al. Echocardiographic assess-
ment of a cardiac lymphoma: beyond two-dimensional imaging. Eur J
Echocardiogr 2009 ; 10 : 975-8.
11.Mioulet D, Braem L, Heno P, et al. Flutter atrial révélateur de
l’extension cardiaque d’un lymphoma malin non hodgkinien. Ann Car-
diol Angeiol 2009 ; 58 : 117-27.
12.Benhamed L, Hysi I, Juthier F, et al. Primary cardiac extrano-
dal B-cell lymphoma mimicking right atrial thrombus. Ann Thorac Surg
2011;91:5.
252
H´
ematologie, vol. 18, n o4, juillet-août 2012
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
1
/
3
100%