Neurotransmission-2013

I Mécanismes généraux de la
neurotransmission
•1. Définition et aperçu historique de la neurotransmission
•2. Comparaison hormone-neuromédiateur
•3. Propriétés des neurotransmetteurs
•4. Mécanisme d’exocytose
•5.Neurotoxines à action présynaptique
•6. Nature chimique, biosynthèse et inactivation des neuromédiateurs.
•7. Récepteurs ionotropique et métabotropique
•8. Sommation spatio-temporelle et genèse du potentiel d’action

Prix Nobel de médecine et physiologie
•1906: Camillo GOLGI et Santiago RAMON Y CAJAL découvrent
la structure du neurone.
•1932: Sir Charles Scott SHERRINGTON et Edgar Douglas
ADRIAN: découvrent le fonctionnement des neurones.
-Neurotransmission inhibitrice.
- Le terme synapse est créé.
•1936: Sir Henry Hallett DALE et Otto LOEWI : découvrent la
neurotransmission cholinergique.
•1970: Sir Bernard KATZ , Ulf VON EULER, Julius AXELROD
découvrent la neurotransmission noradrenergique.

Hormone Transmission synaptique
Directe Transmission synaptique
diffuse
Propriétés des neuromédiateurs
D’après: Neuroscience, 2nd edition. Purves, Augustine, Fitzpatrick, Katz, McNamara,
Williams (eds). Sinauer Associates

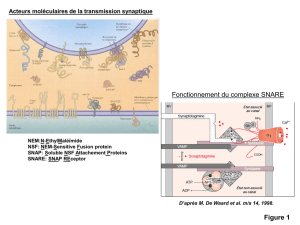
1.4. Acteurs moléculaires de l’exocytose
NEM:N-EthylMaléïmide = réactif
NSF: NEM-Sensitive Fusion protein = ATPase cytosolique
SNAP: Soluble NSF Attachement Proteins = partenaire de NSF
SNARE: SNAP Receptor = cibles de de SNAP
D’après: Neuroscience, 2nd edition. Purves, Augustine, Fitzpatrick, Katz, McNamara,
Williams (eds). Sinauer Associates
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
1
/
35
100%