Chapitre 5

CHAPITRE 5
Les transformations chimiques

I) Les réactions entre acide et métaux.
A C T I V I T E 1C O N C L U S I O N
1) Les ions présents dans l’acide chlorhydrique.
L’acide chlorhydrique contient des ions H+et des ions Cl-.
pH=1 : La solution est
acide et contient donc des
ions H+.
Le Test au nitrate d’argent
met en évidence les ions Cl-

I) Les réactions entre acide et métaux.
A C T I V I T E 2C O N C L U S I O N
2) Réaction avec le Fer.
Lors de la réaction de l’acide
chlorhydrique sur le Fer, il y
a apparition de bulles de
dihydrogène (H2)
POP

I) Les réactions entre acide et métaux.
3) Que reste-t-il dans le tube?
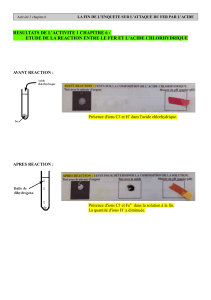
A la fin de la transformation chimique, nous observons la
présence d’ions Fe2+ et Cl-.Les ions chlorure sont présents au
début et à la fin de la transformation. Ils sont spectateurs et
ne réagissent pas!
Nitrate d’argent
Hydroxyde de
sodium ( Soude)
Dihydrogène

On observe également la diminution du pH qui montre une
diminution de la quantité des ions H+. Ils se sont transformés
en molécule de dihydrogène (H2)
H+
H+
Fe
Cl-
H+
H+
Cl-
Cl-Cl-
H+
Cl-
Cl-
Cl-
Cl-
H+
Fe2+
4
1
H
H
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%