Les éléments

Univers Non Vivant
La matière et l’énergie
(Les éléments)

Les éléments
Les éléments sont des briques qui permettent
de construire l’Univers.
On a identifié environ 100 éléments différents
qui sont à la base de toute matière.
92 àl’état naturel, 110 au total
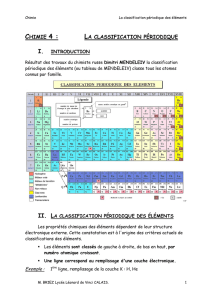
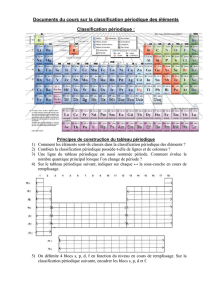
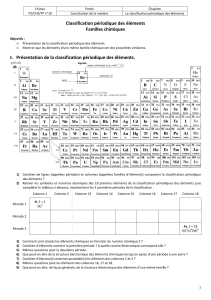
Tous les éléments sont classés dans tableau
Le tableau périodique

Classification des éléments
Tableau périodique
Dimitri Ivanovitch Mendeleïev en 1869

Chaque élément est classé en ordre
croissant par rapport à sa masse atomique.
Chaque élément est classé par groupe
(colonne) qu’on appelle aussi famille.
Les éléments d’une même famille
possèdent des propriétés semblables
**Toute matière est composée d’un
ou de plusieurs atomes**
Les éléments chimiques à la base
de la matière
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
1
/
16
100%