Phase

LE PHENOTYPE malin
Dr. Valentin CERNEA
Institute Oncologique “Prof. Dr. I. Chiricuţa”
Cluj, ROMANIA

PROLIFERATION DES TISSUS NORMAUX
Tissus rapidement prolifératives
Moelle
Gastrique, mucosité intestinale
Le tissu épithélial ovarien,
Le tissu épithélial testiculaire
La peau
Tissus lentement prolifératives
Poumon,
Foie,
Rein,
Tissu glandulaire endocrine,
Endothélium vasculaire.
Tissus nonprolifératives
Muscle,
Os,
Cartilage,
Nerveux.

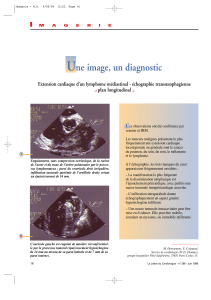
Invasion locale (1)
La phase pré-invasive
Perte du contact cellule-
cellule
Prolifération et croissance
des cellules tumorales sont
limitées au compartiment
épithélial d’origine
Membrane de base
collagène type IV
laminine.
Prolifération initiale
Carcinome in situ
Tissu
Normal Cancer
invasive
Carcinome
in situ

Invasion locale (2)
La phase invasive
Cellule tumorale
Pénétration de la
membrane de base
Cancer micro invasive
Cancer invasive.
Masse tumorale
Invasion des
lymphatiques
Invasion des vaisseaux
sanguines,
Métastase
Tissu
normal Cancer
invasive
Carcinome
in situ

Invasion locale (3)
Importance de la membrane de
base (MB)
MB - la première barrière contre
l’invasion tumorale.
La spécialisation matrice
extracellulaire représente une
« LIMITE » avec le tissu de
connection
Éléments constitutives
Laminine
Collagène de type IV
Fibronectine
Rôle physiologique
Morphogenèse
Différentiation
Maintenance du tissu architecture
et adhésion cellulaire
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
1
/
18
100%