Crise aiguë drépanocytaire Diagnostic, traitement

Crise aiguë drépanocytaire
Diagnostic, traitement
Damien LIPP
DESC Réa Med
2ème année
Session St-Etienne 2005

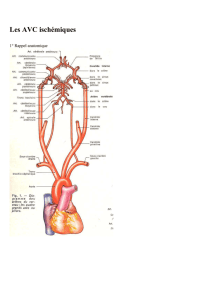
Rappels
•Drépanocytose: 1/3500 naissances en F
•Transmission autosomale récessive (Chr 11)
•Hémoglobinopathie affectant la chaine βde l’
hémoglobine (Hb S remplace l’ Hb « normale » Hb A
α2β2)
•Répartition géographique:
– Toute l’ Afrique, la péninsule Arabique, le pourtour
méditerranéen, le moyen-Orient, Madagascar, Réunion
–Inde
–Amérique centrale, Antilles
• Sélectionnée par l’évolution? (répartition=paludisme)

Rappels
•Conséquences:
–Hémolyse chronique (anémie)
–Falciformation (favorisée par l’hypoxie, l’acidose)
•Les hétérozygotes AS sont asymptomatiques
(falciformation en cas d’hypoxie sévère)
•Les homozygotes SS ou doubles hétérozygotes
SC, SD, SE, Sβthal présentent la maladie
•Pathologie de l’enfant et de l’adulte jeune

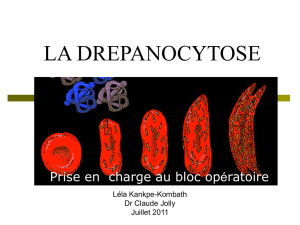
La falciformation
Chaîne de globine:
Ac. Glutamique remplacé par
valine en position 6
Polymérisation
HbS
Stase
sanguine
Drépanocytes
Acidose
hypoxie
Vaso-occlusion
Hyperplasie
intimale
(réaction
endothéliale)

Tableaux cliniques
•Enfant avant 3 mois: indemne (HbF), dépistage néonatal
•3 mois à 5 ans
–Anémie par séquestration splénique aiguë
–Infections à germes encapsulés (asplénie fonctionnelle
nécessitant les vaccinations et la pénicillinothérapie au long
cours)
–Crises vaso-occlusives (dactylite aiguë, infarctus spléniques, des
os longs (+/- ostéomyélite à salmonelles), des GG
mésentériques, priapisme
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
1
/
18
100%