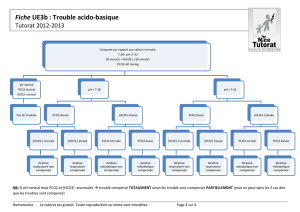
Troubles de l`équilibre acidobasique

TROUBLES DE
L'EQUILIBRE ACIDO –
BASIQUE
Dr Tahraoui Zoulikha MAITRE ASSISTANTE ANESTHESIE
REANIMATION

1. Définition
2. Régulation dé l’équilibre acido-basique
3. Acidose métabolique
4. Acidose respiratoire
5. Acidose métabolique
6. Alcalose respiratoire
7. conclusion

DEFINITION
Modifications des concentrations sanguines des ions H+, des
bicarbonates et de l'acide carbonique, responsables de variations de
la valeur du pH sanguin.
INTERET
Minimes, elles n'entraînent pas de traitement spécifique en
dehors du traitement de la cause.
Majeures, elles peuvent engager le pronostic vital et appellent
un traitement visant à corriger le trouble et simultanément
un traitement étiologique.

Acide :
molécule capable de libérer des ions H+
Base :
molécule capable de capter des ions H+
Equilibre acido-basique
l’organisme contient des composés acides et des composés
basiques qu’il doit maintenir à un état d’équilibre constant
4

Le pH sanguin= 7,40
Bicarbonatémie entre 12-20 mmol/l
pCO2 de 36 à 40 mmHg
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
1
/
37
100%