RVR - 16.10 1 - Accueil xcazer.fre.fr

H. Bobby Gaspar,1, Emma Bjorkegren, Kate Parsley, Kimberly C.
Gilmour, Doug King, Joanna Sinclair, Fang Zhang, Aris
Giannakopoulos, Stuart Adams, Lynette D. Fairbanks, Jane
Gaspar, Lesley Henderson, Jin Hua Xu-Bayford, E. Graham
Davies, Paul A. Veys, Christine Kinnon,1 and Adrian J. Thrasher1
Molecular Immunology Unit, Institute of Child Health, University College
London, 30, Guilford Street, London WC1N 1EH, UK Department of
Clinical Immunology and Bone Marrow Transplantation, Great Ormond
Street Hospital NHS Trust, Great Ormond Street, London WC1N JH, UK
Purine Research Laboratory, Guys and St Thomas’ Hospital, London Bridge
Road, London SE RT, UK
Bui Laurent

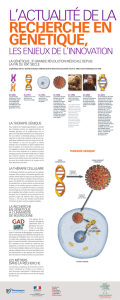
Introduction
ADA = Enzyme qui catalyse l'hydrolyse de
l'adénosine en inosine avec l'élimination de
l'ammoniaque.
L'inosine elle-même donnant l'hypoxanthine sous
l'influence d'une purine nucléoside phosphorylase.
L'inhibition de l'adénosine déaminase tend à
augmenter la concentration d'adénosine.

ADA-SCID
Un déficit de l’Adenosine DéAminase (ADA) entraine
un développement anormal des cellules T, B et NK.
Ce qui donne un déficit immunitaire combiné sévère
(SCID, severe combined immunodeficiency disorder).
Maladie génétique rare qui sans traitement cause des
infections chroniques et des troubles du
développement pouvant amener à la mort dans les
premières années de la vie.

Traitements possibles
ADA-SCID patient
Untreated
Death
Infection
HSCTransplantation PEG-ADA Gene Therapy
Survival > 85%
Good
immunological
and Biochemical
correction
Overall survival good
Variable immun reconstitution
Lymphopenia
Defects LT
< Thymus output
Susceptibility to Viral infection
?

Thérapie Génique
Tri des cellules CD34+
de la moelle osseuse du
patient (PEG-ADA)
25-30 % de
transduction efficace
on réinjecte 1,4 M de
CD34+ADA+/kg
Arrêt pendant 1 mois du
traitement PEG-ADA
Après 2j d’un
traitement Melphalan
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
1
/
15
100%