2 - Edimark

ASBMR 2008La Lettre du Rhumatologue
Chapitre II.
Ostéoporose
Traitements

La Lettre du Rhumatologue ASBMR 2008 - D’après Farina E. et al., Boston, États-Unis, abstract F341, actualisé
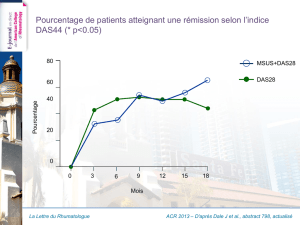
Ces données suggèrent un possible rôle bénéfique sur la santé osseuse
des acides gras essentiels chez la personne âgée
DMO plus élevée chez la personne âgée consommant du
poisson et des acides gras essentiels (AGE) :
étude Framingham
Nutrition et vitamines
0,76
0,74
0,72
0,70
0,68
0,66
0,64
0,62
0,60
0,58
0,56 N-3 EFA apports
(FN) N-3 EFA apports
(TROCH) N-6 EFA apports
(FN)
Q1
Q2
Q3
Q4
*
*
**
* p < 0,05 relatif
au 1er quartile
DMO initiale (g/cm²) par quartile d’apports
en AGE chez les femmes
35

La Lettre du Rhumatologue ASBMR 2008 - D’après Samelson E.J. et al., Boston, États-Unis, abstract 1207, actualisé
Prendre du calcium n’est pas associé à une augmentation
des calcifications artérielles des coronaires
Nutrition et vitamines
Cette étude ne confirme pas l’hypothèse selon laquelle des apports calciques
élevés augmenteraient les calcifications artérielles coronariennes (CCA)
Score de CCA moyen par quartile d’apport calcique total
Q1 Q2 Q3 Q4
0
3
6
4,5
2,29
4,46
2,44
4,06
2,34
4,25
2,35
p pour tendance = 0,95
p pour tendance = 0,27
Hommes Femmes
438 677 907 1 541
525 926 1 331 1 956
Hommes
Femmes
Score de CCA
36
Moyenne en mg

La Lettre du Rhumatologue
Nutrition et vitamines
Stress oxydatif
Radicaux oxygénés
Antioxydants
→Vitamine C
Procollagène Collagène
Ostéoclastes et
résorption
osseuse
NF κB1, NF κB2
Activation
1,4
1,2
1
0,8
0,6
0,4
0,2
0
Ref
T1
(médiane = 97 mg/j) T2
(162 mg/j) T3
(305 mg/j)
1,20
0,73
0,45
0,98
0,56
0,31
Tertiles d’apport total en vitamine C (mg)
Apport total de vitamine C et risque de fracture de hanche
Risque relatif
1,4
1,2
1
0,8
0,6
0,4
0,2
0
Risque relatif
T1
(sans) T2
(médiane = 60 mg/j) T3
(260 mg/j)
Catégories de suppléments en vitamine C (mg)
Ref 1,24
0,50
0,20 0,13
0,30
0,73
Suppléments en vitamine C et risque de fracture de hanche
Apport de vitamine C et risque de fracture de hanche
ASBMR 2008 - D’après Sahni S. et al., Boston, États-Unis, abstract 1168, actualisé
37

La Lettre du Rhumatologue
Supplémentation en vitamine D : D2ou D3?
ASBMR 2008 - D’après Binkley N. et al., Madison, États-Unis, abstract SU425, actualisé
Ces résultats préliminaires suggèrent que la vitamine D3est plus efficace
que la vitamine D2
Essai randomisé en double aveugle de 12 mois, conduit chez 64 sujets, comparant
l’efficacité de la vitamine D2(1 600 UI/j ou 50 000 UI/mois) à la vitamine D3(1 600 UI/j
ou 50 000 UI/mois)
Données préliminaires : 19 patients avec un suivi de 12 mois
Mesure du taux de 25-OH D à 1, 2, 3, 6, 9 et 12 mois
0 1 2 3 6 9 12
0
4
8
12
16
D2quotidienne D3quotidienne
Mois
Variation moyenne des taux
de 25-OH D (ng/ml)
0 1 2 3 6 9 12
0
4
8
12
16
D2 mensuelle D3 mensuelle
Mois
D3
D2
D3
D2
0
10
20
30
40
50
60
70
80
Variabilité individuelle du taux
de 25-OH D sous D2ou D3(ng/ml)
Quotidienne Mensuelle
38
Nutrition et vitamines
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
1
/
31
100%