Les nouveaux traitements de la SEP.J.C. OUALLET.15-11

Les nouveaux traitements de
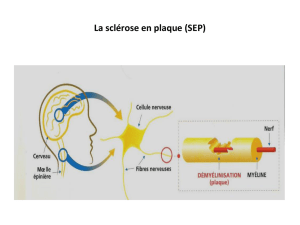
la sclérose en plaques
Dr Jean-Christophe Ouallet
CHU Pellegrin, Bordeaux
Réunion du réseau Aquisep 15/11/2014

Indications actuelles:
Escalade thérapeutique
Interférons
Copaxone
Aubagio
Tecfidera
Tysabri, Gilenya
Elsep

Les indications du Gilenya recommandées par l’AMM
européenne sont les mêmes que pour le Tysabri
DCINDICATIONS
•Tysabri est indiqué en monothérapie comme traitement de fond des formes très
actives de sclérose en plaques (SEP) rémittente-récurrente pour les groupes de
patients suivants :
•Patients présentant une forme très active de la maladie malgré un traitement par
interféron bêta.
Ces patients peuvent être définis comme n'ayant pas répondu à un traitement
complet et bien conduit par interféron bêta (habituellement d'une durée d'au moins
1 an). Les patients doivent avoir présenté au moins 1 poussée au cours de l'année
précédente alors qu'ils étaient sous traitement et doivent présenter au moins
9 lésions hyperintenses en T2 à l'IRM cérébrale ou au moins 1 lésion rehaussée
après injection de gadolinium.
Un « non répondeur » peut également être défini comme un patient dont le taux de
poussées n'a pas changé ou a augmenté par rapport à l'année précédente ou qui
continue à présenter des poussées sévères.
ou
•Patients présentant une sclérose en plaques rémittente-récurrente sévère et
d'évolution rapide, définie par 2 poussées invalidantes ou plus au cours d'une
année associées à 1 ou plusieurs lésion(s) rehaussée(s) après injection de
gadolinium sur l'IRM cérébrale ou une augmentation significative de la charge
lésionnelle en T2 par rapport à une IRM antérieure récente.

PEG-IFN
•Le Peginterferon beta-1a (PLEGRIDY) sous forme d’une injection SC tous
les 15 jours diminue le risque de progresson du handicap de 38% vs
placebo
4
Time on Study (weeks)
Proportion of Patients with
Disability Progression
Baseline 12 24 36 48
0.15
0.10
0.05
0
Placebo (n=500)
Peginterferon beta-1a q4w (n=500)
Peginterferon beta-1a q2w (n=512)
Hazard ratio (95% CI)*
q4w vs placebo=0.62 (0.40–0.97); P=0.0380
q2w vs placebo=0.62 (0.40–0.97); P=0.0383
Number of Patients at Risk
Placebo 500 483 458 439 352
q4w 500 474 456 427 348
q2w 512 482 453 430 355
Disability progression defined as ≥1.0 point increase on the EDSS from a baseline EDSS ≥1.0 sustained for 12 weeks or
≥1.5 point increase on the EDSS from a baseline EDSS of 0 sustained for 12 weeks.
*Based on Cox proportional hazards model, adjusted for baseline EDSS (<4.0 vs ≥4.0), and age (<40 vs ≥40 years).
Calabresi P et al. Presented at AAN; March 16–23, 2013; San Diego, CA. S31.006.

Peginterferon beta-1a
(PLEGRIDY): résultats sur 2 ans
•Diminution de 37% de la fréquence des
poussées (diminution de 49% des
poussées invalidantes)
•Diminution de 41% du risque de handicap
confirmé à 6 mois.
•Diminution de 66% des nouvelles lésions
actives en IRM
•Ces résultats sont très bons, car le groupe contrôle a reçu
l’interféron la seconde année.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
1
/
23
100%