Nouveaux anticoagulants oraux et fibrillation atriale

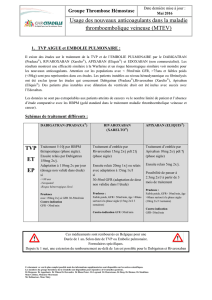
Nouveaux anticoagulants oraux et
fibrillation atriale non valvulaire:
23 Mars 2012
Dr M Martelet
CH LANGRES

Conflits d’intérêts
•Participations à des études cliniques
(Sanofi, BMS, Servier, Boerhinger,
Schering Ploug, Pfizer, Takeda, Daiichi
Sankyo, GSK, Novartis….)
•Animation de soirées


Recommandations ESC 2010:
score CHADS2-VASc ≥ 2: AVK (grade 1A)
= 1: AVK (grade 1A)
aspirine (grade 1B)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
1
/
24
100%