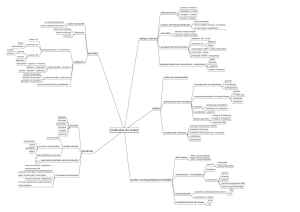
Comment fabriquer des molécules géantes appelées polymères ?

Comment fabriquer des molécules géantes appelées
polymères ?
1. Polymère
Un Polymère est une molécule géante (macromolécule), formée par la répétition d’un groupement
d’atomes appelé motif : il est obtenu par polymérisation de monomères.
Les Motifs sont formés par l’enchaînement d’une ou plusieurs molécule de base servant à la
synthèse du polymère, appelée monomère.
Les motifs se raccordent par liaison covalente au cours d’une réaction chimique de type addition,
condensation.
Le nombre de motif répété dans une macromolécule s’appelle degré de polymérisation noté DP ou
n. Il permet de déterminer la masse moléculaire moyenne du polymère :
2. Polymères obtenus par polyaddition
La polyaddition est l’addition en chaîne d’un grand nombre de monomères identiques, au cours de
laquelle il y a rupture des liaisons doubles carbone-carbone et formation de liaisons simples (ex : le
PVC, polyéthylène, polystyrène…)
Exercice :
1. Ecrire l’équation de polyaddition du PVC (Monomère : chlorure de vinyle (ou
chloroéthylène) CH2=CH-Cl) et l’équation de polyaddition du polyéthylène (Monomère :
éthène CH2=CH2)
2. Connaissant le motif du polystyrène obtenu par polyaddition, retrouver la formule du
monomère utilisé pour la synthèse du polystyrène.
3. Polymères obtenus par polycondensation
La polycondensation est une polymérisation qui s’effectue entre des monomères différents, au
cours de cette réaction il y formation de polymère avec élimination de petites molécules.
Les polyamides (nylon) :
En faisant réagir une diamine avec un diacide ou un dichlorure d’acyle, on obtient un polyamide par
polycondensation, avec élimination d’une molécule d’eau ou de chlorure d’hydrogène.
Equations de la réaction de synthèse du nylon (voir TP)

Les polyesters (tergal) :
En faisant réagir un dialcool avec un diacide, on obtient un polyester par polycondensation, avec
élimination d’une molécule d’eau :
Equations de la réaction de synthèse du tergal :
Les monomères sont l’acide téréphtalique et l’éthylène glycol :
Exercices 5, 6 p 34 et 13 p 36
4. Propriétés des polymères
Activité documentaire : le géotextile
Liaisons intermoléculaires :
Les chaînes d’un polymère peuvent être reliées entre elles soit par des liaisons
covalentes (liaison forte) soit par des liaisons de faible intensité, liaison
intermoléculaire, comme la liaison hydrogène : elle s’observe entre un atome
d’oxygène ou d’azote d’une molécule et un atome d’hydrogène d’une molécule
voisine. Cette interaction intermoléculaire donne à la matière une plus grande
cohésion.
Ex 2 page p 34

Propriétés thermiques :
Les thermoplastiques : PVC, polyamide, polyester, polystyrène
Leurs chaines à structure linéaire sont reliées par des liaisons faibles. Ils
peuvent se ramollir sous l’effet de la chaleur par rupture de ces liaisons
faibles : ils deviennent alors souples et malléables et prennent une nouvelle
forme lors du refroidissement.
Les thermodurcissables : bakelite (poignée de casserole)
Les chaines sont reliées par des liaisons covalentes leur donnant une structure
réticulée (tridimensionnelle). Ils vont prendre une forme définitive lors de leur
fabrication et ne pourront ni être refondus ni remodelés.
Les elastomères : caoutchouc, silicone
Ils sont soit thermodurcissables soit thermoplastiques
Propriétés mécaniques :
Les thermodurcissables sont souvent rigides et cassants tandis que les thermoplastiques et les
elasthomères possèdent une résistance thermique qui diminue quand la température s’élève.
Structure amorphe : l’arrangement des chaines est désorganisée (comme un plat de spaghettis
cuits !) : le matériau est résistant aux chocs, malléable et plastique
Structure semi-cristalline : l’arrangement des chaines est localement organisé et ordonné. Le
matériau est plus rigide et plus cassant (spaghettis crus)
Recyclage :
Tous les polymères thermoplastiques (80 % des matières plastiques utilisées) sont recyclables.
Ex 10 page 35
Animation : http://www.physique-appliquee-renaudeau.net/
LE POLYPROPYLENE COMME GEOTEXTILE
Le polypropylène a trouvé des débouchés dans les textiles techniques, où on l’emploie sous forme de
fils continus ou fibres. Il avait disparu du marché de l’habillement mais revient avec les progrès sous
le nom de polyoléfines.

Le polypropylène est synthétisé par addition d’un monomère.
1. Quel est le motif qui se répète ?
(voir rectangle rouge)
2. Sachant que le polypropylène est synthétisé par addition d’une molécule simple appelée
monomère (c’est à dire sans élimination de groupes d’atomes), déterminer quel est ce monomère ?
(Attention, la formule que vous allez proposer doit respecter les règles du duet et de l’octet)
Le monomère est le propène ou propylène. CH2=CH-CH3. On peut ici donner la réaction d’addition.
3. Pourquoi ce polymère peut-il être utilisé comme géotextile ? Quelles sont les liaisons qui ne
peuvent pas être cassées facilement ?
Les liaisons covalentes sont des liaisons ‘fortes’ qui ne peuvent être pas cassées facilement. Les
documents indiquent également que ce polymère est très résistant, qu’il est résistant chimiquement
etc …etc
4. En quoi la structure microscopique du polymère indique qu’il est hydrophobe ?
Ce polymère est hydrophobe car la chaîne carbonée ne contient aucun atome O, N… possédant de
doublet libre. Les atomes d’hydrogène ‘acide’ ou labile des molécules d’eau ne peuvent y établir de
liaisons.
1
/
4
100%