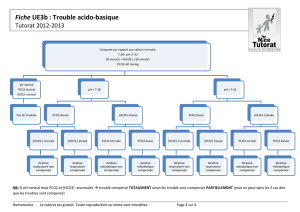
File - Cours L3 Bichat 2012-2013

Module Uro-Néphrologie – L3
PHYSIOLOGIE RENALE
Cours N°5
EQUILIBRE ACIDO-BASIQUE
M. Flamant - 19 Novembre 2012
Physiologie – Explorations Fonctionnelles Rénales
Hôpital Bichat

PREMIERE PARTIE
BILAN DES H+

I - INTRODUCTION
L’homéostasie des H+ permet le maintien constant de la concentration de H+
Sorties H+ =Entrées H+
Concentration [H+] régulée physiologiquement
. Par l’action conjuguée du rein et du poumon
EC
[H+] 36 – 44 nmoL
pH 7,38 – 7,42
IC
[H+] 100 nmoL
pH 7
. Concentration [H+] exprimée sous forme logarithmique pH= log(1/H+] )

II – SOURCES D’IONS H+
2 sources d’acides
1 – ACIDES VOLATILS = C02 produits par le métabolisme cellulaire
C
6
H
12
O
6
+ 6 O
2
==> 6 CO
2
+ 6 H
2
O + ATP
20.000 mmol CO2/j
IC
EC
ACIDES VOLATILS
- Quantité massive (20 mol/j)
- Non stockés (CO2 diffuse)
- Ce n’est qu’une acidité potentielle
-
Elimination ventilatoire
Acide gras
n Acetyl CoA
Beta oxydation
n tours
n NADH
n FADH2
NADH
FADH2
n Cycle de Krebs
ATP + H20
CO2
O2
Pyruvate
Glucose

2 – ACIDES FIXES
C
6
H
12
O
6
+ 6 O
2
==> 6 CO
2
+ 6 H
2
O + ATP
20.000 mmol CO2/j
IC
EC
ACIDES VOLATILS
- Quantité massive (20 mol/j)
- Non stockés (CO2 diffuse)
- Ce n’est qu’une acidité potentielle
-
Elimination ventilatoire
60 mmol/j Alimentation
ACIDES FIXES
- 60 mmol/j
- Vrai acidité
- Prise en charge par les systèmes tampons
- Elimination rénale
Tamponnement
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
1
/
56
100%