Hallucinations associées aux neurostimulants

Volume 58 – n° 7
novembre 2011
Pradax en
période
périopératoire ?
Leucémie
myéloïde
chronique
Fièvre
chez le jeune
enfant
WWW.PROFESSIONSANTE.CA
PP 40070230 1200, avenue McGill College, bureau 800, Montréal (QC) H3B 4G7
Hallucinations
associées aux
neurostimulants

ÉDITORIAL
WWW.PROFESSIONSANTE.CA NOVEMBRE 2011 VOL. 58 N° 7 QUÉBEC PHARMACIE 3
Éditrice Groupe Santé
Caroline Bélisle, 514 843-2569
[email protected]ogers.com
Directeur des rédactions, Groupe Santé
Rick Campbell, 416 764-3891
rick.campbel[email protected]om
Directrice de la rédaction
Caroline Baril, 514 843-2573
[email protected]ogers.com
Rédactrice en chef
Hélène-M. Blanchette, B. Pharm.
Rédacteur en chef adjoint
Jean-François Guévin, B. Pharm., M.B.A., Pharm. D.
Adjointe à la directrice de la rédaction
Mélanie Alain
Direction artistique
Dino Peressini
Graphistes
Jocelyne Demers, Pascal Gornick
Comité de rédaction
AVEZ-VOUS ENTENDU PARLER DE...
Isabelle Giroux, B. Pharm., M. Sc.
Caroline Sirois, B. Pharm., M. Sc., Ph. D.
À VOS SOINS
Sonia Lacasse, B. Pharm.
Sophie Grondin, B. Pharm., M. Sc.
À VOTRE SERVICE SANS ORDONNANCE
Nancy Desmarais, B. Pharm.
Julie Martineau, B. Pharm.
DE LA MÈRE AU NOURRISSON
Caroline Morin, B. Pharm., M. Sc.
D’UNE PAGE À L’AUTRE
Nicolas Paquette-Lamontagne, B. Pharm., M. Sc., M.B.A.
INFOROUTE
Jean-François Bussières, B. Pharm., M. Sc., M.B.A.
LES PAGES BLEUES
Odette Grégoire, B. Pharm., M. Sc., M.A.P.
PHARMACOVIGILANCE
Christine Hamel, B. Pharm., M. Sc.
PLACE AUX QUESTIONS
Noura A. Shahid, B. Pharm.
SANTÉ PUBLIQUE
Marie-Jahelle Desjardins, B. Pharm.
Membre honoraire
Georges Roy, M. Pharm.
Publicité
Directrices de comptes, Montréal
Josée Plante 514 843-2953
Pauline Shanks 514 843-2558
Directrices/Directeurs de comptes Toronto
Teresa Tsuji 416 764-3905
Norman Cook 416 764-3918
Sara Mills 416 764-4150
Stephen Kranabetter 416 764-3822
Carrières et professions, Montréal
Nancy Dumont 514 843-2132
Gestionnaire des projets spéciaux
Chantal Benhamron 514 843-2570
Coordonnatrice de la production
Rosalina Lento 514 843-2557
P-définitions
Pilulo-dépendance : état de gens d’une
société qui dépendent beaucoup des pilules.
Pharmacien : professionnel très au fait de la
pilulo-dépendance. Est souvent présent dans
une pharmacie, mais a aussi une vie en dehors
de la pharmacie. Par contre, est toujours phar-
macien ou pharmacienne, où qu’il soit.
Pharmacie : lieu où un ou des pharmaciens,
spécialistes de la pharmacothérapie, tentent
de réduire la pilulo-dépendance.
Pharmacothérapie : science qui est bien maî-
trisée par le pharmacien et qui lui permet de
faire des présentations magistrales aux pres-
cripteurs (voir dénition) et aux patients qui
boivent ses paroles.
Pilulo-décit : état d’une société qui dépense
beaucoup pour sa pilulo-dépendance.
Pénurie : médicament ou ensemble de médi-
caments non disponibles pour les pilulo-
dépendants. Processus par lequel on induit une
panique, généralement chez le patient. Proces-
sus par lequel on induit une panique, générale-
ment chez le pharmacien. Processus par lequel
on induit des protestations chez les médecins
qui sont contactés par les pharmaciens.
Pénurie : programme articiel d’épuisement
des professionnels.
Parasite : espèce de macro-organisme qui pro-
te de la pilulo-dépendance. Peut parfois créer
une pénurie par des décisions inappropriées.
Première ligne : système peu utilisé d’accès à
des soins de santé primaires, en développe-
ment cependant, avec un objectif d’avoir des
résultats il y a quelques années. Est souvent en
deuxième ligne. Lieu de pratique non privilé-
gié par beaucoup de jeunes prescripteurs.
Endroit où il y a encore moins de pharma-
ciens. Un jour, peut-être, la première ligne
sera en première ligne.
Patient : personne qui aime attendre dans les
salles d’urgence pour recevoir des soins de
première ligne.
Programme d’accès spécial : programme
géré par des fonctionnaires en mal de docu-
mentation pour donner une disponibilité à
des produits généralement non disponibles.
Pot de pilules : nom générique donné à un
pot contenant toutes sortes de choses qui ne
sont pas toujours des pilules. Peut contenir
des gélules, des capsules, des caplets, des
comprimés…
Professionnalisme : état d’âme du pharma-
cien ou du prescripteur qui réagit toujours
avec la même empathie lorsqu’il se fait poser
la même question pour la 38e fois de suite.
Au printemps, ce sont les allergies, à
l’automne, c’est le rhume et la grippe qui sont
les sujets primés.
Professionnel : s’applique à toutes sortes de
personnes. On peut aussi penser que le
patient le pense quand il pense à son phar-
macien qui vient de « désemberlificoter »
son régime de pilulo-dépendance ou qui
vient d’expliquer les eets indésirables asso-
ciés à sa pilulo-dépendance.
Préparation magistrale : une préparation
faite de main de maître. On peut avoir en tête
aussi une présentation magistrale d’un beau
pot de crème gentiment préparé.
Présentation magistrale : (synonyme de
préparation magistrale). Présentation d’un
argument par un pharmacien à un prescrip-
teur qui reconnaît son expertise et qui
accepte son opinion.
Préparation : période de sérénité que se
donne un pharmacien qui s’apprête à don-
ner son 38e conseil pour la grippe durant son
quart de travail.
Protection contre la grippe : souhait que le
pharmacien a face aux 38 patients qui lui
toussent dans la gure pour montrer com-
ment ils toussent quand ils ne sont pas
devant le pharmacien.
Prescription : généralement une façon pour
un prescripteur d’indiquer ce qu’il veut
qu’un patient fasse après qu’il a quitté son
bureau. Parfois, un prescripteur est proli-
que et prescrit la même molécule à tous les
patients qui sont venus le voir au cours des
quatre dernières heures. La prescription ne
génère pas toujours des succès puisque, mal-
gré la pilulo-dépendance, certains patients
ne se collent pas à leur programme de soins.
On peut remplacer « coller » par « adhérer ».
Prescripteur : un professionnel de la santé
qui prend une décision face à un problème
de santé et qui veut qu’un patient réalise des
actions à faire une fois qu’il a quitté le profes-
sionnel de la santé.
Prescrire : acte rééchi par un professionnel
de la santé et/ou un prescripteur qui prépare
un plan d’action dans son domaine d’exper-
tise. Généralement, acte qui n’est pas très
partagé pour éviter la perte de contrôle.
Promotion de la santé : 1 - mettre en vente
la santé par toutes sortes d’armations. Par
exemple, les vendeurs de produits naturels
ont parfois tendance à faire de la promotion
de la santé; 2 - pour les autres, la promotion
de la santé est de favoriser la santé par des
actions concrètes, publiques, qui ont ten-
dance à réduire la pilulo-dépendance.

WWW.PROFESSIONSANTE.CA NOVEMBRE 2011 VOL. 58 N° 7 QUÉBEC PHARMACIE 5
Les Éditions Rogers Media
Kenneth Whyte, Président
Patrick Renard, Vice-président, Finances
Janet Smith, Éditrice exécutive, Groupe Santé
Sandra Parente, Directrice générale de Rogers Connecte,
titres d’affaires et professionnels
WEB
David Carmichael,
Directeur général des activités en ligne
Tricia Benn,
Directrice principale, Études de marché
Rogers connecte
Pour nous joindre :
Québec Pharmacie, 1200 avenue McGill College,
bureau 800, Montréal (Québec) H3B 4G7.
Téléphone : 514 845-5141, Télécopieur : 514 843-2184,
Courriel : [email protected] ou
Éloïse Boucher, adjointe administrative
Tél. : 514 843-2102, eloise[email protected]
Abonnement ou changement d’adresse
Pour les pharmaciens
Ordre des pharmaciens du Québec
par courriel : [email protected]
par télécopieur : 514 284-3420
par téléphone : 514 284-9588
Pour les non-pharmaciens
1200, McGill College, bureau 800
Montréal (Québec) H3B 4G7
Francine Beauchamp, coordonnatrice de la diffusion
Tél. : 514 843-2594 • Téléc. : 514 843-2182
francine.beauchamp@rci.rogers.com
Tarifs : Canada : 69 $ par année, 103 $ pour 2 ans,
8 $ l’exemplaire. Tarif de groupe/vrac : 55,20 $
(min. 6 exemplaires).
États-Unis et international
(abonnement individuel
seul.) : 110 $ par année.
Taxes en vigueur non comprises.
Dépôt légal : Bibliothèque nationale du Québec,
Bibliothèque nationale du Canada ISSN 0826-9874.
Toutes les annonces de produits pharmaceutiques
sur ordonnance ont été approuvées par le Conseil consultatif
de publicité pharmaceutique.
Envoi de poste – publications, convention nº 40070230.
Québec Pharmacie est imprimé par
Imprimeries Transcontinental et est publié
8 fois l’an par Rogers Media.
Vous pouvez consulter notre politique environnementale à :
www.leseditionsrogers.ca/about_rogers/environmental.htm
SOMMAIRE
Volume 58 – n° 7 – novembre 2011
Vous trouverez les questions de formation continue
à la fin de chacun des articles.
3 ÉDITORIAL
P-définitions
6 PLACE AUX QUESTIONS
Peut-on utiliser le Pradax lors de l’arrêt
de la warfarine en période périopératoire ?
11
À VOTRE SERVICE SANS ORDONNANCE
L’automédication dans le cas de fièvre
chez l’enfant
21 LES PAGES BLEUES
Leucémie myéloïde chronique
31 AVEZ-VOUS ENTENDU PARLER DE...
Le prasugrel (EffientMD)
39 PHARMACOVIGILANCE
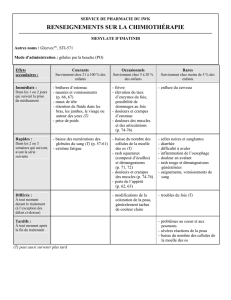
Hallucinations associées
à une formulation à libération
retardée de méthylphénidate
(ConcertaMD)
44 D’UNE PAGE À L’AUTRE
Impact des cabinets automatisés
décentralisés sur la baisse des erreurs
de médication en soins intensifs
46 Perspective sur la pratique pharmaceutique
hospitalière au Canada 2009-2010

6 QUÉBEC PHARMACIE VOL. 58 N° 7 NOVEMBRE 2011
Peut-on utiliser le Pradax
lors de l’arrêt de la warfarine
en période périopératoire ?
La warfarine est utilisée depuis très longtemps
comme traitement anticoagulant, entre autres
chez les patients sourant de brillation auri-
culaire (FA)1. L’anticoagulothérapie permet de
prévenir les événements thromboemboliques
ainsi que les accidents vasculaires cérébraux1,2,3.
Lorsque l’on commence un traitement par la
warfarine, il est nécessaire que le patient soit
traité conjointement par des injections d’hé-
parine4. En eet, la warfarine a un début d’ac-
tion très lent et peut prendre jusqu’à deux à
trois jours avant d’avoir un effet thérapeuti-
que4. Le traitement par l’héparine agit rapide-
ment et permet donc de prévenir la formation
de caillots sanguins durant la période pendant
laquelle la warfarine ne s’avère pas efficace4.
On utilise aussi les héparines lorsque l’on doit
cesser temporairement la warfarine en raison
d’une chirurgie entraînant un risque de sai-
gnements et que le patient est à risque moyen à
élevé d’événements thromboemboliques4,5.
Étant donné que la warfarine possède une lon-
gue demi-vie, on doit cesser la prise plusieurs
jours avant la chirurgie an de minimiser le
risque de saignements, ce qui expose malheu-
reusement le patient à un risque embolique
avant la chirurgie4,5. Les injections d’héparines
contribuent à prévenir la formation de caillots
durant l’arrêt de la warfarine4,5. Plusieurs pro-
fessionnels s’interrogent quant à la possibilité
d’assurer l’ecacité de la warfarine en début de
traitement ou lors de sa cessation en période
périopératoire grâce à un autre médicament
que les héparines4.
Une nouvelle molécule anticoagulante à
prise orale est maintenant disponible au
Canada, soit le dabigatran etexilate (Pra-
daxMD), un promédicament du dabigatran,
converti par les enzymes estérases dans le sang
et le foie2,3,6,7. Le Pradax est un inhibiteur direct
compétitif et réversible de la thrombine (fac-
teur IIa) avec une haute anité sélective2,3,6,7. Il
inactive la thrombine, un agoniste puissant de
l’agrégation plaquettaire, empêchant ainsi la
formation de caillots2,3,6,7. La simplicité d’ad-
ministration (prise orale plutôt qu’administra-
tion parentérale) et le coût moindre du dabiga-
tran portent à envisager la possibilité que cette
molécule devienne une solution de rechange
aux héparines4.
Toutefois, l’utilisation du dabigatran au lieu
des héparines pour combler l’efficacité de la
warfarine ne semble pas pouvoir être prise en
considération4. Il est vrai que le dabigatran a
Texte rédigé par Mélanie Lauzon, B. Pharm.
Texte original soumis le 14 juin 2011.
Texte final remis le 8 juillet 2011.
Révision : Elyse Desmeules, B. Pharm.,
et Geneviève Duperron, B. Pharm.
Tableau I
Avantages et désavantages du dabigatran (PradaxMD),
comparativement à la warfarine1-3,6,7
Avantages Désavantages
Dose fixe ne nécessitant pas de suivi Manque de données chez les patients
périodique insuffisants rénaux sévères et chez ceux atteints
de maladies hépatiques
Efficacité semblable à supérieure dans la pré- Manque de données de sécurité sur une longue
vention des thromboembolies et des accidents période
vasculaires cérébraux (étude RE-LY)
Moins d’interactions avec les médicaments Plus de risque de saignements gastro-
et les aliments intestinaux (à hautes doses)
Risque plus faible à comparable de compli- Administration BID entraînant une non-
cations importantes liées à des saignements observance possible
Aucun antidote permettant de renverser l’effet
anticoagulant
PLACE AUX QUESTIONS
Chez les patients souffrant de fibrillation auriculaire, la warfarine est utilisée comme traitement anticoagulant, conjointement avec des
injections d’héparine. On a aussi recours aux héparines lorsqu’il faut cesser la warfarine en raison d’une chirurgie pouvant entraîner des
saignements et que le patient est à risque d’événements thromboemboliques. Le dabigatran (PradaxMD), un nouvel anticoagulant,
pourrait-il être utilisé en remplacement des héparines en période périopératoire, lorsque la warfarine est cessée ?

WWW.PROFESSIONSANTE.CA NOVEMBRE 2011 VOL. 58 N° 7 QUÉBEC PHARMACIE 7
Peut-on utiliser le Pradax lors de l’arrêt de la warfarine en période périopératoire ?
un début d’action rapide, ce qui permet d’at-
teindre un effet thérapeutique environ deux
heures après la première dose, ce qui est com-
parable aux héparines4,7. Par contre, la demi-
vie de cette molécule varie entre 12 et 17 heu-
res, ce qui implique que son eet anticoagulant
peut persister jusqu’à deux jours après sa cessa-
tion3,4,7. Les héparines agissent et s’éliminent
rapidement4. Lors d ’une chirurgie, il est impor-
tant que le médicament anticoagulant admi-
nistré s’élimine rapidement an de diminuer
le risque de saignements associés à la chirur-
gie4,5. Aussi, il importe de réduire la période
durant laquelle l’effet anticoagulant ne se
retrouvera pas dans l’intervalle thérapeutique
an de minimiser le risque thromboemboli-
que4,5. Ces critères conviennent aux héparines
puisque celles-ci s’éliminent entre 12 et 24
heures après la dernière injection, mais mal-
heureusement pas au dabigatran4. De plus, le
dabigatran ne détient pas toutes les indications
pour lesquelles on doit protéger un patient
avec une héparine lors de la cessation de la
warfarine. En effet, selon les recommanda-
tions du journal médical Chest, les patients
porteurs d’une valve mécanique ainsi que ceux
atteints de brillation auriculaire ou ayant fait
une thrombose veineuse profonde qui sont
considérés comme à moyen ou à haut risque
thromboembolique doivent être couverts par
une héparine4,5. Le dabigatran n’étant pas indi-
qué chez les patients porteurs d’une valve
mécanique, il ne peut être utilisé an de rem-
placer la warfarine lorsque celle-ci doit être
cessée. Enn, le dabigatran peut parfois aug-
menter le rapport international normalisé
(RNI), rendant particulièrement dicile l’éva-
luation quand l’eet de la warfarine est réelle-
ment atteint ou dissipé4.
L’arrivée du dabigatran sur le marché a pro-
voqué des changements importants dans le
domaine médical puisque cette molécule com-
porte plusieurs avantages (tableau I) et s’avère
intéressante dans certaines conditions. Par
contre, elle ne peut malheureusement pas être
utilisée en remplacement des héparines en
période périopératoire, lorsque la warfarine
est cessée4. Toutefois, elle est utilisée en pré-
vention primaire pour éviter des événements
thromboemboliques chez les patients ayant
subi une chirurgie de la hanche ou du genou4,6,7.
Elle a aussi une indication ocielle en tant que
traitement anticoagulant de la brillation auri-
culaire non valvulaire4,6,7. ■
QUESTION DE FORMATION CONTINUE
Répondez maintenant en ligne. Voir page 62.
1) Lequel de ces énoncés est vrai ?
A. Le dabigatran a un mécanisme d’action semblable à celui de la warfarine.
B. On peut déterminer l’efficacité du dabigatran par une mesure du RNI
et ainsi ajuster le dosage.
C. Les héparines demeurent le traitement de choix lorsque la warfarine
doit être cessée en période périopératoire et que le patient est à risque élevé
de thromboembolie.
D. Le dabigatran a un début d’action et une élimination rapides,
comme les héparines.
Références
1. Anonyme. Pradax contre warfarine pour la fibrilla-
tion auriculaire. Pharmacist’s Letter Canadian. 2008;
24(8) : 240813.
2. Anonyme. Dabigatran vs warfarin in patients with
atrial fibrilation. Pharmacist’s Letter 2009;25(10) :
251023.
3. Reynen E. Résumé sur le dabigatran. L’hôpital d’Ot-
tawa, service d’information pharmacothérapeutique.
2010 : novembre.
4. Anonyme. Should Dabigatran be used for bridging ?
Pharmacist’s Letter 2011:27(3) : 270310.
5. Douketis JD, Berger PB, Dunn AS, et coll. The peri-
operative management of antithrombotic therapy :
American college of chest physicians evidence based
clinical practice guidelines (8th edition). Chest 2008;
133(6 supp) : 299S-339S.
6. Anonyme. Pradax (dabigatran) Pharmacist’s letter
2011; 27(1) : 270119.
7. Monographie du Pradax (dabigatran etexilate).
Boehringer Ingelheim Canada Burlington. ON L7L
5H4, octobre 2010.
Vous avez toujours voulu rédiger
un article de formation continue
pour
Québec Pharmacie
?
En voici l’occasion, puisque la chronique
Les Pages bleues
recherchent activement
des auteurs.
Les pharmaciens intéressés peuvent contacter
Odette
Grégoire (odette.gr[email protected]om).
VOUS AIMEZ ÉCRIRE ?
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
1
/
34
100%