Chapitre 2 : La classification périodique des éléments.

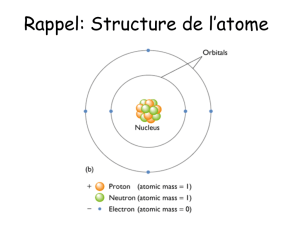
Architecture de la matière
Chapitre 2 : La classification périodique
des éléments
I ) Comment sont classés les atomes?
1 ) Le tableau historique de Mendeleïev
(1869)
Il a classé les éléments par masse
atomique croissante et par propriétés
physicochimiques semblables.


2 ) Construction de la classification
périodique moderne

3 ) Structure de la classification
périodique
●Les blocs
●Les familles
●Les périodes:
1ère ligne: H – He
2ème ligne: Lili Beaucoup But Chez Notre
Oncle Fernand Nestor
3ème ligne: Napoléon Mangea Allégrement Six
Poulets Sans Claquer d'Argent.

4 ) Métaux et non métaux (cf poly)
Certains éléments ont des propriétés qu’on regroupe sous le
terme de caractère métallique. Ces éléments :
●sont peu électronégatifs → ils sont réducteurs et forment des
cations
●sont bons conducteurs de la chaleur et de l’électricité
●Possèdent un éclat métallique
●possèdent des sous-couches de valence p peu remplies
Les non-métaux, au contraire, sont les atomes plutôt
électronégatifs . Ils sont donc en haut et à droite de la
classification périodique. L’hydrogène en fait également partie.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%