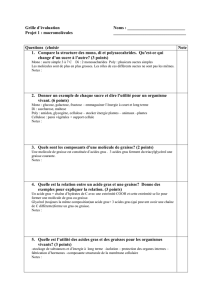
Chapitre 8 : Les acides carboxyliques I) Définitions et rappels

!"#$%&'#(%)*%')+"(#,,%')
-./0123)45)6345/785)
9:0;<)45)=;)>%,=+&*)&:?5;2)
;@516.;4A087BC.DEF;)
)
,5<)/:0;<)<5;:82)/:6@1323<)@.;)1.)<0725E)
!
!!!!!!
!9G.@72;5)H)I),5<)./745<)/.;?:JK17L05<)
)
#M *3F78727:8<)52);.@@51<)
!
Une!molécule!ayant!au!moins!une!fonction!carboxyle!est!un!acide!:!
!
!
!
L’oxygène!est!plus!électronégatif!que!le!carbone,!alors!la!liaison!carbone!–!oxygène!
est!polarisée!δ+!sur!le!carbone!et!δ@!sur!les!oxygènes.!
L’oxygène!a!un!effet!–I!et!le!groupe!OH!un!effet!+M.!L’effet!+M!l’emporte!sur!l’effet!
inductif,!par!conséquent,!le!carbone!du!carboxyle!sera!moins!polarisé!que!le!carbone!
d’un!carbonyle!d’une!cétone!ou!d’un!aldéhyde.!
!
##M >:25827.1723<);3./27B5<)4N08)./745)/.;?:JK17L05)
!
Le!centre!réactif!de!la!molécule!est!le!centre!carboxylique!:!
!
!
Le!centre!carboxylique!contient!deux!oxygènes.!La!mésomérie!met!en!évidence!le!
centre!le!plus!basique!et!le!plus!nucléophile!:!
!
O
C
OH
Fonction carbonyle
Fonction alcool
RUne fonction carboxyle = fonction carbonyle et
fonction alcool présentes sur le même carbone
Grandeur de liaison agrandie
pour une meilleure compréhension
O
C
O
R
H
Site basique et nucléophile
Véritable H acide
Site électrophile

!
,N:JKDO85)40)/.;?:8K15)5<2)15)<725)15)@10<)?.<7L05)52)15)@10<)
80/13:@G715E)
,5)/.;?:JK15)@:<<O45)085)78<.20;.27:8P)45<);3./27:8<)
4N.44727:8<)@50B582)Q2;5)F.725<E)
!8)80/13:@G715).22.L05;.)15)/.;?:85)315/2;:@G715)40)
/.;?:8K15.!
!85)?.<5).22.L05;.)1N:JKDO85)40)/.;?:8K15)
!
Les!acides!sont!plus!ou!moins!solubles!dans!l’eau,!c’est!la!chaîne!R!qui!influe!sur!la!
solubilité!:!
!
!
!
L’acide!peut!avoir!sur!le!carbone!en!α!un!hydrogène!possédant!un!caractère!
acide!:!
!
! !
! !
!
###M =:?71723)40)B3;72.?15)R)./745)
!
La!liaison!O@H!est!très!polarisée!:!
!
!
!
!
O
C
O
R
H
O
C
O
R
H
site plus basique
site plus nucléophile
O
HO
nSi n inférieur à 5, la solubilité est totale
Si n supérieur à 5 la solubilité diminue
O
HO
H
H
H à caractère acide
Ne sera pas traité en PACES
O
O
R
H
+
H
O
H
O
O
R
+
H
O
H
H
L'acide sera fort si la forme acétate est stabilisée

Plus!une!liaison!est!polarisée,!plus!elle!sera!solvatée!par!le!solvant!polaire!protique!
qu’est!l’eau.!
Plus!le!pKa!est!petit,!plus!l’acide!est!fort.!
Le!pKa!des!acides!carboxyliques!est!compris!entre!4!et!5.!
Le!pKa!des!alcools!est!18.!
La!forme!acétate!est!stabilisée!par!mésomérie!:!
!
!
!
! !
Quelques!exemples!de!pKa!pour!illustrer!:!
!
Acide! ! ! ! pKa!
!
CH3COOH!!!!4,80!
Cl2CHCOOH!!!1,29! ! effet!–I!des!chlores!
CH3CH2COOH!!!4,87! ! Effet!+I!du!CH3CH2!
!
Les! acides! carboxyliques! réagissent! spontanément! avec! les! bases! tels! que! NaOH,!
KOH,!etc…!
!
!
!
Le! corps! humain! est! composé! de! 70%! d’eau,! généralement,! les! médicaments! sont!
sous!forme!de!sel!hydrosoluble.!
!
#$M &3./27:8)4N5<23;7F7/.27:8)
!
La!réaction!d’estérification!est!une!attaque!nucléophile.!Elle!débute!par!une!addition!
nucléophile! sur! le! carbone! du! carbonyle! qui! est! suivie! d’une! élimination.! En!
définitive,!elle!correspond!à!une!réaction!de!substitution!nucléophile!:!
!
!
!
O
O
R
O
O
R
Si R a un effet -I, la force de l'acide augmente
Si R a un effet +I, la force de l'acide diminue
O
O
R
H
+
O
O
R
Na+OH-
Na++H2O
Sel soluble dans l'eau
O
O
R
H
+ R1OH
O
O
R
R1
+H2O
C'est une réaction équilibrée

A!première!vue,!on!peut!penser!qu’un!H!a!été!remplacé!par!le!groupement!R1.!En!
étudiant!le!mécanisme!réactionnel,!on!voit!bien!que!c’est!une!addition!nucléophile!
qui!est!suivie!d’une!élimination!:!
!
!
!
95225);3./27:8)5<2)/.2.1K<35)@.;)08)./745)+R!
!
Le!mécanisme!de!cette!réaction!en!catalyse!acide!:!
!
!
O
OH
R
+R1O
HO
C OH
O
R
R1
H
O
C OR1
R
+H2O
Addition nucléophile
Elimination de H2O
En conclusion, on obtient une substitution de H par R1
O
OH
R
+
O
OH
R
O
C
OH
R
A-H+
H
+A-
H
R1
O
H
+
OH
OH
O
R
H
R1
HO
C O
H
H
R
O
R1
C
O
OR1
R
H
+H2O
Présent dans la
solution
O
C
OR1
R
+
A-H+
+
H2O
Le catalyseur AH se retrouve en début et en fin de réaction.

!
«!Si!vous!trouvez!une!erreur!dans!un!mécanisme,!un!oubli,!merci!de!me!prévenir!par!
courriel!».!
!
Ce!mécanisme!est!très!fréquent!avec!les!acides!carboxyliques.!
A!partir!de!l’acide,!on!peut!former!des!amides,!des!acides!aminés,!des!chlorures!
d’acide,!etc..!
Cas!d’un!chlorure!d’acide!:!
!
!
Le!mécanisme!débute!par!la!formation!d’une!molécule!de!HCl!:!
!
!
!
@ -:;6.27:8)4N.8GK4;745)
!
2!molécules!d’acide!carboxylique!réagissent!l’un!sur!l’autre!pour!former!un!
anhydride!d’acide!et!le!départ!du!nucléofuge!(H2O).!
)
!
!
O
C OH
R
+
Cl
S
Cl
O
O
C Cl
R
+SO2 + HCl
Chlorure d'acide
Chlorure de thionyle
O
C O
R
H
+
Cl
S
Cl
O
1
2
3
4
O
C
RO
S
O
Cl
O
C
Cl
R
+
SO2
+ HCl
1
23
O
C
ROH
+
O
C
ROH
P2O5
Chaleur
O
RO
O
R
+H2O
Le mécanisme est toujours addition nucléophile suivi d'un départ nucléofuge
Ici le nucléofuge est l'eau
Le nucléofuge est le groupe partant.
 6
6
 7
7
 8
8
 9
9
1
/
9
100%