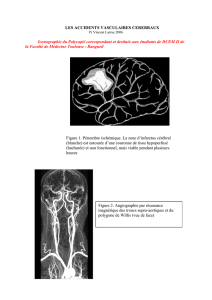
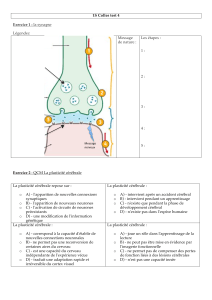
Les termes anatomiques employés dans ce document sont ceux

Dr. C. TESSIER SAR Beaujon 2007/2008 1
MODULE DE NEURO-RÉANIMATION
A – RAPPELS D'ANATOMIE – MISE EN PLACE DU SYSTÈME
NERVEUX
Les termes anatomiques employés dans ce document sont ceux utilisés en pratique
clinique quotidienne, c’est-à-dire ceux de l’ancienne nomenclature d’anatomie.
- Le système nerveux est subdivisé en 3 parties :
Système nerveux
central
Système nerveux
périphérique
Système nerveux
végétatif
Encéphale
- cerveau
- tronc cérébral
- cervelet
Moelle épinière
Nerfs
crâniens
Nerfs rachidiens
périphériques
Système
sympathique
Système
parasympathique
• le système nerveux central (SNC)
• le système nerveux périphérique (SNP)
• le système nerveux autonome (SNA)
- Le système nerveux central comprend 2 parties :
• un segment supérieur qui occupe la boîte crânienne : l’encéphale subdivisé en
3 parties : . le cerveau,
. le tronc cérébral et
. le cervelet.
• un segment inférieur contenu dans le canal rachidien : la moelle épinière.
- L'espace intra crânien se compose de 3 compartiments :
• le parenchyme cérébral : 80 %
Il est composé du : secteur interstitiel extracellulaire
et du secteur intracellulaire
• le liquide céphalorachidien (LCR) : 15 %
Il est distribué à : 75 % dans le système ventriculaire
et à 25 % dans l'espace sous-arachnoïdien
• le volume sanguin cérébral (VSC) : 5 %
1°) Ostéologie
a) Le crâne
Os oc
c
Cond
u
extern
e
Masto
ï
Styloï
d
Crâne osseux de profil
La surface endocrânienne de la voûte est concave, on y distingue 3
dépressions :
- l’étage antérieur ou ethmoïdo-frontal limité en avant par la portion
verticale du frontal, et en arrière par le bord postérieur de la petite aile du
sphénoïde

Dr. C. TESSIER SAR Beaujon 2007/2008 2
- l’étage moyen ou sphéno-temporal compris entre la limite postérieure de
l’étage antérieur en avant et la lame quadrilatère du sphénoïde et le bord
supérieur du rocher en arrière
- l‘étage postérieur ou occipito-temporal compris entre la limite postérieure de
l’étage moyen en avant et les gouttières des sinus latéraux en arrière.

Dr. C. TESSIER SAR Beaujon 2007/2008 3
b) Le rachis
- La colonne vertébrale est formée de : • 7 vertèbres cervicales,
• 12 vertèbres dorsales,
• 5 vertèbres lombaires,
• 5 vertèbres sacrées soudées et
• 4 vertèbres coccygiennes mobiles.
- Elles sont articulées les unes avec les autres par l’intermédiaire :
• de facettes articulaires,
• des disques intervertébraux et
• de ligaments
r
e
tal
v
erse
lame
n
euse
Vue postéro-supérieure des vertèbres cervicales supérieures

Dr. C. TESSIER SAR Beaujon 2007/2008 4
Vertèbre lombaire
2°) Architecture macroscopique du système nerveux central
a) L’architecture de l’encéphale
La surface de chaque hémisphère est creusée de sillons qui permettent de limiter
des circonvolutions et de scissures qui individualisent des lobes.
- Les lobes : quatre principaux
• Le lobe frontal • Le lobe temporal
• Le lobe pariétal • Le lobe occipital
et deux plus petits : • L’insula invaginée au fond de la vallée sylvienne et
• Le rhinencéphale situé au-dessus du lobe temporal.
- Les scissures :
• La scissure inter hémisphérique est la plus profonde, elle sépare les 2
hémisphères cérébraux, d’où son nom.
• La scissure de Rolando sépare les lobes frontal en avant et pariétal en
arrière.
• La scissure de Sylvius sépare les lobes frontal et pariétal en haut du lobe
temporal en bas.
• La scissure pariéto-occipitale limite le lobe occipital en arrière, du lobe
pariétal en avant.
Vue latérale de l'encéphale
(
Avant
Arrière

Dr. C. TESSIER SAR Beaujon 2007/2008 5
a
l
x
l
e
l
e
e
u
s
a
l
cérébral
u
bérance
a
nnulaire
Bulbe
Scissure
de
Rolando
L
o
o
c
Gande
c
Atlas
Odontoïde
Lobe pari
é
Sinus lon
g
supérieur
Epiphyse
Tente du
cervelet
Aqueduc
de Sylvius
Torcular
Cervelet
IVe ventricule
Sinus droit
Coupe sagittale du crâne - rapports de l’encéphale et du crâne
Avant
Scissure interhémisphérique
Corp
s
V
e
V
p
s
u
x
u
Pallidum
Putamen
Coupe horizontale du cerveau : les noyaux gris centraux
- Les nerfs crâniens prennent leur origine ou se terminent dans l'encéphale.
A l’exception des nerfs olfactif et optique, ils prennent tous naissance
dans chaque côté du tronc cérébral. Ils émergent de la boîte crânienne par
les trous de la base du crâne du côté correspondant à leur site de
naissance. On décrit donc 12 paires de nerfs crâniens qui sont numérotés
d'avant en arrière et de haut en bas d'après leur ordre d'émergence à la
surface de l'encéphale et leur ordre de sortie de la cavité crânienne. Ils
sont souvent représentés par leur numéro en chiffre romain. Ils assurent
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
 70
70
 71
71
 72
72
 73
73
 74
74
 75
75
 76
76
 77
77
 78
78
 79
79
1
/
79
100%