Surveillance clinique des antiarythmiques en soins

SURVEILLANCE CLINIQUE DES ANTIARYTHMIQUES
EN SOINS CRITIQUES
Jean-Luc Beaumont, infirmier — clinicien spécialisé en soins infirmiers
cardiovasculaires et respiratoires
Les antiarythmiques constituent, en milieu clinique, une classe importante de la pharmacologie
cardiologique. Le but de cet article vise notamment la compréhension des mécanismes d’action des
antiarythmiques et, conséquemment, la surveillance clinique reliée aux effets attendus de ceux-ci.
L’article est présenté en deux parties; la première intitulée l’électrophysiologie explique le lien entre le
potentiel d’action de la fibre myocardique et le point d’impact des antiarythmiques. La seconde partie,
les antiarythmiques, aborde la classification des antiarythmiques, les mécanismes d’action de chacune
de ses classes ainsi que certaines particularités spécifiques à chacune d’elle, dont la surveillance
clinique.
PREMIÈRE PARTIE : L’ÉLECTROPHYSIOLOGIE
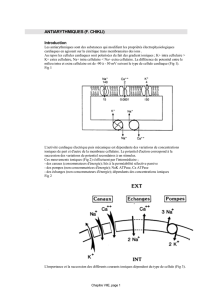
Dans le myocarde siège un système spécifique de fibres spécialisées différentes des fibres contractiles.
Ces fibres forment le tissu nodal et sont dotées de deux types de populations cellulaires. Certaines
cellules dites automatiques, sont génératrices des impulsions cardiaques (automaticité) alors que
d'autres, dites conductrices propagent les influx de proche en proche à travers le système de conduction
(conductibilité). L’ensemble de ces cellules réagit à une stimulation (excitabilité). Ces trois propriétés
constituent le noyau du système nerveux intrinsèque du cœur. De plus, certaines fibres afférentes dites
sensitives connectées au système de conduction électrique du cœur influencent l’électrophysiologie
cardiaque. En effet, le système sympathique sous l’influence de l’adrénaline et le parasympathique
activé par l’acétylcholine constituent le système nerveux extrinsèque et permettent de moduler le
fonctionnement du cœur.
L’activité électrique du cœur est générée par de fortes concentrations ioniques réparties de part et
d’autre de la membrane cellulaire. Une perturbation importante des transferts ioniques
transmembranaires est précurseur d’arythmies cardiaques. L’activité de travail et de repos de la cellule
appelée, potentiel électrique, s’enregistre à l’aide de micro-électrodes placées de part et d’autre de la
1

membrane cellulaire. Le potentiel électrique engendre une image caractéristique appelée potentiel
d’action (Fig. 1).
Figure 1 : Phases du potentiel d’action et mouvements ioniques transmembranaires
Beaumont, J-L (2006)
Classe I
Classe
IV
Classe
III
Classe II
Le potentiel d’action se subdivise en cinq phases (Fig. 1).
La première phase, « phase 0 » correspond à l’activation cellulaire ou dépolarisation.
L’impulsion se propage aux cellules avoisinantes grâce à l’avalanche d’ions sodium (Na+) qui
pénètrent dans la cellule et favorisent l’automaticité. Ces ions circulent rapidement le long de
fibres dites à réponse rapide au Na+ par des canaux spécifiques. Ce type de fibres à courant
sodique active principalement le fonctionnement des oreillettes, le système His-Purkinje et les
fibres du muscle ventriculaire (Fig. 2). Les médicaments susceptibles d’inhiber les entrées de
Na+ (phase 0) dans la cellule constituent la classe 1 des antiarythmiques appelés bloquants des
canaux sodiques (Tableau 1). La « phase 0 » correspond au complexe QRS sur l’ÉCG de
surface (Fig. 3).
2

Les deuxième et troisième phases, « phases 1 et 2 » du potentiel d’action correspondent à la
repolarisation initiale de la cellule. L’inactivation sodique fait place aux entrées de calcium dans
la cellule. Au cours de ces phases, la vitesse de repolarisation est diminuée, car les sorties
intracellulaires de potassium cheminent vers l’extérieur de la cellule. Ce courant calcique
influence particulièrement le fonctionnement des fibres à réponse lente localisées au noeud
sinusal et au nœud auriculoventriculaire (Fig. 2). Lors de tachycardies supraventriculaires, les
bloquants calciques sont des indications de choix, puisque ces arythmies naissent au pourtour
de fibres dont le potentiel d’action à caractère calcique influence fortement la fréquence
cardiaque pour le nœud sinusal et la conduction auriculoventriculaire (AV) pour le nœud AV.
Les médicaments capables d’inhiber les entrées de Ca+ dans la cellule constituent la classe 4
des antiarythmiques, les bloquants des canaux calciques (Tableau 1). Les phases 1 et 2 du
potentiel correspondent au segment ST sur l’ÉCG de surface (Fig. 3).
La quatrième phase, « phase 3 » du potentiel d’action correspond à la repolarisation terminale
de la cellule. Cette phase résulte d’un courant sortant de potassium (K+) qui augmente la durée
du potentiel d’action. À ce stade, la fibre retrouve ses charges initiales de repos. Cette phase
correspond à l’onde T sur l’ÉCG de surface (Fig. 3). Certaines conditions nécessitent parfois le
contrôle des sorties de potassium intracellulaire ce qui a pour effet d’augmenter la durée du
potentiel d’action et conséquemment l’intervalle QT sur l’ÉCG de surface (Fig. 3). Les
médicaments qui atténuent les sorties du « K+ » dans la cellule constituent la classe 3 des
antiarythmiques appelés les bloquants potassiques (Tableau 1).
La cinquième phase, « phase 4 » du potentiel d’action représente l’intervalle de temps entre
deux potentiels d’action. À ce stade, la cellule a récupéré son potentiel de repos ou potentiel de
membrane étroitement lié au rôle du sodium et du potassium. Des enzymes concourent à fournir
à la cellule l’énergie nécessaire aux échanges ioniques. Schématiquement un battement
cardiaque peut être superposé à un potentiel d’action. La phase 4 du potentiel d’action
détermine la fréquence cardiaque. Plus la phase 4 d’un potentiel d’action est brève, plus il y
aura de potentiels d’action dans une minute et plus grand sera le nombre de battements
cardiaques par minute. En comparant les potentiels d’action des centres d’automatismes du
cœur (nœud sinusal, faisceau de His et le réseau de Purkinje), la phase 4 du noeud sinusal
étant la plus courte, cela explique la dominance du nœud sinusal, d’où l’expression « rythme
sinusal ». Cette phase 4 correspond à la fin de l’onde T et le début du complexe QRS sur l’ÉCG
3

de surface (Fig. 3). Les systèmes sympathique–parasympathique interfèrent directement sur la
fréquence cardiaque et la conduction AV. Les médicaments agissant sur la phase 4 du potentiel
d’action constituent la classe 2 des antiarythmiques désignés bloquants des récepteurs bêta-
adrénergiques ou bêta-bloquants (tableau 1).
Figure 2 : Système de conduction électrique du
coeur
Figure 3 : Corrélation entre les mouvements
ioniques transmembranaires, le
potentiel d’action et l’ECG de
surface
4

DEUXIÈME PARTIE : LES ANTIARYTHMIQUES
Les antiarythmiques agissent sur l’une ou l’autre des phases du potentiel d’action en modifiant la
perméabilité de la membrane myocardique aux ions sodium, calcium et potassium. Ils sont répartis en
quatre classes selon la classification de Vaughan Williams (tableau 1). Bien que la digitale et
l’adénosine aient des propriétés antiarythmiques, elles feront l’objet d’une présentation
complémentaire.
Classe 1 : bloquants des canaux sodiques
Les fibres à « courant sodique » activent la dépolarisation des fibres auriculaires, du système His-
Purkinje et des fibres ventriculaires. Les substances susceptibles de diminuer la dépolarisation de ces
fibres constituent la clef de cette classe pharmacologique. Les substances courantes de cette classe
sont la procaïnamide (pronestylmd),et la flécaïnide (tambocor md) .
La procaïnamide (pronestylmd) constitue une indication de choix pour le syndrome de préexcitation
symptomatique de type Wolff-Parkinson-White (WPW). Lors de ce syndrome, l’impulsion contourne
la jonction nodohissiene (du nœud de His) pour atteindre les ventricules par des voies anormales dites
accessoires ce qui peut favoriser des arythmies ventriculaires majeures. La procaïnamide ralentit la
dépolarisation et conséquemment la conduction des voies accessoires, ce qui protège les ventricules. La
surveillance clinique pour la voie intraveineuse vise principalement la détection d’une baisse du débit
cardiaque, la prise des signes vitaux, le monitorage des arythmies pour les traitements d'urgence.
L’effet sur la repolarisation cellulaire peut entraîner une augmentation des intervalles du complexe
QRS et de l’intervalle QT. Toute durée du complexe QRS supérieure à 25 % de sa valeur initiale et de
la durée de l’intervalle QT supérieure à 0,44 seconde doivent être rapportées.
La flécaïnide (tambocormd) est l’antiarythmique le plus puissant de cette classe. Ses effets sont
l’allongement du temps de la dépolarisation cellulaire (phase 0) au niveau auriculaire, du réseau de
Purkinje et ventriculaire. Un ralentissement de la conduction intraventriculaire peut être observé. En
l’absence de coronaropathie, la flécaïnide est particulièrement efficace pour le traitement des
extrasystoles ventriculaires (ESV) fréquentes. La surveillance clinique consiste en la prise des signes
vitaux, la détection de l’allongement de l’intervalle QRS à l’ECG et au monitorage des arythmies
5
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%