D`où vient l`énergie fournie par une pile électrochimique ?

Groupe Collège 2009-2010 Académie de Créteil Page 1
D’où vient l’énergie fournie par une pile
électrochimique ?
Je me souviens
On a appris en troisième que le courant électrique est un déplacement concerté d’électrons dans
les conducteurs métalliques ; il est provoqué par une tension électrique, différence d’état entre les
deux bornes de la pile.
Je découvre
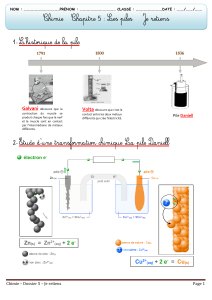
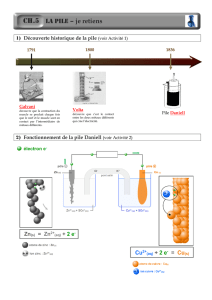
Document 1 : La découverte des piles
Bien que Alessandro Volta soit l'inventeur de la première pile, d'autres chercheurs avant lui l'ont
influencé. Un des chercheurs qui influença le plus Alessandro fut Luigi Galvani, professeur
d'anatomie à l'Université de Bologne. Celui-ci étudiait l'effet de décharge produite par un
générateur sur des grenouilles mortes.
Les expériences de Galvani démontraient que les grenouilles avaient des contractions musculaires
lorsque l'on faisait passer dans le corps de celles-ci un courant électrique produit par une machine
électrostatique. Ensuite, après plusieurs expériences, il découvrit que le générateur n'était qu'un
accessoire pour que les muscles de la grenouille se contractent. Les muscles se contractaient
uniquement au contact de deux morceaux de métal. Ses expériences démontraient aussi que la
grenouille ne réagissait pas de la même façon au contact de tous les métaux. En effet, il remarqua
que la grenouille avait de très légères contractions lorsque l'on utilisait un même métal pour relier
les deux bouts de la grenouille et que ces mêmes contractions étaient nettement plus prononcées
lorsque les métaux étaient différents. Après plusieurs essais, il conclut que les contractions étaient
optimales lorsque la grenouille était reliée par un fil de cuivre et un fil de zinc. Toutes ces
expérimentations l'amenèrent à la conclusion que l'électricité qui faisait bouger la grenouille était
contenue à l'intérieur de celle-ci.
Volta s'intéressa aussitôt aux expériences de Galvani, et il recommença chacune d'elles
exactement comme Galvani les avait faites. Après maintes observations, Volta rejeta les
conclusions émises par Galvani; il démontra que les convulsions de la grenouille n'étaient pas le
produit de l'électricité contenu à l'intérieur de la grenouille mais plutôt le résultat d'une source de
courant extérieur. Il émit donc l'hypothèse que l'électricité était générée par les deux plaques de
métal. Ses plaques doivent alors être mises en contact avec un conducteur humide. Donc les
expériences de Galvani répondaient à l'énoncé de Volta: [deux plaques de métal (zinc et cuivre)
réunies par un liquide conducteur (liquide corporel de la grenouille)].
À partir des résultats obtenus dans ses recherches et celles de Galvani, Volta réalisa la première
pile. Cette pile était composée de rondelles de métal différent, soit du zinc et du cuivre. Entre
chaque superposition de rondelle, il y en avait une imbibée de saumure (H2O+NaCl) pour conduire
le courant. La première pile était née.
Alessandro Volta intéressa le monde entier par la découverte de sa pile. La gloire de cet homme
fut à jamais gravée dans l'histoire de l'électricité.
Document 2 : quelques expériences
On dispose de tournures de cuivre, de grenaille de zinc, d'une solution (incolore) contenant des
ions Zn2+ et d'une solution (bleue) contenant des ions Cu2+. On place du zinc dans la solution
contenant Cu2+ et du cuivre dans la solution contenant Zn2+. Après quelques minutes un morceau
de solide est retiré de la solution bleue pour mieux l'observer, et placé à droite d'un morceau de
zinc (photo 1) :

Groupe Collège 2009-2010 Académie de Créteil Page 2
D'autre part on met dans un tube à essais de la poudre de
zinc et une solution contenant des ions Cu2+, à température
ambiante. Le tube est agité et on mesure la température
(photo 2) ; le thermomètre est retiré et on attend quelques
minutes encore en agitant de temps en temps (photo 3) :
En plaçant une lame de cuivre dans une
solution contenant des ions Cu2+ et une lame
de zinc dans une solution contenant des ions
Zn2+, puis en reliant les deux solutions par un
pont de gel conducteur, une tension électrique
apparaît entre les deux plaques métalliques
(photo 4).
Je réponds aux questions
1°) Comment a-t-on rendu hommage à Volta ?
2°) Pourquoi le dispositif inventé par Volta a-t-il été appelé “pile” ?
3°) Avec les connaissances actuelles sur la tension, pouvait-on prévoir que des métaux différents
étaient nécessaires pour obtenir un courant électrique ?
4°) Que met en évidence la photo 1 ? Comment interpréter la photo 3 ?
5°) Quel phénomène est mis en évidence par la photo 2 ?
6°) Quel est le rôle du pont de gel conducteur de la photo 4 ?
Zn Zn ayant séjourné avec Cu2+ Cu
photo 1
photo 2
photo 3
photo 4

Groupe Collège 2009-2010 Académie de Créteil Page 3
Je vérifie
1°) On a rendu hommage à Volta en choisissant son nom comme base d'une unité électrique : le
volt, unité de la tension électrique.
2°) Volta a fait un empilement de rondelles de métal et de rondelles humides.
Remarque : cet empilement constitue un placement en série des générateurs, leurs tensions
s'additionnent donc.
3°) On sait que la tension provient d'une différence entre les bornes d'une pile, elle est due à la
différence des métaux employés.
4°) La photo 1 montre que le métal cuivre ne réagit pas avec les ions du zinc, alors que le métal
zinc réagit avec les ions Cu2+. La décoloration de la solution en photo 3 montre que les ions
Cu2+ sont consommés.
5°) La solution est chauffée par la réaction qui a lieu dans le tube à essais : la réaction du zinc
avec les ions Cu2+ produit de l'énergie, ici sous forme thermique.
6°) Le gel conducteur permet d'assurer la fermeture du circuit électrique en mettant en "contact"
les solutions ioniques, sans les laisser se mélanger.
Je retiens
Cette partie est à recopier / imprimer sur le cahier / classeur
Une pile électrochimique convertit de l'énergie chimique, provenant d'une réaction, en
énergie électrique.
Elle est constituée de métaux et leurs ions séparés par un pont conducteur.
L'utilisation de la pile entraine la consommation de certains de ces réactifs : quand un des
réactifs est totalement transformé la pile est usée.
Une pile électrochimique peut faire tourner un petit moteur.

Groupe Collège 2009-2010 Académie de Créteil Page 4
Je m’entraîne
1°) Un élève a fait le schéma d'une pile électrochimique alimentant une lampe. Quelles sont les
deux erreurs dans son schéma ? Les corriger.
2°) On trouve parfois le schéma d'une pile "en un seul pot" :
a) Quel rôle joue le becher en
céramique poreuse ?
b) Quelle critique peut-on faire de
la pile schématisée ci-contre ?
solution contenant
des ions Cu2+
solution contenant
des ions Zn2+
lame de cuivre
lame de zinc
solution contenant
des ions Cu2+
solution contenant
des ions Zn2+
lame de cuivre
lame de zinc
céramique
poreuse
solution contenant
des ions Cu2+
lame de cuivre
lame de zinc

Groupe Collège 2009-2010 Académie de Créteil Page 5
Correction :
1°) Les deux lames métalliques ont été inversées (ou les solutions), on observera simplement une
réaction dans le becher de gauche. De plus il manque le pont ionique entre les deux bechers.
2°) a) Le becher en céramique poreuse joue le rôle du pont ionique : il permet un échange électro-
chimique entre les deux solutions (passage d'ions) sans leur permettre de se mélanger.
b) Cette pile va s'user quand on ne s'en sert pas ! En effet la lame de zinc étant en contact direct
avec les ions Cu2+, elle va réagir et sera consommée, comme les ions cuivre, sans que la pile ne
débite.
Remarque : Cette pile peut fonctionner quelque temps si on n'agite pas la solution, la lame de zinc
s'entourant d'une couche où les ions de cuivre ne sont pas présents, mais la diffusion entraine
rapidement son usure. Elle ne correspond en aucun cas au principe des piles couramment
utilisées.
solution contenant
des ions Cu2+
solution contenant
des ions Zn2+
lame de cuivre
lame de zinc
pont ionique
1
/
5
100%