La pile, une source d`énergie - images.hachette

CHAPITRE 6•La pile, une source d’énergie 11
Programme officiel
De nombreux appareils courants (lampes de poche,
télécommandes, calculatrices, petits appareils
domestiques tels que rasoirs, appareils photogra-
phiques,téléphones portables, outils de bricolage…)
fonctionnent avec des piles électrochimiques ou des
accumulateurs.
Quelques notions d’énergie chimique sont donc pro-
posées à ce niveau d’enseignement en se limitant
aux piles électrochimiques.
Approche de l’énergie chimique:
une pile électrochimique
Comment une pile peut-elle être une source
d’énergie?
Connaissances
•Les espèces chimiques présentes dans une pile
contiennent de l’énergie chimique, dont une partie
est transférée sous d’autres formes d’énergie
lorsqu’elle fonctionne.
•L’énergie mise en jeu dans une pile provient d’une
réaction chimique : la consommation de réactifs
entraîne l’usure de la pile.
Capacités
•Réaliser, décrire et schématiser la réaction entre
une solution aqueuse de sulfate de cuivre et de la
poudre de zinc.
•Interpréter l’échauffement du milieu réactionnel
comme le résultat de la conversion d’une partie de
l’énergie chimique en énergie thermique.
Commentaires
La réaction chimique entre une solution de sulfate de
cuivre et de la poudre de zinc, par exemple, est l’occasion
d’un transfert d’énergie sous forme d’énergie thermique
vers le milieu extérieur. Dans une pile électrochimique,
l’énergie rendue disponible par la transformation chimi-
que est principalement transférée sous forme d’énergie
électrique vers les autres composants du circuit. À noter
que la pile va « s’user », ce qui la différencie d’une pile à
Chapitre 6
La pile, une source d’énergie
combustible alimentée en continu en réactifs.
La réalisation de la pile est l’occasion de montrer l’appa-
rition d’une tension aux bornes des deux lames, capable
d’alimenter un dipôle adapté. La notion de couple oxydo-
réducteur est hors programme.
Objectifs de la leçon
Les objectifs sont clairement énoncés dans les pages
d’ouverture du chapitre ; ils annoncent les compétences
théoriques et expérimentales visées dans le chapitre.
•Savoir qu’une tension apparaît entre deux lames
plongées dans un électrolyte.
•Réaliser, décrire et schématiser la réaction chi-
mique entre une solution aqueuse de sulfate de
cuivre et du zinc.
•Savoir que l’énergie électrique produite par une
pile provient d’une réaction chimique.
•Interpréter l’échauffement du milieu réactionnel
comme le résultat de la conversion d’une partie
de l’énergie chimique des réactifs en énergie ther-
mique.
•Interpréter l’usure de la pile comme la disparition
des réactifs qu’elle contient.
Activités
1. Comment réaliser une pile
expérimentale?
Cette première activité présente la réalisation de la
plus simple des piles électrochimiques : deux métaux
différents plongés dans une solution conductrice.On
choisit l’eau salée comme électrolyte car l’élève sait
déjà que cette solution est conductrice (chapitre 3).
En mesurant la tension aux bornes de cette pile élé-
mentaire, l’élève prend immédiatement conscience
de l’origine chimique de l’énergie électrique fournie
par ce générateur.
Le montage en série de trois piles permet de cons-
tater le passage du courant dans la diode et démontre
ainsi l’intérêt d’associer les piles.
Prof_PhysiqueChimie.qxd 10/06/08 17:38 Page 11

2. Comment est constituée une pile
du commerce?
Les notions d’électrodes et d’électrolyte étant
établies à l’activité 1, cette activité, documentaire,
permet de faire le parallèle entre pile expérimentale
et pile ronde du commerce. On montre ici les simili-
tudes existantes et les éléments communs à toutes
les piles, c’est-à-dire les deux électrodes et l’élec-
trolyte.
3. Que devient l’électrode en zinc
quand la pile fonctionne?
L’interprétation des deux photographies est immé-
diate : l’élève associe le phénomène d’usure de la
pile, à la disparition de l’électrode en zinc.
Remarque : si l’on souhaite présenter en classe ces
deux piles, il est conseillé de choisir un modèle dont
l’emballage protecteur est en matière plastique
« collée » il s’agit la plupart du temps de pile très bon
marché.
4. Le métal zinc réagit-il avec
une solution de sulfate de cuivre?
L’activité 4 permet de mettre en avant le concept de
transformation chimique se produisant entre le zinc
(dont la présence dans les piles est montrée aux acti-
vités 2 et 3) et un électrolyte (notion rencontrée dans
l’activité 1). L’effet visuel (décoloration de la solution
de sulfate de cuivre et dépôt du cuivre) est rapide
(avec une solution moyennement concentrée).
L’apparition d’un précipité blanc lors de l’ajout de
soude dans la solution finale incolore permet aussi
une conclusion aisée quant à la présence des ions
zinc. L’élève retient alors que, dans une pile, l’élec-
trode et l’électrolyte réagissent.
5. Comment modéliser l’action
du métal zinc sur les ions cuivre?
L’élève sait (chapitre 2) que le courant électrique est
dû à un déplacement d’électrons. Il a constaté dans
l’activité précédente que le zinc réagit avec les ions
cuivre. Il s’agit ici de mettre en relation, de manière
simple, ces deux connaissances pour expliquer com-
ment la réaction chimique peut produire du courant
électrique.
Remarque : on rappelle que la notion de couple
oxydo-réducteur est hors programme.
6. La réaction du zinc avec les ions
cuivre produit-elle de l’énergie?
En plaçant une lame de zinc dans une solution de
sulfate de cuivre, on constate une élévation de tem-
pérature ; parallèlement la solution se décolore et le
zinc se recouvre de cuivre. La transformation chi-
mique produit donc de l’énergie thermique.
Cette conclusion, associée à celle de l’activité pré-
cédente permet de satisfaire une recommandation
du programme : montrer que dans une pile, l’énergie
chimique est transférée sous forme d’énergie élec-
trique et d’énergie chimique.
Documents
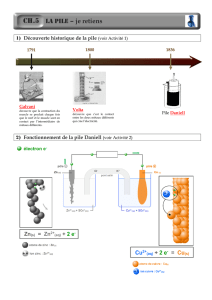
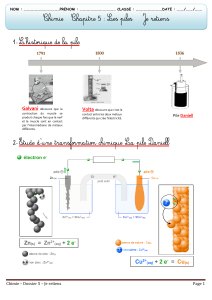
1. Les différentes sortes de piles
Les piles sont des générateurs d’usage courant. Dans
la première partie du document, l’élève découvre la
diversité des piles.Bien connaître les caractéristiques
de chacune permet de les utiliser à bon escient.Dans
une deuxième partie, le principe des accumulateurs,
appelés de manière erronée « piles rechargeables »,
est présenté.
Réponses aux questions
1. Les piles au lithium ont la particularité de pouvoir
maintenir une tension proche de leur tension nomi-
nale pendant un temps plus long (comparé aux piles
alcalines et salines). Elles permettent ainsi de faire
fonctionner plus longtemps des appareils perfec-
tionnés (ce qui peut justifier un coût supérieur).
2. On juge souvent, à tort, qu’une pile est usée
lorsqu’elle ne permet plus le fonctionnement de l’ap-
pareil qu’elle alimente. Mais certains appareils ces-
sent de fonctionner dès que la tension délivrée par
les piles qui les alimentent descend en dessous d’un
seuil, encore proche de leur tension nominale.
D’autres appareils,nécessitant une tension d’alimen-
tation moins élevée, pourraient encore fonctionner
un long moment avec ces piles « usées »!
3. Lorsqu’une pile usée cesse de fonctionner, ses
réactifs ont disparu et elle ne peut pas être « rechar-
gée ». L’appellation « rechargeable » est donc im-
propre,seuls les accumulateurs peuvent se recharger.
4. Un accumulateur fonctionne comme un généra-
teur lorsqu’il alimente un appareil. Mais, lorsqu’on le
recharge sur le secteur (par l’intermédiaire d’un
adaptateur), il se comporte comme un récepteur. On
peut donc parler de fonctionnement « réversible ».
PARTIE 1•La chimie, science de la transformation de la matière
12
Prof_PhysiqueChimie.qxd 10/06/08 17:38 Page 12

CHAPITRE 6•La pile, une source d’énergie 13
pratiques, leur coût est assez élevé; la construction
d’une « pile » avec des lames de zinc et de cuivre,
bien que moins esthétique et moins pratique,
conduira aux mêmes conclusions.
Correction des exercices
Les exercices 2 et 3 font uniquement appel aux
connaissances et capacités du socle commun.
Je contrôle mes connaissances
Je retrouve l’essentiel
On constitue une pile avec deux matériaux conduc-
teurs différents (électrodes) plongeant dans une
solution conductrice (électrolyte). Lors du fonction-
nement de la pile, le métal zinc subit une transfor-
mation chimique : les atomes donnent des ions
zinc. Les électrons libérés par cette transformation
circulent, à l’extérieur de la pile,vers l’autre électrode
et créent ainsi le courant électrique. La consom-
mation des réactifs entraîne l’usure de la pile. Une
pile convertit l’énergie chimique des réactifs en
énergie thermique et en énergie électrique.Ces
réaction
.
Comparer pile neuve et pile usagée
a. L’enveloppe d’une pile neuve est en zinc.
b. On constate que l’enveloppe de la pile usagée est
détériorée, une partie du métal zinc a été consom-
mée.
c. Quand la pile fonctionne,le zinc qui constitue son
enveloppe extérieure disparaît. Le fonctionnement
de la pile est donc bien associé à une transformation
chimique dont le zinc est l’un des réactifs.
Interpréter des observations
a. Les ions cuivre sont mis en évidence par l’appa-
rition du précipité bleu lors de l’ajout de soude.
Les ions cuivre ne sont plus présents dans la solution
3
2
Générateur
électrochimi
q
ue
Énergie thermique
Énergie électrique
Énergie chimique
1
5. Les piles usagées contiennent des composants
toxiques (métaux lourds…) et nocifs pour l’environ-
nement. Il est indispensable de s’en débarrasser en
les déposant dans un collecteur spécialement prévu
à cet effet. Elles pourront ensuite être retraitées et
recyclées.
2. Des piles que l’on ne remplace pas
Le dihydrogène est de plus en plus présenté par les
médias comme une « nouvelle » source d’énergie,
non polluante, alternative au pétrole. Ce document
présente le principe de fonctionnement de la pile à
dihydrogène. Il permettra aux élèves de prendre
conscience de l’intérêt de la pile à combustible et
d’en connaître également les limites.
Réponses aux questions
1. Les réactifs qui permettent le fonctionnement de
la pile à combustible sont le dioxygène et le dihydro-
gène. Le seul produit est l’eau.
2. La pile à dihydrogène n’a pas besoin d’être rem-
placée,car elle peut être alimentée continuellement
en dihydrogène et en dioxygène. Les réactifs de la
réaction chimique dont elle est le siège (et qui per-
met la production d’énergie électrique) sont donc
renouvelés en permanence.
3. Le seul produit résiduel de la pile à dihydrogène
est l’eau; on peut donc la qualifier de « propre ».
Capacité expérimentale
et démarche d’investigation
La réalisation de la pile est l’occasion
de montrer l’apparition d’une tension
aux bornes de deux lames.
La démarche d’investigation proposée s’appuie sur
l’interprétation d’un texte historique. Sa lecture sera
l’occasion de découvrir le personnage d’Alessandro
Volta et de comprendre comment la première pile a
été fabriquée (les élèves comprendront ainsi l’origine
du nom « pile »).
L’élève devra ensuite réfléchir au moyen de recon-
stituer la pile de Volta et d’en mesurer la tension.
Une réflexion quant à l’intérêt d’associer plusieurs
couples de métaux lui est demandée à la fin de l’étude.
Remarque : On trouve chez les fournisseurs habituels
de matériel pédagogique des dispositifs permettant
de reconstruire la « pile de Volta ». L’un d’eux est
photographié page 98 (manuel élève). Bien que très
Prof_PhysiqueChimie.qxd 10/06/08 17:38 Page 13
énergies trouvent leur origine dans une
chimique

(fig. 2) car celle-ci est incolore.
b. Les ions cuivre (responsables de la coloration
bleue) disparaissent (la solution se décolore). Ils se
transforment en métal cuivre et se déposent sur la
lame de zinc.
Modéliser une réaction chimique
a. Les espèces chimiques présentent à l’état initial
sont les ions cuivre et les atomes de zinc. À l’état
final, on trouve des ions zinc et des atomes de cuivre.
b. Un ion cuivre se transforme en atome de cuivre en
captant deux électrons. Un atome de zinc se trans-
forme en ion zinc en cédant deux électrons.
Comprendre le fonctionnement
d’une pile
a. Lors du fonctionnement de la pile, les atomes de
zinc se transforment en ions zinc,ce qui se traduit par
une disparition du métal zinc (et une usure de la pile).
b. Les électrons sont produits par l’électrode en zinc
au cours de la transformation chimique du métal
zinc en ions zinc.
c. Sens des électrons et sens conventionnel du
courant sont opposés.
J’utilise mes connaissances
Les exercices 8 et 11 font uniquement appel aux
connaissances et capacités du socle commun.
Monter des piles en série
Marianne constate qu’aux bornes d’une pile, la
tension est de 0,82 V. Lorsqu’elle associe trois piles,
elle mesure 2,44 V, soit approximativement trois fois
la tension entre les bornes d’une pile seule. Associer
plusieurs piles en série permet de disposer d’une
tension plus importante.
6
Électrode
en zinc
Sens de déplacement
des électrons
Sens conventionnel
du courant
Zn Zn2+ +
+
–
5
4
Construire un raisonnement
Je sais que la tension aux bornes d’une pile ronde
neuve vaut 1,5 V.
J’observe que la pile plate est constituée de trois piles
rondes.
J’en conclus que la tension aux bornes de la pile plate
vaut 3 x 1,5 V soit 4,5 V.
Choisir la bonne représentation
L’ordre chronologique des schémas est ➂,➀et ➁.
En effet, lors de cette expérience, la quantité de
cuivre qui se dépose sur la lame augmente et la colo-
ration de la solution s’atténue.
Prévoir un résultat d’expérience
a. Le filtrat est incolore car les ions cuivre ont
disparu.
b. Si on ajoute de la soude dans le bécher, un
précipité blanc va apparaître.
c. Le précipité blanc obtenu lors de l’ajout de soude
caractérise la présence d’ions zinc.
Modéliser
a. La bonne modélisation des produits de la réaction
est celle de Sofiane. En effet, l’ion cuivre et l’atome
de zinc, modélisant les réactifs, se transforment
respectivement en atome de cuivre et en ion zinc.
b. Erreurs commises par les autres élèves: la repré-
sentation de Karen ne fait pas apparaître de nou-
veaux produits. Camille a représenté un ion Fer II,
mais l’élément fer n’existe pas dans les réactifs.
Transférer l’énergie
a. On peut voir que le courant délivré est très intense
car il fait rougir le fil en métal qui court-circuite la pile.
b. Quand la pile débite un courant très intense, la
réaction chimique qui le produit s’accélère et
l’échauffement associé augmente : la pile s’échauffe
d’autant plus que le courant débité est intense.
c.
Énergie
thermique
Énergie
électrique
Énergie
chimique
11
10
9
8
7
PARTIE 1•La chimie, science de la transformation de la matière
14
DÉMARCHE
SCIENTIFIQUE
Prof_PhysiqueChimie.qxd 10/06/08 17:38 Page 14

CHAPITRE 6•La pile, une source d’énergie 15
J’approfondis mes connaissances
Associer plusieurs piles
a.
b. Associer plusieurs piles rondes en série permet de
disposer d’une tension plus importante aux bornes
de l’ensemble (les tensions s’additionnent).
c. La pile photographiée est constituée de 6 piles
rondes : la tension aux bornes de l’ensemble vaut
6 x 1,5 = 9 V.
De l’énergie en bouteille !
a. La borne positive de la pile de Grenet est consti-
tuée par deux plaques de charbon, la borne négative
est constituée d’un cylindre en zinc.
b. L’électrolyte utilisé est une solution de dichromate
de potassium acidifié.
c. Sortir l’électrode en zinc de l’électrolyte empêche
la transformation chimique d’avoir lieu et limite par
conséquent l’usure de la pile.
Traduire un texte par un schéma
a. La borne positive est la lame de cuivre ; la borne
négative est la lame d’aluminium.L’électrolyte utilisé
est une solution d’eau salée.
b.
Décrire une pile expérimentale
a. Lorsque la diode est connectée aux bornes de
l’ensemble, elle s’allume. Le dispositif expérimental
(citrons et lames de zinc et de cuivre) produit donc
une tension capable de faire briller la diode : il s’agit
d’une pile.
15
Sens de
déplacement
des électrons
Sens
conventionnel
du courant
Lame
de cuivre
Lame
d’aluminium
–+
Eau salée
V
14
13
–+
12
b. Les deux métaux constituant les électrodes sont le
cuivre et le zinc.
c. L’électrolyte est constitué par le jus de citron.
Pour aller plus loin
a. La coloration bleue prise progressivement par la
solution traduit l’apparition d’ions cuivre.
b. Les ions cuivre peuvent être mis en évidence en
ajoutant de la soude dans la solution: un précipité
bleu caractéristique apparaît.
c. Au cours de l’expérience, les atomes du métal
cuivre se transforment en ions cuivre.
d. Le dépôt gris est constitué de métal argent.
e. Le bilan de cette réaction est :
ion argent + atome de cuivre atome d’argent
+ ion cuivre
Chemistry in English
Traduction de l’énoncé
On a placé une lame de zinc dans une solution de sul-
fate de cuivre.
a. Quelle était la couleur initiale de la solution?
b. Pourquoi la couleur de la solution disparaît-elle
progressivement?
Réponse en français
a. Initialement la solution était bleue.
b. La couleur de la solution disparaît progressivement
car les ions cuivre se transforment en métal cuivre.
Réponse en anglais
a. The solution was initially blue.
b. The colour of the solution disappeared gradually
because the copper ions were transformed into
metallic copper.
Exercices supplémentaires
Recycler les piles
Énoncé
Suivant leurs caractéristiques, les piles contiennent
différents métaux : zinc, plomb, nickel, lithium… Si
les piles usagées sont rejetées dans la nature, tous
ces métaux peuvent se répandre dans les sols, les
cours d’eau, les nappes phréatiques…
Par ailleurs, certains de ces métaux pourraient être
recyclés. Depuis 1999, la loi impose de rapporter les
piles dans des lieux où elles sont collectées.
a. Pourquoi ne doit-on pas jeter les piles usagées à la
poubelle?
b. Quel autre avantage présente la collecte des
piles?
18
17
16
Prof_PhysiqueChimie.qxd 10/06/08 17:38 Page 15
 6
6
 7
7
1
/
7
100%