I. La comète de Halley ( points)

17/04/2017 769788367 1/10
Le 20/02/2013
Page : 1 / 10
DEVOIR COMMUN N°2 (3h30min)
Tale S
CALCULATRICE AUTORISEE
Durée : 3h30min
Les portables seront éteints et placés dans le sac (ou cartable)
Le sac sera déposé aux extrémités de la salle
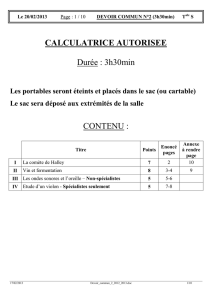
CONTENU :
Titre
Points
Enoncé
pages
Annexe
à rendre
page
I
La comète de Halley
7
2
10
II
Vin et fermentation
8
3-4
9
III
Les ondes sonores et l’oreille – Non-spécialistes
5
5-6
IV
Etude d’un violon - Spécialistes seulement
5
7-8

17/04/2017 769788367 2/10
doc.1 La comète de Halley, photographiée le
8 mars 1986 sur l'Ile de Pâques.
I. La comète de Halley ( points)
Découverte de la comète de Halley
"Comètes que l’on craint à l’égal du tonnerre,
Cessez d’épouvanter les peuples de la Terre,
Dans une ellipse immense achevez votre cours,
Remontez, descendez près de l’astre des jours,
Lancez vos feux, volez, et revenant sans cesse,
Des mondes épuisés ranimez la vieillesse." Voltaire (1694-1778)
Ecrits en 1738 par Voltaire à son amie la marquise du Châtelet, ce
poème illustre d’une façon remarquable une révolution capitale dans l’histoire de la compréhension des comètes
par l’humanité. Jusque-là, ces astres au cours apparemment erratique, à l’apparition imprévisible, à l’aspect
spectaculaire et rapidement changeant, étaient considérés avec crainte et superstition comme des présages
néfastes et annonciateurs de grandes catastrophes. Mais au XVIIème siècle, on comprenait enfin, grâce
notamment aux travaux de Johannes Kepler, d’Isaac Newton et d’Edmund Halley que le mouvement
apparemment étrange des comètes sur la voûte céleste obéit en fait aux mêmes lois que le mouvement des
planètes. Dans le cas des comètes, l’ellipse est simplement beaucoup plus allongée (plus excentrique) que celles
qui sont parcourues par les planètes.
Selon des annales chinoises, les premières observations de la comète de Halley datent de 240 av. J.C. En 1682,
Edmund Halley (1656 - 1743), alors âgé de 26 ans, aidé par Isaac Newton, prédit le retour de cette comète pour
1759. La comète fut au rendez-vous, vérifiant ainsi les lois de Kepler.
Durant l’été 1911, la Terre traversa la queue de poussière et de gaz de la comète provoquant une grande
inquiétude populaire allant même jusqu’aux grandes prédictions de fin du monde apocalyptique propres à toute
fin proche d’un millénaire. On avait en effet détecté par spectroscopie la présence dans l’atmosphère de la
comète d’un gaz très toxique, le cyanogène CN, et des escrocs en profitèrent pour vendre des pilules
« anticomète » …
Etude du mouvement de la comète
1. Analyse du texte (Analyser)
1.1. D’après le poème de Voltaire, quelle est la trajectoire d’une comète ?
1.2. Que signifie l’alexandrin "Remontez, descendez près de l’astre des jours" ?
1.3. Ces deux réponses sont-elles en accord avec la première loi de Kepler ? Justifier.
2. Analyse du mouvement (S’approprier)
Le document en annexe, page 10, représente la chronophotographie de la comète de Halley.
2.1. Sur le document en annexe page 10, utiliser les données pour placer précisément la position du Soleil.
2.2. Justifier qualitativement que le mouvement de la comète autour du Soleil respecte la deuxième loi de Kepler.
2.3. Déterminer la valeur de la vitesse (en km.s-1) de la comète en 1988 ainsi que celle en 1990.
2.4. Construire page 10, avec soin, le vecteur accélération
Error!
en 1989. Que remarque-t-on ?
2.5. Parmi les trois relations ci-dessous, quelle est l’expression correcte du vecteur
Error!
de la comète ?
Justifier.
Données : Dans le repère de Frenet centré sur la comète :
Error! = Error! Error!n +
Error! Error!t
Error! =Error! Error!t
Error! = Error! Error!n
Le vecteur unitaire
Error!
n est normal à la trajectoire et centripète ;
Le vecteur unitaire
Error!
t est tangent à la trajectoire et dans le sens du mouvement.
2.6. Quelle est la principale force qui s’exerce sur la comète ? Calculer sa norme en 1989.
Données : Constante universelle de gravitation : G = 6,67 10-11 usi ; Masse du Soleil : MS = 2,0 1030 kg
2.7. Représenter cette force en 1989 en précisant l’échelle.
2.8. Justifier que la deuxième loi de Newton est bien respectée.
3. Vers la troisième loi de Kepler (Valider)
3.1. Pour la comète de Halley, calculer le rapport
Error!
.
3.2. Calculer ce même rapport pour la Terre.
3.3. Que remarque-t-on ? Quelle conclusion peut-on tirer de ces calculs ?

17/04/2017 769788367 3/10
II. Vin et fermentation
Pour améliorer les qualités organoleptiques d’un vin, certains vignerons ensemencent les lies avec une bactérie
lactique de manière à réaliser la transformation de l’acide malique en acide lactique, suivant la réaction d’équation :
HO2C – CH(OH) – CH2 – CO2H(aq) CH3 – CH(OH) – CO2H(aq) + CO2(g)
acide malique
acide lactique
1.1. Quel est le rôle des bactéries dans la transformation ?
1.2. Ecrire la formule semi-développée de l’acide malique ; Y entourer les groupes caractéristiques et nommer les
fonctions correspondantes.
1.3. Ecrire la formule semi-développée de l’acide lactique et identifier son(ses) carbone(s) asymétrique(s).
1.4. Donner la représentation de Cram de l’acide lactique ainsi que celle de son énantiomère.
1.5. Donner la formule semi-développée d’un isomère de constitution de l’acide lactique qui possède les mêmes
fonctions, mais qui n’est pas chiral.
1.6. L’acide tartrique est l’acide organique le plus abondant contenu dans le vin. Les molécules et
représentent deux de ses isomères. Comment qualifier ces isomères l’un par rapport à l’autre ? Justifier.
2. Spectres RMN
2.1. Les spectres RMN du proton de l’acide lactique et de l’acide malique ont été réalisés sur le doc.1 page 9.
On n’a représenté que les multiplets caractéristiques. Attribuer chaque spectre en justifiant.
3. Suivi de la fermentation par chromatographie
Pour suivre l’évolution de la fermentation malolactique les vignerons utilisent couramment la chromatographie
sur papier. L’éluant utilisé est un mélange de butan-1-ol et d’acide éthanoïque.
3.1. Ecrire les formules topologiques des molécules de l’éluant.
3.2. Indiquer la polarisation des liaisons polaires du butan-1-ol.
Données : électronégativité de quelques éléments chimiques : χF = 4,0 ; χO = 3,5 ; χC = 3,0 ; χC = 2,6 ; χH =
2,2 ; χNa = 0,9
À deux dates différentes, le 9 décembre et le 26 décembre, un viticulteur a réalisé une chromatographie de
certains vins numérotés de sa production (voir doc.2).
3.3. Expliquer comment la chromatographie permet de suivre la cinétique de la fermentation malolactique
(FML).
3.4. Parmi les vins testés dans le chromatogramme du 26 décembre, quels sont ceux pour qui, à la date indiquée,
la FML n’a pas commencé, est en cours de réalisation, est terminée ?
3.5. Pourquoi la chromatographie n’est-elle pas suffisante pour contrôler la réaction ?
Doc.2 : Référence et chromatographies des vins

17/04/2017 769788367 4/10
4. Suivi de la fermentation par dosage
Parallèlement, un organisme de contrôle suit régulièrement l’évolution de la présence d’acide malique dans un
vin. Pour un volume V = 50,0 mL de vin, les résultats sont les suivants :
Concentration massique Cm
en acide malique (en g/L)
3,60
2,37
1,51
0,82
0,48
0,27
0,16
0,07
0,03
0,02
Date t (en jours)
0
4
8
12
16
20
24
28
32
36
4.1. Exprimer la concentration molaire C de l’acide malique en fonction de sa concentration massique. Calculer
sa valeur initiale dans le vin étudié.
4.2. A l’aide éventuellement d’un tableau d’avancement, exprimer littéralement l’avancement de la réaction x en
fonction de Cm et des constantes du problème.
4.3. Vérifier que, numériquement on a, pour x en mmol et Cm en g/L : x (t) = 1,34 – 0,373×Cm(t)
4.4. On obtient la courbe du doc.3 page 9. Déterminer le temps de demi-réaction.
4.5. Le dosage a été fait sur le vin n°17, alors que son ensemencement fut le 1er décembre. Déterminer les
concentrations massiques en acide malique dans le vin n°17 au moment des chromatographies. Ces valeurs
confirment-elles les observations des chromatogrammes ?
Données : MC = 12 g/mol ; MO = 16 g/mol ; MH = 1,0 g/mol ; On considère la FML achevée lorsque la teneur
en acide malique résiduel est inférieure à 0,20 g/L.

17/04/2017 769788367 5/10
III. Les ondes sonores et l’oreille – Non-spécialistes seulement
Document 2 : Le diagramme de Fletcher indique les courbes isosoniques qui correspondent aux niveaux d’intensité
sonore perçue par l’oreille.
Sur la figure 1 ci-dessous, on a le diagramme pour une personne « normale ».
Sur figure 2 ci-dessous, on indique les limites de la parole et de la conservation.
Document 3 :
Document 1 : Camille réalise les observations suivantes :
Aucun signal sonore ne nous parvient du Soleil, alors qu’il s’y déroule en permanence de gigantesques
explosions.
Une bougie est placée devant un haut-parleur qui émet un son très grave. La flamme se rapproche et s’éloigne
alternativement de la membrane du haut-parleur, mais elle n’oscille pas dans la direction perpendiculaire.
Document 4 : Données
Intensité sonore de référence : I0 = 1,0 .10 -12 W.m -2
Le niveau d’intensité sonore L d’une source s’exprime par L = 10 log(Error!) avec I, l’intensité sonore de la
source, en watt par mètre carré.
L’intensité sonore I à une distance d d’une source émettant dans toutes les directions est liée à la puissance P de
cette source par : I = Error! avec S, la surface de la sphère de rayon d : S = 4 . d2
- - - - - seuil d’audibilité
500
Figure 2
Figure 1
Fréquences (Hz)
40
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%