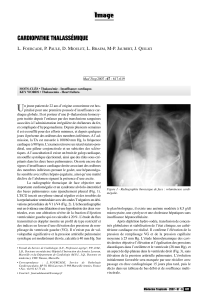
IV- Les acteurs du système cardio circulatoire

1/13
Marine Le Pommelet et Laure Daniel
15/02/2011
EC physio-pharmaco, physiopathologie de l’insuffisance cardiaque, Pr Carré
Le poly est disponible sur le réseau pédagogique.
PHYSIOPATHOLOGIE DE
L’INSUFFISANCE CARDIAQUE (IC)
I- Définition de l’insuffisance cardiaque
A- Classification
- selon la région anatomique altérée :
Insuffisance cardiaque ou ventriculaire gauche
Insuffisance cardiaque ou ventriculaire droite
Insuffisance cardiaque globale
- selon le temps majeur de l’insuffisance :
insuffisance cardiaque diastolique : la fonction de relaxation du cœur est altérée
insuffisance cardiaque systolique : altération de la contraction cardiaque
- selon le stade :
insuffisance cardiaque compensée : le patient a une IC mais par les mécanismes
d’adaptation il arrive à compenser. Il est peu gêné dans son quotidien.
insuffisance cardiaque décompensée : le patient a une poussée d’IC et sa maladie
est déséquilibrée, c’est généralement un épisode aigu
- selon la temporalité :
insuffisance cardiaque aigue : poussée (généralement la 1ère) d’insuffisance
cardiaque sur quelques jours, après un IDM par exemple. Après traitement,
l’insuffisance cardiaque disparaît.
Insuffisance cardiaque chronique : le cœur est altéré de manière définitive après
une 1ère poussée. Le patient est traité à vie.
Ex : IDM très important IC aigue par manque de contraction du cœur grâce aux
médicaments le patient n’est plus IC
Mauvais fonctionnement d’une valve poussée d’ICA changement de la valve
disparition de l’IC
Le cours se basera sur l’insuffisance ventriculaire systolique
chronique.

2/13
B- Définitions
On peut donner 3 définitions à l’insuffisance cardiaque :
1) 1ère définition
L’insuffisance cardiaque est la limite des adaptations du cœur aux conditions de travail anormales
auxquels il est soumis. Par exemple, lors d’une HTA chronique, le cœur fait des efforts
supplémentaires pour surpasser l’excès de pression. Quand ses limites d’adaptation sont dépassées
ou épuisées, on parle d’insuffisance cardiaque.
Pour autant cette définition n’est pas satisfaisante dans la mesure où elle limite l’insuffisance
cardiaque au cœur seul, alors que la maladie a des répercussions sur tout l’organisme.
Par exemple, une insuffisance cardiaque peut être révélée par une insuffisance rénale provoquée par
la mauvaise perfusion de l’organe.
2) 2ème définition
L’insuffisance cardiaque est considérée comme une maladie générale (touchant tout l’organisme)
résultant de l’incapacité du cœur à adapter le débit sanguin aux besoins métaboliques et
fonctionnels des différents organes dans des conditions de pressions de remplissage ventriculaires
normales. L’insuffisant cardiaque se plaint d’être essoufflé et fatigué. Le cœur ne peut plus envoyer
assez de sang au niveau de ses muscles. Ce n’est pas une plainte de mal de cœur.
3) 3ème définition : définition moderne
L’insuffisance cardiaque est un syndrome (ensemble de signes) qui associe des composantes et des
mécanismes cliniques (dyspnée, fatigue), biologiques (modification de la natrémie, augmentation
des BNP) et étiologiques (HTA, valve, IDM) variés en partie dus aux mécanismes compensateurs
cardiaques et extracardiaques (systèmes hormonaux, vasodilatation/vasoconstriction)
II- Epidémiologie
L’insuffisance cardiaque est une maladie qui touche davantage les hommes que les femmes.
Sa fréquence augmente avec l’âge.
L’incidence annuelle est 3 % (c'est-à-dire 3% de patients en plus par an)
La prévalence est en augmentation, du fait de l’âge de la population et des progrès thérapeutiques
en cardio (on meurt moins de son IDM mais on développe par la suite une insuffisance cardiaque)
Les résultats montrent que 8 hommes sur 10 et 7 femmes sur 10 sont IC de 80 à 89 ans alors
qu’avant 30 ans il n’y en a pratiquement pas.
Le pronostic n’est pas très bon.
Les causes de décès consécutifs à une insuffisance cardiaque sont :
- des troubles du rythme pouvant entraîner une mort subite
la cachexie : stade ultime de l’insuffisance cardiaque. Amaigrissement profond avec fonte
musculaire, qui rend incapable de faire le moindre exercice (grabataires)

3/13
Mortalité : 59% chez l’homme contre 47% chez la femme reste élevée malgré les progrès
médicaux.
L’insuffisance cardiaque est classée de I à IV (classification NYHA en fonction de la dyspnée et de
la fatigue du patient)
→ Mortalité en fonction des stades : (à titre purement informatif bien sûr)
- I : 5-7% (peu d’essoufflement au quotidien)
- II : 10-12%
- III : 18-25%
- IV : 35-50% (essoufflement au moindre geste)
III- Etiologies
Au départ , surcroit de travail au niveau du cœur dont les causes peuvent être très variées :
A- Maladies intrinsèques du myocarde
Hypertrophie cardiaque
Cœur dilaté
Infarctus
Infiltration du myocarde (ex : sarcoïdose : maladie pulmonaire avec une infiltration
myocardique possible)
B- Surcharge barométrique (de pression) ou volumétrique
HTA (barométrique)
Valvulopathies
Barométrique : rétrécissements aortique ou mitral
Volumétrique : insuffisances aortique (fuite aortique) ou mitral
Anomalies congénitales
C- Affections extracardiaques (ne concernent ni le cœur ni les
vaisseaux)
Pulmonaire : par exemple emphysème, bronchite chronique, qui donnent d’abord une
insuffisance cardiaque droite
Infections (ex : grippe) :
du muscle : myocardite
des valves : endocardite
Intoxications par différentes drogues, produits, en particulier l’éthylisme.
Les causes principales sont :
- l’infarctus (ischémie) : 50%
- non ischémique : 36,4%
- idiopathique (surtout les IC dilatées) : 4%

4/13
NB : Il existe 0,4% de risque de développer une insuffisance cardiaque post-partum (cause non
ischémique)
IV- Les acteurs du système cardio circulatoire
Le cœur est en relation avec les poumons par la circulation pulmonaire et avec les muscles et les
autres organes tels que le foie et les reins par la circulation périphérique, d’où la plainte
d’essoufflement et de douleurs musculaires. Un dysfonctionnement du cœur entraine un
dysfonctionnement de tout l’organisme.
IV- Physiopathologie
A- Adaptation du cœur : remodelage
Le remodelage ventriculaire est la réponse adaptative du cœur face aux contraintes qui lui sont
imposées. Il se produit des modifications morphologiques et constitutionnelles (le cœur est un
organe dynamique d’un point de vue histologique).
Le remodelage est un facteur important de l’insuffisance cardiaque.
Il s’agit d’un processus évolutif et adaptatif, qui touche toutes les cellules.
« Remodelage : expression génomique aboutissant à des modifications moléculaires, cellulaires et
interstitielles qui se manifestent cliniquement par des modifications de taille, de forme et de
fonction du cœur au décours d’une atteinte cardiaque » Cohn et al J.Am Coll Cardiol 2000
= modification de l’expression de certains gènes
Exemple : La cardiomégalie observée chez les insuffisants cardiaques est une réponse du

5/13
remodelage myocardique. Les gènes ont modifié leur expression.
L’effet bénéfique de ce remodelage est l’hypertrophie qui permet d’adapter le cœur à un surcroit de
travail. Mais lorsque cette adaptation atteint ses limites, on se retrouve dans une inadaptation et on a
donc un effet négatif du remodelage.
D’après le schéma général de Swynghedauw : biologie et pathologie du cœur et des vaisseaux, 2002
Surcharge mécanique
modification de qualité des fibres cardiaques et nouvelle économie musculaire adaptée à la nouvelle
charge
processus adaptatifs : récapitulation du programme fœtal (des gènes qui étaient quiescents sont
réexprimés afin de répondre aux besoins). On retrouve chez l’IC des fibres cardiaques présentes
chez le fœtus, ainsi qu’une modification des l’expression de certains gènes
restauration d’une économie normale
altérations surajoutées : réarrangement du programme fœtal par l’ischémie, la sénescence et les
réactions neurohormonales
cœur trop gros : différents types d’IC
La performance du ventricule gauche peut être évaluée à deux niveaux :
- au niveau des fibres et environnement
- au niveau du cœur entier
1) fibres cardiaques et environnement
Lors d’une altération cellulaire, le remodelage touche toutes les cellules et permet la mise en place
de tous les moyens d’adaptation possible :
- hypertrophie myocytaire
- transformation de fibroblastes en myoblastes
- modification de la matrice extracellulaire vers la fibrose. (Due à la sécrétion de certaines
hormones dans un but adaptatif)
- il n’y a pas de multiplication des vaisseaux (pas de surexpression de gènes permettant
d’augmenter le nombre de vaisseaux ce qui entraîne des problèmes de perfusion = limite de
l’adaptation)
Exemple : IC = cœur fatigué donc diminution du débit cardiaque l’organisme se met en
vasoconstriction pour augmenter les résistances afin de maintenir un PA constante augmentation
du travail du cœur adaptation délétère à la longue.
Des mécanismes moléculaires se mettent en place :
facteurs déclenchant : HTA, infection….
sécrétions de facteurs
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%