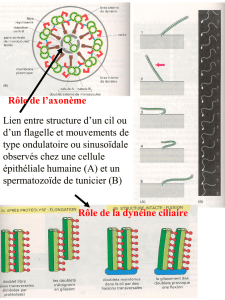
Voir - ULB

35
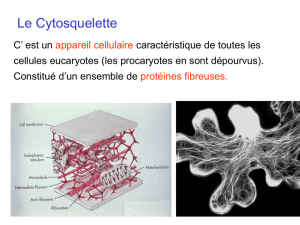
5. Le cytosquelette
C'est un réseau tri-dimensionnel « dynamique » de « polymères protéiques » formant des filaments
au sein du cytoplasme. Il participe au maintien (morphologie) et aux déplacements cellulaire
(mobilité cellulaire et déplacement des organites)
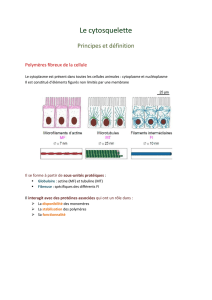
Il y a trois types de filaments résultant de la polymérisation de monomère protéiques différents, du
plus fin au plus épais:
Les microfilaments ont un diamètre de 6 à 8 nm (polymérisation des monomères d'actine). Ils se
trouvent à la surface de la cellule et confère à celle-ci une structure particulière (ronde,
cylindrique...)
Les filaments intermédiaires ont un diamètre de 8 à 12 nm (protéines fibreuses variables). Ils
prennent naissance sur la membrane et se développe dans la cellule. Ils sont absents des cellules
eucaryotes végétales.
Les microtubules ont un diamètre de 25 nm (polymérisation d'hétérodimères, tubuline α et β). Ils
prennent naissance près du noyau et se développe dans la cellule. Ils participent à la dynamique des
différents transports intracellulaires.
Microfilament (Actine)
L'actine en se polymérisant en structures filamentaires, confère à la cellule une structure
tridimensionnelle.
Elle est présente dans toutes les cellules eucaryotes. Dans une cellule, elle représente 5% des
protéines; dans une cellule musculaire, elle représente 20 % des protéines. Il en existe deux formes:
la forme globulaire (monomère: Actine G) et la forme filamentaire (polymères: Actine F)
L'Actine globulaire (G)
C'est une protéine de forme globulaire (Poids moléculaire de 43 kDa = 43.000). Le dalton est l’unité
de masse (1/16 de l’oxygène). Une solution à 1 molaire d'actine pèse 43 kg.
La structure inter-espèce est très conservée.
La structure tridimensionnelle présente une « Fente » dans laquelle peut se « glisser » une molécule
d’ATP. C'est à cet endroit que peut avoir lieu la transformation d'ATP en ADP en fournissant de
l'énergie.
L'Actine filamentaire (F)
Structure : Filaments torsadé de 7 nm de diamètre
Composition : Actine globulaire (Actine G) polymérisée sous forme de filaments torsadés (Actine
F). D'un côté, les monomères d'actine s'ajoute (bout +), de l'autre côté, ils se séparent (bout -) -->
dynamique de polymérisation : équilibre dynamique entre monomère et polymère. Si on marque on
monomère d'actine, on voit qu'il voyage dans le polymère du bout + au bout -. On obtient un
équilibre entre l'élongation et le raccourcissement en fonction de la concentration d'actine G. La
polymérisation implique la présence d'ATP dans le monomère d'actine G.
Fonction : Il y a deux fonctions : la morphologie cellulaire et le mobilité cellulaire.
La morphologie cellulaire est le soutien mécanique de la membrane plasmique, jonctions
cellulaires, augmentation de la surface membranaire et de la surface d’(ré)absorption (intestin, rein),

36
résistance mécanique.
La mobilité cellulaire est la production d'une force motrice en association avec la myosine,
migration de la cellule par polymérisation/dépolymérisation de l'actine fibrillaire (Filipodes -
Lamellipodes). L'énergie mécanique correspond à un glissement de l'actine sur la myosine. Lorsque
plusieurs cellules riches en éléments contractiles s'organisent en tissus, on a ce que l'on appelle un
tissu musculaire.
Exemple 1 : Spectrine (protéine membranaire du globule rouge) dans les globules rouges.
Pathologie : la sphérocytose : anomalie des protéines constituant la membrane du globule rouge qui
deviennent sphériques et fragiles.
Exemple 2 : Actine et dystrophies musculaires : il n'y a pas assez de protéine dystrophine qui est
sécrétée, la membrane de la cellule est donc affaiblie et tente de se déchirer.
Matrice extracellulaire et Contacts Focaux - Lamellipode
Déplacement : polymérisation au front
(lamellipode), dépolymérisation du cortex
d’Actine à l’arrière par rapport au sens de
déplacement de la cellule
Contacts Focaux avec la matrice extracellulaire
et l’actine
Mobilité & Phagocytose
Mécanisme qui permet a certaines cellules spécialisées ainsi qu'a certains organismes unicellulaires
(protistes) l'ingestion de particules étrangères tels que des bactéries, des débris cellulaires, des
poussières... La phagocytose a un rôle important dans la fonction immunitaire, c'est en effet un
moyen de défense de l'organisme, notamment lors d'infections bactérienne et parasitaire.
Les filaments d'actine entoure le parasite et le fait entrer dans la cellule.
La Listériose
La listériose est attrapée par contamination orale. Elle affecte plus particulièrement les femmes
enceinte, les enfants en bas âge et les personnes immunodépressives. Elle provoque une septicémie,
des méningites ou des avortements spontanés.
Protéines associées à l'actine: rôles et fonctions
La concentration en Actine-G a une action sur la régulation de la polymérisation.

37
La spectrine jour un rôle dans l'assemblage des microfilaments pour la formation du cortex
cellulaire qui est un assemblage de fibres de tensions au sein de la cellule.
Deux Présentations de l’actine
Faisceaux : filaments d'actine parallèles
A l'intérieur de la cellule : fibre de tension : filaments écartés et les côtés – et + ne sont pas dans le
même sens (faisceau contractile). La protéine associée est l'α-actinine.
Sur les filipodes qui sont en bout de cellule. On a un faisceau parallèle serré. La protéine associée
est la fimbrine.
Réseau : filaments d'actine croisés orienté aléatoirement se trouvent dans le cortex cellulaire. Le
réseau est semblable à un gel. La protéine associée est la filamine : protéine dimérique de 280 kDa.
On la retrouve à l'intersection des filaments d'actine.
Les différentes protéines et leur fonction
Tropomyosine
Consolidation des filaments
Fimbrine et alpha-actinine
Formation des faisceaux de filaments. La
fimbrine augmente la surface membranaire.
Filamine
Réticulation des filaments en un gel
Gelsoline
Fragmentation des filaments
Myosine II
Glissement des filaments
Myosine I
Mouvement des vésicules sur les filaments
Spectrine
Ancrage latéral des filaments à la membrane
plasmique
Thymosine
Rétention des monomères d'actine. Régulation
de la concentration de l'actine au moment de la

38
polymérisation.
Muscle : association d'actine et de myosine
Il existe un cycle de liaison/séparation entre l'actine et la myosine. Les fonctions de cette
association sont le transport intracellulaire (organites, vésicules, transport axonal…) et la
contraction musculaire (mécanisme: variation de la concentration en calcium intracellulaire dans la
fibre musculaire)
Qu’est ce que la myosine? C'est un “Hexamère” qui contient 2 chaînes lourdes et 4 chaînes légères.
Le couple protéique Actine/Myosine peut produire un travail mécanique à partir de l’énergie
contenue dans la molécule d’ATP. Elle se compose d'une tête, d'un coup et d'une queue. La tête
interagit avec l'actine. Plusieurs molécules de myosine s'assemblent entre elles, on a des têtes de
chaque côté et une partie centrale sans tête. L'actine est une protéine filamenteuse de structure
hétérogène par rapport à l'actine. La myosine peut représenter jusqu'à 35% des protéines totales
dans les cellules musculaires des mammifères.

39
Les fibres musculaires sont une alternance de bandes sombres (superposition actine & myosine =
[bande A]) et de bandes claires (Actine = [Bande I]). L'interaction actine-myosine est contrôlée par
le complexe « tropomyosine/troponine »
Complexe de jonction
Il existe plusieurs types de jonction: les jonctions serrées, les jonctions adhérentes (Actine) et les
desmosomes (Filaments Intermédiaires).
Poison de l'actine
Deux toxiques interagissent avec la dynamique de polymérisation de l’actine :
1.La Cytochalasine (toxine produite par un champignon microscopique). Elle se lie à l’extrémité (+)
de l’actine F et bloque l’addition de monomères. La dépolymérisation “spontanée” à l’extrémité (-)
cause la disparition du filament
2.Phalloïdine (Amanite Phalloïde) se lie le long du filament d’actine et le stabilise (= blocage de la
dynamique de fonction). Techniquement, la phalloïde associée à un marqueur fluorescent marque
l'actine F qui devient visible en microscopie à fluorescence.
Microtubules
Structure : Tubules (cylindres creux) de 25 nm de diamètre
Composition : Hétérodimère de tubulines alpha et béta globulaire formant 13 protofilaments ayant
la même polarité associés latéralement les uns aux autres, associées à des protéines (kinésine,
dynéine, tau,...)
Fonction: arrimage des organites internes, organisation des compartiments intracellulaires,
transports intracellulaires (ex: fuseau mitotique)(les mouvements des chromosomes sont consécutifs
à la modification de l'équilibre polymérisation – dépolymérisation des microtubules), mouvement
(cils et flagelles)
Le Centriole – Centrosome
Le centriole consiste en une structure composée de microtubules qui organisent en association avec
des protéines spécifiques le fuseau mitotique au cours de la division cellulaire.
Le microtubule est fixé au niveau de son extrémité (-) au centre organisateur (le centrosome). Le
centriole, c'est neuf triplets de microtubules. Le centrosome, c'est deux centrioles disposés à 90°
l'un par rapport à l'autre et des protéines qui associent les triplets.
 6
6
 7
7
 8
8
1
/
8
100%