Présentation du document : Quelques pages internet (disponibles

Présentation du document :
Quelques pages internet (disponibles par un lien) sur un forum santé où une internaute pose la question suivante : « … on
veut convertir la glycémie de mg/dl ou vice-versa en mmol/l. Qu'est ce que cela veut dire ? ». D’autres internautes répondent
…
Le document de travail est constitué d’un lien internet vers le forum Doctossim (http://forum.doctissimo.fr/) avec des
internautes qui présentent leurs connaissances sur la glycémie et d’un questionnaire qui permet d'analyser les propos des
internautes.
D’autres liens sur la glycémie et le diabète :
http://www.essentielsante.net/ebn.ebn?pid=23&domain=ess&site=8&uid=documentess_103&rub=39
http://www.doctissimo.fr/html/sante/analyses/ana_meta_sucres01.htm
http://www.med.univ-rennes1.fr/excomp/sommaire.html#diab (très technique)
http://www.esculape.com/fmc/dnid2.html
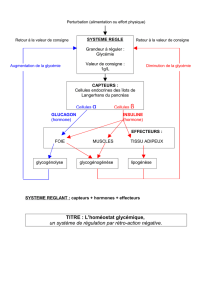
Le programme : LA SANTÉ
Les citoyens doivent acquérir une culture scientifique de façon à procéder à des choix raisonnés en matière de santé.
L'objectif de ce thème est de montrer et d’expliquer le rôle des sciences physiques et chimiques dans les domaines du
diagnostic médical et des médicaments.
NOTIONS ET CONTENUS
COMPÉTENCES ATTENDUES
Le diagnostic médical : l’analyse de signaux périodiques, l’utilisation de l'imagerie et des analyses médicales
permettent d’établir un diagnostic. Des exemples seront pris dans le domaine de la santé (électrocardiogramme,
électroencéphalogramme, radiographie, échographie, fibroscopie, …).
L’observation de résultats d’analyses médicales permet d’introduire les notions de concentration et d’espèces chimiques
ainsi que des considérations sur la constitution et la structure de la matière.
Solution : solvant, soluté, dissolution d’une espèce
moléculaire ou ionique.
Analyses médicales ; concentrations massique et molaire
d’une espèce en solution non saturée.
La quantité de matière. Son unité : la mole.
Constante d’Avogadro, NA.
Masses molaires atomique et moléculaire : M (g.mol-1).
Savoir qu’une solution contient des molécules ou des ions.
Savoir que la concentration d'une solution en espèce
dissoute peut s'exprimer en g.L-1 ou en mol.L-1.
Connaître et exploiter l’expression des concentrations
massique et molaire d’une espèce moléculaire ou ionique
dissoute.
Calculer une masse molaire moléculaire à partir des masses
molaires atomiques.
Pratiquer une démarche expérimentale pour déterminer la
concentration d’une espèce (échelle de teintes, méthode par
comparaison).

Accéder au document en cliquant sur le lien ci-dessous :
http://forum.doctissimo.fr/sante/diabete/convertir-glycemie-mmol-sujet_150926_1.htm
Quelques questions à propos de ce document
Données : Représentations symboliques de quelques atomes : carbone
C
12
6
, hydrogène
H
1
1
, oxygène
O
16
8
Masse d’un nucléon : m = 1,67.1027 kg
1. Définir la glycémie.
2. Relevez les mots clés dans les interventions des internautes qui ont un lien avec le domaine de la biologie ou de la
chimie.
3. A quelle molécule particulière est liée la glycémie ? (recherchez sa formule chimique, les atomes qui la composent,
comment ils sont reliés entre eux dans la molécule, comment écrire une représentation de cette molécule, etc.)
4. Quelles sont les différentes unités utilisées dans le document ?
5. A quelles grandeurs correspondent ces unités ?
6. D’après le texte, expliquez en reformulant la signification de la mole.
7. Quel sous-multiple de la mole est évoqué dans le document ?
8. Expliquez comment calculer la masse d’une molécule de ce sucre ? Calculez la masse d’une molécule.
9. Expliquez comment calculer la masse d’une mole de ce sucre ? Calculez la masse d’une mole de ce sucre et vérifier
que la valeur donnée dans le document (180 g.mol1) est correcte.
10. Pour simplifier, on peut considérer qu’une glycémie moyenne correcte a pour concentration molaire 5,5 mmol.L1 de
sucre dans le sang. Un des internautes indique que cette glycémie correspond à une concentration massique de
1 mg.dL1. Faites le calcul pour vérifier si l’internaute dit juste ou non.
Sujet du forum : Convertir la glycémie de mol.L1 en g.L1 Diabète
D’après le site Doctossimo
1
/
2
100%