Endocrinologie : cours n°3 Jeudi 24 janvier 2008 10h30

- 1 -
Endocrinologie : cours n°3
Jeudi 24 janvier 2008
10h30-12h30
Dr DE ROUX
Ronéotypeuse : Isabelle NAIIM HABIB
BIOCHIMIE :
AXE HYPOTHALAMO-
HYPOPHYSAIRE

- 2 -
PLAN
1) Anatomie fonctionnelle
a) Hypothalamus
b) Hypophyse
c) Liens entre l’hypothalamus et l’hypophyse
d) Organisation en noyaux de l’hypothalamus
e) Organisation cellulaire de l’hypophyse
f) Conclusion
2) Développement de l’axe hypothalamo-hypophysaire
a) Développement de l’hypothalamus
b) Développement de l’hypophyse
3) Biochimie du système hypothalamo-hypophysaire
a) Neuropeptides
b) Récepteurs
c) Voies de signalisation intracellulaires
4) Les différents axes neuro- endocriniens
a) Axe corticotrope
b) Axe thyréotrope
c) Axe gonadotrope
d) Axe somatotrope
e) Axe lactotrope
5) Pathologie
6) Les neurones magnocellulaires
PS : J’ai regroupé certaines parties du prof car sinon, cela faisait trop de répétitions
(Vous allez voir que niveau répétitions, il y en a déjà pas mal mais bon, il paraît que
plus on répète et plus ça rentre…).

- 3 -
1) Anatomie fonctionnelle
a) Hypothalamus
L'hypothalamus est une structure située dans le cerveau, c'est une structure
neuro- endocrinienne, c'est-à-dire qu'elle est composée de neurones et elle
participe à la fonction endocrine. En effet, elle régule un certain nombre
d'effecteurs au niveau de l'hypophyse, mais pas seulement, elle va aussi avoir
d'autres fonctions dont on parlera peu car on se limite à la fonction
endocrinienne.
C’est un organe qui est très conservé. Il a été démontré qu'un certain nombre de
composants de cet organe sont présents dans les êtres les plus inférieurs, avant la
séparation vertébrés/invertébrés.
C'est un système intégrateur qui va recevoir des informations
- neuronales, notamment du cortex,
- endocriniennes, notamment de la périphérie sous forme de rétrocontrôle,
et qui va recevoir des informations internes (on vient d'en parler) et externes
(exemple : la lumière reçue par l'intermédiaire de la rétine est transformée en 1
signal électrique qui passe par l'intermédiaire des neurones, arrive à l'hypothalamus
au niveau du noyau supra chiasmatique notamment. Cet influx nerveux dépendant de
la lumière participe à la régulation du cycle nycthéméral et donc du cycle circadien
chez l'homme.)
Il participe au contrôle des hormones périphériques, à la fonction motrice d’un
certain nombre d’organes digestifs et à certains comportements alimentaires
voire à certains comportements agressifs.
b) Hypophyse
Elle est située dans la selle turcique. C’est une glande qui est en contact étroit
avec le cerveau.
Elle est composée de deux régions :
- une antérieure : organe endocrine
- une postérieure appelée neuro-hypophyse car composée d’extrémités
axonales de neurones dont le corps cellulaire est situé dans
l’hypothalamus. Ces neurones sont les neurones magnocellulaires qui vont
synthétiser la vasopressine notamment.
Elle reçoit des informations
- de l’hypothalamus, notamment par l’intermédiaire d’un système vasculaire
qui est le système porte
- de la périphérie qui peuvent être métaboliques ou hormonales.
Ces informations périphériques sont très importantes car il y a souvent un stimulus
hypothalamique qui donne l’information à l’hypophyse de synthétiser certaines
hormones et, en contrepartie, en périphérie, il y a des stimuli qui vont surtout être
inhibiteurs (parfois activateurs), qui vont chercher à réguler cette sécrétion.

- 4 -
La fonction immédiate de l’hypophyse est de synthétiser un certain nombre de
peptides dont la fonction est d’aller réguler les glandes endocrines périphériques,
de participer à l’homéostasie hydro électrolytique au niveau du rein, et de
participer à certaines fonctions au niveau de l’utérus.
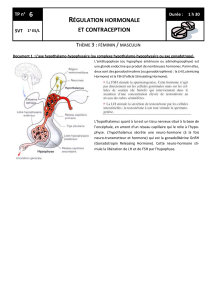
Schéma : Le chiasma optique est intéressant dans le sens où il donne des informations,
en clinique sur l’hypophyse. En effet, lorsqu’il y a un adénome de l’hypophyse, il y a une
expansion cellulaire au niveau de l’hypophyse dont la conséquence est la compression
du chiasma optique et donc une des indication pour opérer ces patients est la
compression de ce chiasma optique pour éviter les conséquences au niveau de la vision.
Chiasma optique
Hypothalamus
Hypophyse

- 5 -
c) Liens entre l’hypothalamus et l’hypophyse
Ce système porte est extrêmement important. Il n’est pas présent avec un
développement aussi important chez tous les mammifères, il est surtout très développé
chez les primates.
d) Organisation en noyaux de l’hypothalamus
L’hypothalamus est organisé de façon un peu particulière, contrairement à d’autres
régions du cerveau, il est organisé en noyaux et chaque noyau a une certaine spécificité
fonctionnelle. On définit deux grands types de neurones :
- Les neurones parvicellulaires qui ont pour fonction de synthétiser des
peptides, dont les corps cellulaires sont situés dans les noyaux et dont
l’extrémité axonale est située au niveau de l’éminence médiane.
L’éminence médiane est une structure qui ne possède pas de barrière
hémato-encéphalique c’est-à-dire qui a la possibilité de subir des
stimulations par des peptides dans la circulation sans pénétration dans le
cerveau, c’est la région qui permet l’interaction entre l’hypothalamus et le
système vasculaire dans le sens où c’est là que sont relargués tous les
peptides de l’hypothalamus qui sont synthétisés dans les neurones
parvicellulaires.
Donc le but des neurones parvicellulaires +++ est une neurosécrétion vers le
système porte hypothalamo-hypophysaire.
- Les neurones magnocellulaires qui sont des neurones beaucoup plus gros
qui ont donc un corps cellulaire situé dans l’hypothalamus. Ils synthétisent
l’ocytocine et notamment la vasopressine. La neurosécrétion va survenir
dans la veine hypophysaire, c’est-à-dire que l’extrémité est située au
niveau de la post-hypophyse.
- Il y a des neurones dont les corps
cellulaires sont situés dans l’hypothalamus
et dont l’extrémité axonale est située dans
l’hypophyse. Il s’agit de la post-hypophyse.
Le lien se fait de façon logique par
l’intermédiaire des axones.
- Pour l’antéhypophyse, il n’y a pas de lien
cellulaire direct : le lien passe par un réseau
vasculaire qu’on appelle le système porte
qui a donc pour fonction de recevoir des
peptides hypothalamiques et de les
transporter à l’hypophyse antérieure où ils
vont pouvoir aller activer leurs récepteurs
spécifiques et donc réguler la voie
endocrinienne.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
1
/
25
100%