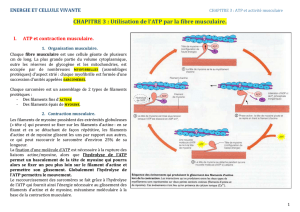
Répartition du MB entre les différents organes Poids en Kg % relatif

Biologie énergétique : Introduction
C’est l’étude des organismes vivants assimilés à un système de transfert d’énergie. On peut donc appliquer
à cet organisme les lois de la thermodynamique. L’énergie former provient de la combustion des aliments,
il n’y a que cette énergie ainsi produite qui est utilisée, les autres formes d’énergie ne sont pas utilisées. Le
phénomène de combustion qui entre en jeu se produit grâce à la présence d’O2 (dans les phénomènes
respiratoires). Cette énergie sert aux dépenses de fonctionnement qui sont la thermogenèse de
réchauffement (énergie qui doit lutter contre le froid) ou l’activité physique pas seulement sportive mais
musculaire. S’il n’y a pas de dépense de fonctionnement l’énergie servira aux dépenses de fond ; c’est le
métabolisme basal.
1-Les lois de la thermodynamique
a) Premier principe
L’énergie contenue dans un système clos faisant passer d’un état initial à un état final reste constante.
Ereçue = E dépensée ± ΔE
Dans le cas d’un homme, l’énergie reçue provient des aliments et l’énergie dépensée provient de l’activité
physique. La variation d’énergie représente un stock d’énergie du tissu adipeux. On peut noter que l’énergie
reçue peut être transformée en d’autres formes comme par exemple l’énergie mécanique (travail), l’énergie
chimique (synthèse moléculaire), énergie de transport des molécules de part et d’autres de la membrane
(phénomène osmotique) c’est une énergie convertible. On va donc utiliser des unités communes qui est
le Joule ou KJ mais couramment on utilisera la calorie ou Kcal ; à savoir que 1Kcal = 4,18 joules. La calorie
représente la quantité de chaleur qui peut élever la température de 1 g d’eau d’1 °C.
b) Deuxième principe
Notion d’entropie qui représente la dégradation d’énergie, le désordre croissant de la matière. Quand
l’énergie passe d’une forme à une autre, elle se dégrade en partie sous forme de chaleur. Il n’y a pas de
rendement à 100%, cette énergie sous forme de chaleur est perdue et est restituée à l’environnement.
L’organisme vivant est représenté par une hétérogénéité de ses structures qui vont évoluer vers
l’égalisation. Pour lutter contre le désordre, l’organisme utilise une énergie haute qualité (chimique) qu’il
transforme en énergie basse qualité (chaleur), au passage il va prélever de l’ “ ordre ”.
Notion de biosphère
On utilise une cloche retournée sur un milieu végétal, humains avec aussi de l’air (c’est un système clos) ;
on retrouve le milieu quelques milliers d’années plus tard et on se rend compte qu’il ne reste plus que des
cendres mais la quantité d’énergie mesurée reste toujours la même.
Aliments (énergie potentielle) Respiration cellulaire (acétylCoA) énergie utile
disponible
Mise en réserve utilisée quand jeûne par exemple
Energie mécaniq.
Travail externe
Energie osmotique
Energie chimique
Les flux peuvent se mesurer à plusieurs niveaux. L’énergie sous forme chimique est appelée ATP, elle est
utile et disponible et est utilisée dans des phénomènes mécaniques, osmotique forme de transport vers
les sites de production (mitochondries) aux sites d’utilisation. Cette molécule peut se stocker à court terme.
Si l’on fait un exercice long, on va puiser dans nos réserves de graisse pour fabriquer de l’ATP.
Premier chapitre
L’aliment est un composé complexe comestible, il apporte de l’énergie. Un aliment est composé d’un
certain nombre de nutriment que l’on peut classer en différents groupes.
Par exemple, le pain contient comme nutriments du gluten, de l’amidon (c’est le nutriment), des vitamines,
des sels minéraux …
Il faut savoir que tous les nutriments n’apportent pas d’énergie, c’est le cas notamment des fibres. Chaques
nutriments n’apportent pas la même quantité d’énergie. On distingue alors 4 catégories :
1. Les protides (peptides + protéines + acides aminés)
2. Les lipides (matière grasse)
Perte sous forme de
chaleur
Environnement

3. Les glucides qui sont soit des monosaccharides (ose) comme le fructose, des disaccharides (dioside)
comme le lactose ou le saccharose, les polysaccharides (polyoside) comme l’amidon.
4. Les alcools
L’énergie contenue dans un aliment est mesurée grâce à une bombe calorimétrique, c’est un système où
l’on place l’aliment à étudier dans un sac entouré d’une enceinte pleine d’eau isolée de l’environnement ;
on met de l’O2 dans le sac pour la combustion et un dispositif de mis à feu pour démarrer cette combustion.
On va, à la fin mesurer la chaleur produite représentant la variation de la température de l’eau environnant.
Pour les glucides : G + O2 CO2 + H2O + E soit 4,1 Cal/g
Pour les lipides : L + O2 CO2 + H2O + E soit 9,45 Cal/g
Pour les protides : P + O2 CO2 + H2O + N2 + E soit 5,65 Cal/g
Ce sont des valeurs moyennes que l’on calcule par l’intermédiaire d’une bombe calorimétrique mais ce
n’est pas les mêmes valeurs que l’on retrouve pour le corps humain et ceci pour 2 raisons :
Il y a encore un peu d’énergie dans les excrétats (pour 2000 Cal ingérer, il reste encore 50 Cal dans les
selles). Tous les ingestats ne sont pas absorbés et le rendement est quand même de 97% soit (2000 –
50)/2000 qui représente le coefficient d’utilisation digestive CUD = (Qi – Qe)/Qt
Ce coefficient est pour les glucides d’environ 100%, pour les lipides 95%, pour les protides 78 à 97 % selon
la nature des protides et pour l’alcool de 100%.
La deuxième raison et que les protéines se dégradent dans l’organisme mais pas jusqu’au stade de N2 mais
de l’urée.
P + O2 CO2 + H2O + Urée + E soit 4,35 Cal/g
Valeurs énergétiques des nutriments :
Glucides = 4 Cal/g
Lipides = 9 Cal/g
Protéines = 4 Cal/g
Alcool = 7 Cal/g
Bioénergétique
Introduction :
La bioénergétique est l’étude des organismes vivants envisagés comme des systèmes de transfert
d’énergie.
L’énergie provient de la combustion des aliments :
Principes de la thermodynamique :
Dans un système isolé, si l’on passe d’un état initial à un état final et que le système est isolé, le
contenu en énergie reste le même.
Si par contre il y a une variation du contenu de l’énergie :
Energie reçue = énergie dépensée ΔE. (variation de l’énergie)
Energie reçue des aliments = énergie dépensée (fcont et fond) ΔEc (énergie corporelle)
L’énergie reçue par les aliments est convertie en d’autre sorte d’énergie : énergie chimique
(nécessaire au transport des ions), mécanique…
On utilise comme unité la calorie ou le kilojoule. Une calorie permet d’élever la température d’1
gramme d’eau de 1°C.

Comme la calorie est une petite unité, on utilise volontiers la kilocalorie (kcal) ou grande calorie.
Principe d’entropie : où principe du désordre croissant (de la dégradation de l’énergie)
L’énergie lorsqu’elle passe d’une forme à une autre, se dégrade et apparaît sous forme de chaleur.
L’organisme vivant est caractérisé par la diversité et la complexité de la structure.
Pour lutter contre cette tendance au désordre, l’organisme utilise l’énergie chimique (une énergie de
haute qualité). L’organisme la restitue sous forme d’énergie de LowTeel (chaleur) à l’environnement.
les aliments contiennent une énergie potentielle :
L’ATP est rattaché à ce système.
I) Les apports nutritionnels :
I)1) les aliments (assemblage complexe)
On recherche dans notre alimentation les nutriments situés dans les aliments :
Bombe calorimétrique :
On brûle un aliment dans une bombe calorimétrique, on observe :
G(glucide) + O2 CO2 + H2O + E.
E = 4,1 Kcal/g.
L(lipide) + O2 CO2 + H2O + E.
E = 9,45 Kcal/g.
Protide + O2 CO2 + H2O + E.
E = 5,65 Kcal/g.
On étudie ici le CUD (coefficient d’Utilisation Digestive) :
Qi : quantité ingérée
Qe : quantité excrétée
Si, par exemple, on ingère une bille, elle ressortira intact, alors :
Pain
Glutène
Amidon
Vitamines
Protides
Protéine
Peptides
Acides aminés
Glucides
Mono-saccharide : ose.
Disaccharide : lactose saccharose.
Polysaccharide : amidon.
Alcool
Apport énergétique
Lipides
Corps gras
CUD =
Qi – Qe
Qi
H2O
Biosphère
Quelques millions
d’années plus tard.
Q
Tout a été transformé en chaleur
Respiration
cellulaire.
oxygène
Réserve de graisse
(tissu adipeux)
Energie disponible
(utile)
Energie chimique
(macromolécules)
Energie osmotique
(transport)
Energie mécanique
Travail mécanique
(Wméca)
Chaleur
O2
°C
H2O
Ingesta
Excreta
2000
50
1950

= 0
Sur 2000 Kcal ingérée, notre organisme en prélève 1950 grâce à la
digestion (CUD) et rejette environ 50Kcal.
CUD =
2000 – 50
2000
=
1950
2000
= 97%
Pour les glucides :
CUDG = 100%
Pour les lipides :
CUDL = 95%
Poule les protides :
CUDP = 78 à 97%
Nombre de calorie par gramme de substances
Glucides 4Kcal/g.
Protides 4Kcal/g.
Lipides 9Kcal/g.
Alcool 7Kcal/g.
Les dépenses énergétiques
Tous les aliments sont convertis en énergie disponible grâce à l’utilisation de l’O2, ces aliments
seront transformés en chaleur mais aussi pour une petite part en travail externe rendu à
l’environnement.
1- La DE au repos
Comment mesurer cette dépense énergétique (DE) ?
En considérant que tous sera converti en chaleur.
1. Par calorimétrie directe : on enferme un sujet dans un calorimètre (chambre fermée
qui empêche les échanges avec l’extérieur). On étudie ensuite la dépense de
chaleur par un serpentin contenant de l’eau car on connaît le débit de l’eau à
l’entrée et à la sortie du tube. C’est une technique très peu utilisée car nécessite un
calorimètre assez grand pour y faire rentrer un homme.
2. Par mesure de la quantité d’O2 utilisée car l’énergie est rendue disponible grâce à
l’O2 respiré. Les nutriments qui sont oxydés libèrent du CO2, H2O voire de l’urée
on regarde alors la quantité d’O2 consommée.
Combien, la combustion de glucose, produit d’énergie ?
C6H12O6 + 6CO2 6CO2 + 6H2O + 686 Cal, c’est une expérience qui est faite in vitro mais les
conditions de combustion in vivo sont identiques et produisent la même quantité d’énergie.
Sachant qu’une mol d’O2 représente 22,4 L d’O2 et que les 686 Cal sont apportées par 6 molécules
d’O2, on en déduit que cette combustion apporte environ 5,1 Cal/L d’O2.
Cette valeur est appelée Valeur Energétique du Litre de O2 lors de l’utilisation du Glucose. On
peut effectuer la même expérience pour les AG et les protéines.
VELO2LUG = 5,1 Cal/l O2
VELO2LUL = 4,66 Cal/l O2
VELO2LUP = 4,64 Cal/l O2
CUDbille =
1 – 1
1

La quantité d’O2 utilisée pour la combustion met à la disposition une moyenne de 4,85 Cal/l O2.
Il suffit donc pour connaître la DE calculer la consommation d’O2. La DE s’exprime en Cal/min.
La quantité d’O2 présente en permanence dans l’organisme est très faible car il n’y a pas de forme de
stockage, sans O2 on meurt en 3 minutes. Le peu de réserves peut quand même faire le système tampon pour
améliorer l’adaptation à un effort physique.
Si on mesurait la DE d’un sujet assit, il faudrait le faire après ces trois minutes d’adaptation.
2- Analyse factorielle de la DE
Métabolisme basal MB
C’est la consommation d’O2 exprimée en litres d’O2 par heure ou en Cal/min chez un sujet en situation de
jeun (12h) protéique (18h). Cet état physiologique élimine l’état de digestion dans un environnement
thermique neutre, au repos musculaire depuis ou moins 30 Minutes et aussi au repos émotionnel (sans
stress). On mesure en fait la DE qui est liée uniquement à la survie.
Ces conditions ne sont plus utilisées car on a remarqué que le métabolisme du sommeil descend encore plus
bas.
Métabolisme au repos MR, on le mesure chez les personnes à jeun d’environ 12 h. Il faut savoir que le MR
dépend de la dimension corporelle, du travail de certains organes comme le cœur, les reins, le foie … Cet
ensemble d’activité est plus grand chez les personnes grandes. IL faut donc le rapporter à la dimension
corporelle que l’on mesure de différentes façons.
La meilleure normalisation utilisée est de diviser le MR par P 0,75 qui représente la masse active du sujet
c’est-à-dire ce qui coûte de l’énergie au repos comme par exemple le diaphragme(pour la respiration) à la
différence du squelette qui est la masse inactive.
Actuellement, on prend préférentiellement la surface corporelle qui est quand même moins bon pour
l’homogénéisation.
SC est trouvée dans les abaques (document graphique) en fonction du sexe, de la taille, du poids. Pour un
adulte moyen jeune, la SC est de 1,73 m².
Chez un homme de 25 ans le MB est de 37 Cal/m²/h avec une SC de 1,73 m² 37 x 1,73 x 24 = 1540 Cal
c’est la dépense de fond qui est le coût de la vie.
Répartition du MB entre les différents organes
Poids en Kg
% relatif
% MB
Foie
1.5
2
27
Cerveau
1.5
2
19
Cœur
0.4
0.4
7
Reins
0.4
0.4
10
Muscles
44
18
Restes
51
19
1 gramme de cœur travaille 50 fois plus qu’un gramme de tissu adipeux.
Facteurs qui modifient ce MB
L’âge si on rapporte le MB sur la SC
A 25 ans MB = 37 Cal/m²/h
A 1ans MB = 53 Cal/m²/h coût énergétique de la croissance
A 70 ans MB = 34 il y a une transformation progressive de la masse active en masse inactive.
Sexe car le MB de la femme est plus faible de 10 % que celui de l’homme car la masse grasse
chez la femme est plus élevée. Ce chiffre de 1540 Cal/m²/h est une énergie nécessaire pour lever une
masse de 60 tonnes de 10 mètres.
Thermogenèse postprandiale TPP
C’est la quantité de chaleur dégagée en supplément par rapport à la dépense de fond (après les heures de
repas). Le MB augmente de 10% pendant 1 h30 après le repas.
Une première hypothèse dit que c’est du au travail de la digestion mais ce n’est pas tout car quand on injecte
directement les aliments dans le sang il y a quand même une augmentation de chaleur. La deuxième
hypothèse dit que c’est le coût du passage du jeun à une situation nourrit. Ces réorganisations coûtent de
l’énergie supplémentaire surtout au niveau du foie.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
1
/
15
100%