CP Blanpain Nature Cell Biology

Communiqué de presse
Bruxelles, le 25 août 2014
Publication dans la revue Nature Cell Biology (Advanced online publication in Nature
Cell Biology) : des chercheurs de l’Université libre de Bruxelles, ULB ont défini un
nouveau modèle de ségrégation précoce des progéniteurs cardiovasculaires au cours
du développement du cœur murin.
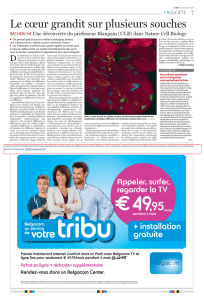
Le cœur est un organe formé de quatre chambres et de différents types cellulaires tels que
les cardiomyocytes, les cellules endothéliales couvrant la surface interne du cœur, les
cellules de l’épicarde constituant la couche supérieure du cœur et les cellules de muscle
lisse qui couvre les coronaires et les grands vaisseaux. Au cours du développement
embryonnaire, les cellules qui vont former le cœur doivent être spécifiées au bon moment,
migrer au bon endroit et proliférer pour garantir le développement harmonieux et une bonne
croissance du cœur. La moindre erreur lors de ces étapes critiques du développement
conduira à des malformations cardiaques congénitales qui représentent la première cause
de malformations sévères à la naissance. Différents progéniteurs, contribuant au
développement du cœur, ont déjà été identifiés. Cependant l’origine des cellules cardiaques,
à savoir si elles dérivent d’un progéniteur commun ou de distincts progéniteurs qui sont
spécifiés à différents moments du développement embryonnaire, reste encore méconnue.
Dans un article publié dans la revue Nature Cell Biology, une équipe de chercheurs dirigée
par le Pr. Cédric Blanpain, chercheur WELBIO au sein de l’Institut Interdisciplinaire en
Recherche Humaine et Moléculaire (IRIBHM, Faculté de Médecine), Université libre de
Bruxelles, Belgique, a identifié différents progéniteurs cardiovasculaires qui naissent à
des moments différents, se différencient dans des cellules cardiovasculaires
différentes et contribuent à la formation de différentes régions du cœur.
Fabienne Lescroart, Samira Chabab et leurs collègues ont effectué pour la première fois
une analyse clonale, temporellement contrôlée, des progéniteurs cardiovasculaires
précoces, dans laquelle ils ont marqué une cellule unique au cours du développement et
étudié leur contribution individuelle au cours du développement cardiaque. Contrairement à
la notion précédemment répandue que les cellules cardiaques proviennent de progéniteurs
cardiovasculaires communs, les chercheurs ont ici montré que ces progéniteurs n’avaient
pas d’ancêtre commun, mais étaient spécifiés indépendamment à différents moments du
développement et qui contribuent seulement à former certaines régions du cœur. Cette
nouvelle donnée suggère que le cœur est construit à partir de différents blocs formés à
différents moments du développement. De plus, les chercheurs ont démontré qu’au cours du
développement embryonnaire, la population des progéniteurs cardiaques la plus précoce
Département
Relations
Extérieures
Service Communication Recherche
Nancy Dath, T : +32 (0)2 650 92 03, +32 (0) 473 97 22 56
M : ndath@ulb.ac.be
Nathalie Gobbe, T : +32 (0)2 650 92 06, +32 (0)474 84 23 02
M : ngobbe@ulb.ac.be

n’est pas capable de se différencier dans plus d’un sous-type de cellules cardiovasculaires
(cellules cardiaques, endothéliales, épicardiques et cellules musculaires lisses),
contrairement à leur capacité de donner tous les sous types de cellules cardiovasculaires in
vitro. Ceci suggère que le destin final des progéniteurs cardiovasculaires pourrait être régulé
par des facteurs environnementaux que ces cellules rencontrent au cours de la
morphogénèse cardiaque. “Nous étions extrêmement surpris de découvrir que les
progéniteurs cardiovasculaires précoces avaient une contribution régionale aussi étroite et
n’étaient pas capable de se différentier en plus d’un type cellulaire comme le font les
progéniteurs cardiaques tardifs. Cela nous amène à repenser fondamentalement la manière
dont le coeur se forme” commente Fabienne Lescroart, la première auteur de cette étude.
A l’aide de nouveaux outils génétiques pour isoler pour la première fois les progéniteurs
cardiaques précoces au cours du développement embryonnaire, Fabienne Lescroart, Samira
Chabab et leurs collègues ont défini les caractéristiques moléculaires de ces différents
progéniteurs montrant que bien que très similaires moléculairement, ces progéniteurs
présentent aussi des différences notables, consistantes avec les régions du cœur et le(s)
type(s) de cellules cardiovasculaires qu’ils vont donner. De plus, la caractérisation
moléculaire de nombreuses cellules uniques a démontré que les progéniteurs cardiaques
étaient moléculairement hétérogènes et exprimaient différentes combinaisons de gènes qui
définiront le destin cellulaire de chaque progéniteur. Comprendre comment cette spécificité
est atteinte sera important pour instruire et/ou restreindre le destin des progéniteurs
cardiovasculaires multipotents dans un type cellulaire particulier in vivo. Les réponses à ces
questions seront importantes pour imaginer de nouvelles stratégies pour diriger la
différentiation des cellules souches embryonnaires (ESC) et des cellules pluripotentes
induites (iPS), directement en une population pure de cardiomyocytes qui permettra
d’améliorer la thérapie cellulaire des maladies cardiovasculaires.
En conclusion, ce travail dévoile comment le cœur est formé à partir de populations de
progéniteurs temporellement distincts qui vont former différentes régions du cœur et donner
différents types de cellules cariovasculaires. Ce travail fournit pour la première fois une
analyse clonale temporelle du développement cardiaque et la première analyse moléculaire
des progéniteurs cardiaques au cours des étapes très précoces du développement
cardiaque. “Cette nouvelle étude change réellement la manière dont nous voyons le
développement cardiaque et a des implications importantes pour mieux comprendre
l’étiologie des malformations cardiaques congénitales. Elle devrait être le point de départ de
futures études pour comprendre comment un progéniteur cardiovasculaire acquiert un destin
particulier et contribue à la formation d’une région particulière du cœur. Ceci pourrait ainsi
être applicable pour la thérapie cellulaire nécessaire pour la réparation cardiaque »
commente le professeur Cédric Blanpain, le directeur de ce travail.
Ce travail a été soutenu par le FNRS, la Fondation ULB, la Fondation contre le Cancer, le
Conseil Européen de la Recherche (ERC) et la Fondation Bettencourt Schueller (C.B. et
F.L.). Cédric Blanpain est un investigateur du WELBIO. Fabienne Lescroart a été
séquentiellement soutenue par le FNRS et un EMBO long-term fellowship. Samira Chabab
est soutenue par une bourse du FRS/FRIA.

La revue Nature Cell Biology demande que les journalistes la créditent comme source de
l’histoire couverte.
Fabienne Lescroart *, Samira Chabab *, Xionghui Lin, Steffen Rulands, Catherine Paulissen,
Annie Rodolosse, Herbert Auer, Younes Achouri, Christine Dubois, Antoine Bondue,
Benjamin D Simons and Cédric Blanpain. Early lineage restriction in temporally distinct
populations of Mesp1 progenitors during mammalian heart development. Nature Cell Biology
2014, DOI: 10.1038/ncb3024. * denotes equal contribution
Contacts scientifique:
Cédric Blanpain, MD, PhD
WELBIO, Interdisciplinary Research Institute (IRIBHM)
Université Libre de Bruxelles (ULB)
808, route de Lennik, BatC, C6-130
1070 Bruxelles, Belgium
Tel: +32-2-555 4175
Email: Cedric.Blanpain@ulb.ac.be
Lab Website: http://blanpainlab.ulb.ac.be/index.htm
PA Nathalie Moguet: [email protected]
1
/
3
100%