1
Travaux Pratiques
La photosynthèse :
Séparations physique et chimique des pigments végétaux
Pr Salama AISSAM

2
Généralités théoriques
Les végétaux pourvus de pigments chlorophylliens ont la propriété d’utiliser l’énergie
lumineuse pour réaliser la synthèse des glucides et d’autres constituants organiques à partir du
gaz carbonique atmosphérique et de l’eau.
L’équation globale de la photosynthèse est la suivante :
L’énergie lumineuse nécessaire à l’activité photosynthétique des végétaux verts est fixée dans
les chloroplastes par des substances colorées ou pigments qui appartiennent à 2 groupes
chimiques distincts.
Groupe des porphyrines :
Représenté par les chlorophylles de coloration verte et dont la molécule comporte un noyau
porphyrique constitué par 4 groupes pyrroliques unis entre eux et combinés à un atome de
magnésium. Ce noyau tétrapyrrolique porte 2 groupements carboxyliques estérifiés l’un par le
méthanol et l’autre par le phytol (alcool à longue chaîne C20H39OH)
- La chlorophylle a : Représente la forme universelle rencontrée chez tous les organismes qui
photosynthétisent. Elle possède un groupement méthyle (CH3) en position R sur le cycle du
noyau tétrapyrrolique.
La chlorophylle b : Diffère de la chl a par la présence d’un groupe (CHO) à la place de CH3.
Elle n’est rencontrée que chez les végétaux supérieurs et les algues vertes.

3
Structure des pigments (chlorophylles a et b)
Groupe des tétraterpènes
Appelés aussi caroténoïdes, de couleur jaune, sont constitués par les carotènes
(hydrocarbures) et les xanthophylles qui diffèrent des premiers par la présence d’oxygène
dans leur molécules.
Les chlorophylles et les caroténoïdes sont solubles dans les lipides et dans leurs solvants : ce
sont des pigments liposolubles. Les chlorophylles absorbent essentiellement la lumière rouge
et la lumière bleue. Les caroténoïdes absorbent les radiations bleues.
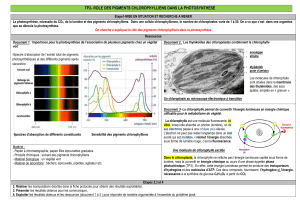
L’absorption de la lumière par un pigment varie suivant la longueur d’onde de la radiation
utilisée. La représentation graphique de l’absorption en fonction de la longueur d’onde
constitue le spectre d’absorption du pigment que l’on établit grâce à la technique de
spectrophotométrie.
Les formules de MAC KINNEY et BRUNSMA permettent de calculer les quantités de
chlorophylles a et b contenues dans une solution en utilisant des mesures de densités optiques
à différentes longueurs d’onde :

4
Ca = 12,7 x DO663 – 2,69 x DO645 (en mg/L)
Cb = 22,9 x DO645 – 4,68 x DO663 (en mg/L)
* Solvant des chlorophylles = Acétone 80%
Manipulations
I/ Extraction des pigments
- Dans un mortier, broyer 10g de feuilles vertes avec une pincée de sable de
Fontainebleau.
- Ajouter 20mL d’acétone et continuer le broyage durant 10min. Filtrer sur filtre
imprégné d’acétone en entraînant le moins possible de broyat.
- Réaliser une nouvelle extraction avec 20mL d’acétone et entraîner de nouveau l’extrait
sur le filtre.
- Faire une troisième extraction comme précédemment.
- Les 3 filtrats sont recueillis dans une ampoule à décanter qui contient alors un extrait
acétonique vert-foncé renfermant tous les pigments.
II/ Dosage des chlorophylles
Prélever 4mL de l’extrait acétonique auquel on ajoute 1mL d’eau distillée de façon à obtenir
une solution de chlorophylles dans l’acétone à 80%.
On mesure grâce au spectrophotomètre la densité optique aux 2 longueurs d’onde 645 et 663.
Une 1ère cuve de référence contient le solvant pur soit l’acétone à 80% et une 2ème cuve
contient la solution des pigments à doser.
Au cas où la solution serait trop concentrée, procéder à des dilutions dans des proportions
connues.
A l’aide des formules citées plus haut et en tenant compte des différents volumes obtenus,
calculer les quantités de chlorophylles contenues dans 1g de matière végétale fraîche.

5
III/ Séparation chimique des pigments
- Verser 75mL d’éther de pétrole dans l’ampoule à décanter contenant le reste de
l’extrait acétonique.
- Boucher et agiter l’ampoule renversée de façon continue, robinet ouvert, durant 5min
en évitant de créer des émulsions.
- Refermer le robinet, replacer l’ampoule sur son support et faire couler le long de la
paroi interne 50mL d’eau distillée.
- Agiter comme précédemment puis laisser décanter pendant 10min.
Deux phases alors se séparent :
La phase supérieure : Phase concentrée de couleur vert-foncé, contient les
chlorophylles, les carotènes et les xanthophylles dans l’éther de pétrole (A
conserver).
La phase inférieure : Jaune-verdâtre, dans l’acétone, sera éliminée (enlever le
bouchon de l’ampoule et ouvrir le robinet).
- Rincer 2 fois de suite la solution de pigments conservée, en ajoutant à chaque fois
dans l’ampoule 75mL d’eau distillée.
- On agite alors comme précédemment, on laisse reposer. On éliminera chaque fois la
phase inférieure.
La solution de pigments dans l’éther de pétrole est maintenant purifiée et peut être
utilisée pour une séparation chimique en suivant les étapes ci-dessous.
- Transvaser 50mL de la solution de pigments dans une nouvelle ampoule à décanter, y
ajouter 50mL d’alcool méthylique à 92%, agiter par un mouvement de rotation lent
mais régulier.
- Laisser reposer pendant 10min puis recueillir la phase inférieure, constituée par la
chlorophylle b et les xanthophylles en solution méthanolique dans un bécher.
La phase supérieure renferme chlorophylle a et les carotènes en solution dans
l’éther de pétrole.
- Ajouter alors dans l’ampoule 25mL d’une solution fraîchement préparée d’alcool
méthylique ayant 30% de potasse. Effectuer le mélange à la solution de pigments par
un mouvement de rotation régulier.
 6
6
 7
7
 8
8
1
/
8
100%