Dochead fiche
Sous-dochead physiologie
Les reins
Flavien Bessaguet
Docteur en neurosciences
Alexis Desmoulière*
Professeur des universités
Faculté de pharmacie, 2 rue du Docteur-Marcland, 87025 Limoges cedex, France
*Auteur correspondant.
Adresse e-mail : alexis.des[email protected] (A. Desmoulière).
Résumé
Les reins, qui appartiennent au système urinaire, permettent d’éliminer les métabolites toxiques
issus du catabolisme. Par ailleurs, ils jouent un rôle fondamental dans le maintien de l’homéostasie
hydro-électrolytique du milieu intérieur. Enfin, ils ont une fonction endocrine dans l’érythropoïèse et
la synthèse de vitamine D active.
© 2020
Mots clés – endocrinologie ; homéostasie ; néphron ; physiologie ; rein
Pas de summary et keywords dans les fiches. Merci
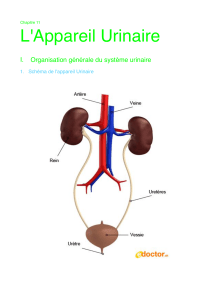
Les reins sont localisés au sein du rétropéritoine, dans la partie postérieure de la cavité abdominale,
de part et d’autre de la colonne vertébrale. Le rein gauche est situé plus haut que le rein droit. Chez
l’adulte, ils mesurent environ 12 cm de hauteur, 6 cm de largeur et 4 cm d’épaisseur [1]. Chaque rein
est surmonté d’une glande surrénale présentant une activité endocrine fondamentale permettant
notamment la synthèse d’adrénaline ou d’aldostérone. Le bord interne situé face à la colonne
vertébrale présente une cavité appelée sinus rénal dans laquelle passent les vaisseaux sanguins, les
nerfs et l’uretère [1]. Ces différents éléments sortent du rein par le hile rénal (figure 1).
© 2020 published by Elsevier. This manuscript is made available under the Elsevier user license
https://www.elsevier.com/open-access/userlicense/1.0/
Version of Record: https://www.sciencedirect.com/science/article/pii/S0515370020300707
Manuscript_92261b4c335dbe30eafda85d33c6726c

La vascularisation rénale est importante puisque 20 à 25 % du débit cardiaque au repos sont
consacrés à la perfusion rénale, soit plus de 1 L/min [2]. L’artère rénale est issue directement de
l’aorte et pénètre dans le rein par le sinus et le hile rénal. Plusieurs ramifications successives
permettent la formation d’artérioles afférentes qui irriguent les glomérules et favorisent la filtration
glomérulaire. Le retour veineux se fait par les veines du tissu rénal qui se regroupent et forment la
veine rénale qui rejoint directement la veine cave inférieure [1].
L’innervation rénale est originale car elle présente exclusivement des afférences sympathiques qui
modulent le tonus vasculaire et la sécrétion de rénine [1].
Le rein est divisé en deux : le cortex rénal est la partie la plus superficielle, sous la capsule fibreuse
qui l’entoure, contenant principalement les glomérules et les tubes contournés proximaux et
distaux ; la médulla correspond à la zone située plus en profondeur qui rassemble en grande majorité
les anses ascendantes et descendantes de Henlé ainsi que les tubes collecteurs (figure 2) [1].
L’ensemble des tubes collecteurs se réunissent au niveau du bassinet pour former l’uretère
(figure 1).
T1 Le néphron
Le nombre total de néphrons présents dans chaque rein varie entre 800 000 et 1,5 million [1].
Chaque néphron est composé d’un glomérule, d’un tube contourné proximal, d’une anse de Henlé,
d’un tube contourné distal et d’un tube collecteur (figure 2). Il s’agit donc de l’unité fonctionnelle du
rein. L’urine définitive est formée par des phénomènes de réabsorption et de sécrétion sous le
contrôle de médiateurs systémiques et locaux.
T2 Le glomérule
Le glomérule constitue, avec la capsule de Bowman, le corpuscule rénal de Malpighi [2].
Il correspond anatomiquement à une ramification vasculaire issue de l’artériole afférente. C’est le
siège de l’ultrafiltration plasmatique et de la formation de l’urine primitive. Ces petits capillaires se
regroupent ensuite et forment l’artériole efférente qui sort de la capsule de Bowman.
T3 Anatomie
Trois éléments sont présents au niveau de la membrane glomérulaire et sont garants de la filtration
glomérulaire : les cellules endothéliales vasculaires, la membrane basale et les podocytes. Ces
derniers sont des cellules épithéliales spécialisées qui émettent des prolongements appelés
pédicelles limitant le passage des grosses molécules dans l’urine primitive [1]. À la sortie du
glomérule, cette dernière présente une composition presque identique à celle du plasma, à
l’exception des macromolécules (poids moléculaire égal ou supérieur à 68 000 Da) qui ne passent pas
la barrière glomérulaire.

T3 Débit de filtration glomérulaire
Le débit de filtration glomérulaire (DFG) est un indicateur majeur du bon fonctionnement rénal et
permet généralement de poser un premier diagnostic d’insuffisance rénale aiguë ou chronique [3].
Le DFG correspond à un volume de liquide filtré au niveau du glomérule par unité de temps [4]. Il est
généralement rapporté chez l’adulte à une surface corporelle moyenne de 1,73 m
2
. Un DFG
physiologique est compris entre 110 et 130 mL/min/1,73 m
2
à 30 ans, puis diminue progressivement
avec l’âge [5].
Le DFG dépend de plusieurs facteurs physiques qui sont l’apport sanguin rénal, la perméabilité et la
surface du glomérule, ainsi que les pressions présentes de part et d’autre du filtre glomérulaire.
L’apport sanguin est modulé finement par un jeu de vasoconstriction-vasodilatation au niveau des
artérioles afférentes et efférentes. Une vasodilatation de l’artériole afférente ou une
vasoconstriction de l’artériole efférente augmente le DFG. Le volume d’ultrafiltrat produit par jour
est d’environ 180 L, mais la quantité d’urine totale émise quotidiennement est comprise entre 1 et
2 L/jour [4]. Des mécanismes de réabsorption sont donc présents au niveau tubulaire.
T2 Le tube contourné proximal
Le tube contourné proximal (TCP) succède directement au glomérule. Au niveau histologique, il est
composé d’une monocouche de cellules épithéliales reposant sur une lame basale [1]. C’est dans
cette partie du néphron que 67 % de l’eau et du chlorure de sodium (NaCl) sont réabsorbés,
entraînant la réabsorption d’autres molécules nécessaires pour l’organisme.
T3 Réabsorption du glucose et des protéines
Le glucose est totalement réabsorbé dans le TCP. Un cotransporteur
1
(ou symport) sodium/glucose
(Na
+
/glucose) permet la réabsorption avec le Na
+
du glucose puisque le gradient électrochimique du
Na
+
est favorable. De la même manière, un symport Na
+
/acide aminé participe à la réabsorption des
acides aminés et des protéines [1]. En conditions physiologiques, le glucose et les protéines ne sont
donc pas présents dans l’urine définitive.
T3 Réabsorption de l’eau et des électrolytes
La plupart des ions comme le Na
+
, le potassium (K
+
), les bicarbonates (HCO
3-
), le chlore (Cl
-
) et le
calcium (Ca
2+
) sont réabsorbés en grande quantité (75 à 85 %) dans le TCP. Le Na
+
est réabsorbé et les
protons sont sécrétés par un antiport Na
+
/H
+
. Les protons proviennent d’un mécanisme mettant en
jeu l’anhydrase carbonique intracellulaire qui hydrolyse le H
2
CO
3
en H
+
et HCO
3-
. Cette sécrétion de
H
+
induit la réabsorption des bicarbonates [1].
L’anhydrase carbonique peut être inhibée pharmacologiquement par l’acétazolamide qui est indiqué
dans la prise en charge de certaines alcaloses métaboliques notamment (figure 2).

T3 Sécrétion des H
+
et NH
4+
Bien qu’il s’agisse d’une zone fondamentale pour la réabsorption, une sécrétion importante de H
+
est
également observée. La production des protons est liée à l’activité de l’anhydrase carbonique.
Par ailleurs, la présence d’une glutaminase dans le TCP induit la formation de glutamine puis
d’ammoniac (NH
3
) qui peut se lier à 1 H
+
pour former l’ion ammonium (NH
4+
) sécrété dans la lumière
tubulaire [1].
L’élimination de nombreux médicaments a lieu au niveau du TCP. Chez l’insuffisant rénal, cette
élimination est diminuée et nécessite donc des adaptations posologiques et/ou l’augmentation de la
fréquence des prises médicamenteuses.
T2 L’anse de Henlé
L’anse de Henlé est une structure en forme d’épingle à cheveux, qui présente une branche
descendante et une branche ascendante. Cette partie du néphron est le moteur de la concentration
des urines par un jeu subtil entre la réabsorption d’eau et de NaCl [6].
T3 L’anse de Henlé descendante
La branche descendante de l’anse de Henlé (BDAH) est très perméable à l’eau et très peu aux
solutés, ce qui favorise la concentration de l’urine au fur et à mesure qu’elle s’enfonce dans l’anse de
Henlé par réabsorption massive d’eau. L’urine devient alors hypertonique par rapport au plasma [6].
Néanmoins, cette réabsorption d’eau nécessite la réabsorption préalable de NaCl dans la branche
ascendante de l’anse de Henlé (BAAH).
T3 L’anse de Henlé ascendante
La BAAH est perméable aux solutés et quasiment imperméable à l’eau. L’urine étant très
hypertonique en arrivant dans la BAAH, cela entraîne la réabsorption des ions comme le Na
+
, le K
+
et
le Cl
-
par l’intermédiaire d’un symport Na
+
/K
+
/2Cl
-
. La réabsorption active de Na
+
dans le tissu
interstitiel (ou interstitium) entourant l’anse de Henlé est très importante au début de la BAAH avant
de diminuer progressivement, formant un gradient cortico-médullaire. Ce gradient favorise la
réabsorption passive d’eau dans la BDAH par osmolarité et rend l’urine hypertonique au fond de
l’anse : il est question de multiplication à contre-courant [7]. Comme il existe toujours un léger
décalage entre la concentration de l’urine et celle de l’interstitium, le gradient se renforce
progressivement. La réabsorption des solutés est tellement importante dans la BAAH que l’urine se
trouve hypotonique par rapport au plasma dans les premiers segments du tube contourné
distal (TCD).
Les diurétiques dits de l’anse, comme le furosémide, sont des inhibiteurs du symport Na
+
/K
+
/2Cl
-
.
Ils empêchent la réabsorption du Na
+
et, indirectement, celle de l’eau. Ces diurétiques sont très
puissants et d’action rapide. Ils sont indiqués dans la prise en charge en urgence des œdèmes aigus

du poumon par voie intraveineuse ou de l’hypertension artérielle (HTA) (par voie orale à libération
prolongée) (figure 2).
T2 Le tube contourné distal
Le TCD permet une réabsorption supplémentaire de Na
+
d’environ 5 %. Cette quantité est donc
nettement inférieure à celle observée dans le TCP ou l’anse de Henlé. Néanmoins, cela favorise une
régulation très fine de l’homéostasie sodique. Le Na
+
, le K
+
et le Ca
2+
sont réabsorbés au niveau des
cellules dites principales. La réabsorption du Na
+
est possible grâce à un cotransport Na
+
/Cl
-
et à des
canaux sodiques spécifiques [1]. Le Ca
2+
est réabsorbé via des canaux calciques spécifiques appelés
transient receptor potential vanilloid de type 5 (TRPV5) [6]. D’autres cellules, les cellules intercalaires
A et B, sont responsables de la régulation du pH par ajustement de l’équilibre entre les H
+
et les
HCO
3-
. Les cellules de type A sont actives, surtout en acidose en éliminant les protons, et les cellules
de type B fonctionnent surtout en alcalose pour éliminer les bicarbonates [1].
L’utilisation de diurétiques agissant sur cette partie du néphron (diurétiques thiazidiques
principalement) présente de nombreux avantages puisque l’effet natriurétique et diurétique est
moins puissant mais rapide. Ils sont donc plutôt administrés en traitement de fond de l’HTA et de
l’insuffisance cardiaque congestive (figure 2).
T2 Le tube collecteur
Le tube collecteur (TC) est la partie la plus distale du néphron. Il permet l’ajustement final de la
concentration en Na
+
et en K
+
notamment, et du pH de l’urine définitive. Les cellules rencontrées
dans cette partie du néphron sont les mêmes que dans le TCD (cellules principales et cellules
intercalaires A et B). Cependant, contrairement aux autres parties du néphron, les mécanismes de
réabsorption et de sécrétion sont ici principalement sous contrôle hormonal. Ces différents types
cellulaires expriment donc les récepteurs aux différentes hormones impliquées dans les régulations
hydrique et électrolytique [1].
La réabsorption d’eau est modulée finement par le système multiplicateur à contre-courant, mais se
trouve également sous le contrôle de l’hormone antidiurétique (ADH). Cette hormone
hypothalamique stimule la synthèse et l’adressage membranaire de canaux perméables à l’eau
appelés aquaporines. La synthèse d’ADH est liée à l’osmolarité du plasma et à la volémie [4].
La réabsorption du Na
+
et la sécrétion du K
+
sont directement modulées par l’aldostérone qui fait
partie des hormones minéralocorticoïdes synthétisées dans la partie corticale des glandes surrénales.
L’aldostérone stimule la synthèse et augmente la conductance d’un canal sodique spécifique appelé
canal épithélial sodique (ENaC). Cette entrée massive de sodium augmente le gradient
électrochimique cellulaire qui favorise la sécrétion de K
+
[1].
La régulation du pH de l’urine se réalise essentiellement par sécrétion de H
+
, soit sous forme libre
(le pH urinaire est acide), soit sous forme de NH
4+
ou complexé aux phosphates.
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%