CTM_Chapitre 7 TP 1
Comment synthétiser le paracétamol ? Avec quel rendement ?
L’utilisation clinique du paracétamol (contraction de para-acétyl-amino-phénol) date de 1893.
Le paracétamol est un composé organique ayant une activité analgésique et antipyrétique d'intensité
comparable à celle de l'aspirine mais qui n’a pratiquement pas d'effet sur l'inflammation. Il n'a pas les
effets secondaires de l'aspirine.
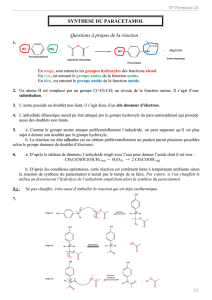
La synthèse du paracétamol est réalisée par réaction de l'anhydride éthanoïque sur le 4-aminophénol
Cette réaction, exothermique, produit également de l'acide éthanoïque :
Données physicochimiques
Composé
4-aminophénol
anhydride
éthanoïque
paracétamol
acide éthanoïque
(acide acétique)
Formule
brute
C6H7NO
C4H6O3
C8H9NO2
CH3COOH
Aspect à 25
°C et 1 bar
solide blanc
liquide incolore
(densité : 1,08)
solide blanc
liquide incolore
Pictogramme
s de danger
Solubilité
dans l’eau
peu soluble
dans l’eau
réagit avec l’eau (en
donnant l’acide dont
il est issu)
10 g.L-1 à 20°C
250 g.L-1 à 100°C
très grande
solubilité de 0°
C à 100°C
Température
s de
changement
d’état
θfusion = 186 °C
θfusion = -73 °C
θéb = 136 °C
θfusion = 168 °C
θfusion = 17 °C
Masse
molaire
109,2 g.mol-1
102,9 g.mol-1
151,2 g.mol-1
60,1 g.mol-1
Réflexions préliminaires
1. Entourer dans l’équation de la réaction de synthèse du paracétamol, les groupes caractéristiques
justifiant la terminaison -ol du 4-aminophénol et du paracétamol. Rappeler le nom de ce groupe
caractéristique. …………………………………………………………………………………………………………..………………
2. Donner l’état physique (à 25 °C et sous 1 bar) des réactifs utilisés lors de la synthèse du paracétamol.
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
3. Observer les pictogrammes des réactifs utilisés Rechercher les risques inhérents à leur
manipulation. S’organiser en conséquence. …………………………………………………….
…………………………………………………………………………………………………………………………………………………….

Protocole expérimental
Etape 1
1. Préparer un bain marie à 80 °C environ, à l’aide
d’un récipient en verre rempli à moitié d’eau et
de l’agitateur magnétique chauffant.
2. Dans un erlenmeyer propre et sec, peser une
masse m = 2,7 g de para-aminophénol
3. Ajouter 20 mL de solution d’acide éthanoïque à
2 mol.L-1 à l’aide d’une éprouvette graduée.
4. Ajouter le turbulent et adapter le réfrigérant à
air.
5. Chauffer au bain-marie 10 min à 80 °C, tout en
agitant jusqu’à dissolution complète du para-
aminophénol.
6. Sortir l’erlenmeyer du bain marie et refroidir le
mélange (à 40 °C environ) en le plaçant sous un
courant d’eau froide.
7. Apporter l’erlenmeyer sous la hotte puis
ajouter lentement et en agitant, 3,5 mL
d’anhydride éthanoïque (0,5 mL par 0,5 mL), à
l’aide d’une pompe doseuse.
8. Remettre au bain-marie 10 min à 60°C en agitant.
Etape 2
1. Refroidir le mélange en plaçant l’erlenmeyer dans un
bain d’eau glacée et attendre la cristallisation.
2. Avec précaution, frotter le fond de l’erlenmeyer avec une
baguette en verre pour déclencher la cristallisation.
3. Lorsque la cristallisation est terminée, filtrer sous vide
sur Büchner.
4. Rincer les cristaux avec un peu
d’eau glacée.
Etape 3
1. Transvaser les cristaux de paracétamol « brut » (avec le barreau aimanté) dans l’erlenmeyer rincé.
2. Ajouter, petit à petit, lentement, environ 20 mL d'eau bouillante à l’aide d’une éprouvette graduée.
3. Poser l’erlenmeyer sur la plaque chauffante et maintenir à ébullition, tout en agitant.
4. Si la redissolution n'est pas totale, ajouter encore 5 mL d'eau bouillante.
5.
Refroidir doucement : d’abord à l’air, puis en faisant couler de l’eau sur l’extérieur de l’erlenmeyer, puis
en
le plaçant dans un bain d’eau glacée, jusqu’à la cristallisation totale du paracétamol. Filtrer sur
Büchner, rincer avec un peu d’eau glacée.
6. Filtrer à nouveau sur Büchner.
7. Sécher les cristaux entre deux feuilles de papier filtre ou les placer à l’étuve.
Etape 4
1.
Mesurer et noter la masse de cristaux obtenus. …………..………………
2.
Mesurer et noter leur température de fusion à l’aide d’un banc Köfler. ………………………………
Montage expérimental

Commentaires sur la mise en œuvre du protocole
Etape 1 :
* Compléter les légendes du schéma.
* Quel est le rôle du réfrigérant à air ?
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
* Quel est le rôle de l’acide éthanoïque ?
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
* Pourquoi chauffe-t-on le mélange après l’ajout d’acide éthanoïque ?
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
* Justifier l’ajout lent d’anhydride éthanoïque au mélange acide acétique-4-aminophénol. Quelles
autres précautions ont été prises ?.......................................................................................................................................
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
Etape 2 :
* Comment élimine-t-on l’excès d’anhydride éthanoïque en fin de réaction ?
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
* Justifier le refroidissement du mélange réactionnel.
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
* Après la filtration, pourquoi faut-il laver les cristaux à l’eau ? Pourquoi avec un minimum d’eau ?
Pourquoi de l’eau glacée ? …………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
Etape 3 :
On dissout les cristaux bruts de paracétamol dans un solvant tel que :
-
à chaud : le paracétamol et les impuretés sont solubles dans ce solvant.
-
à froid : le paracétamol est insoluble dans ce solvant tandis que les impuretés le sont.
* Quel est le solvant utilisé ?
…………………………………………………………………………………………………………………………………………………….
* En déduire l’intérêt de cette étape.
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….

Etape 4 :
* Calculer la masse maximale de paracétamol que l’on peut espérer obtenir lors de cette synthèse.
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
* La comparer à celle obtenue expérimentalement et en déduire le rendement r de la synthèse.
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
* Comparer la température de fusion du produit obtenu à celle du paracétamol.
…………………………………………………………………………………………………………………………………………………….
* Conclure sur la pureté du produit obtenu.
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
Questions complémentaires
* Associer à chaque étape du protocole, un titre parmi ceux proposés dans la liste suivante (attention,
tous les noms ne serviront pas) :
Distillation ; Purification ; Synthèse ; Analyse ; Isolation ; Décantation
* Rappeler la verrerie utilisée pour mesurer : 20 mL d’eau et 20 mL d’acide éthanoïque ; 3,5 mL
d’anhydride éthanoïque. Justifier ces choix.
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
* Proposer au moins deux autres méthodes qui auraient pu permettre de de vérifier la pureté du
produit synthétisé. ………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
Données complémentaires
Spectre IR du paracétamol Spectre IR du para-aminophénol
WAVENUMBER (cm-1)
WAVENUMBER (cm-1)
TRANSMITTANCE
TRANSMITTANCE
1
/
4
100%