Place et résultats de l`efficacité clinique du contenseur cardiaque

ARTICLE ORIGINAL
Place et résultats de l’efficacité clinique du contenseur cardiaque
CorCap
®
dans le traitement de l’insuffisance cardiaque chronique
Clinical evaluation of the CorCap
®
cardiac support device in patients with progressive heart failure
C. BAUDET DROUILLARD
1
*, V. PHILIP
1
, L. LABROUSSE
2
1
Pharmacie des dispositifs médicaux stériles, Hôpital Haut Lévèque, avenue de Magellan, 33604 Pessac
2
Bloc chirurgie cardiaque, Hôpital Haut Lévèque, avenue de Magellan, 33604 Pessac
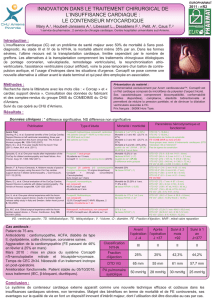
Résumé
.Le dispositif CorCap
®
est un contenseur passif permanent placé autour du ventricule gauche, destiné à
diminuer la tension pariétale et à redonner au cœur dilaté sa forme elliptique initiale chez des patients atteints
d’insuffisance cardiaque progressive. Il a pour but de limiter la dilatation ventriculaire gauche et de maintenir voire
d’améliorer la fonction cardiaque du patient. C’est un filet biocompatible en polyester présentant un aspect tricoté et
une conformabilité bidirectionnelle. Il est indiqué chez les patients adultes (18 ans ou plus) présentant une insuffisance
cardiaque chronique de classe III ou IV (NYHA) associée à une dilatation ventriculaire gauche et sous traitement
médical stable et optimal. Au CHU de Bordeaux, 43 patients ont bénéficié de la pose du contenseur CorCap
®
entre
juin 2002 et mai 2006. Les patients opérés présentaient une moyenne d’âge de 56 ± 11 ans avec une insuffisance
cardiaque datant de 4 ± 2 ans. La majorité des patients était en classe III (NYHA) et présentaient tous une diminution
de la fraction d’éjection ventriculaire gauche (24 ± 6 %). Au cours de la période de suivi (17 ± 5 mois), il a été recensé
cinq décès précoces soit au cours de l’hospitalisation soit dans les 30 jours qui ont suivi l’intervention et quatre décès
plus tardifs (> 3 mois). Chez tous les autres patients, il a été observé une amélioration des paramètres hémodynami-
ques, une amélioration de la classe NYHA et une amélioration de la qualité de vie des patients. Au vu de ces résultats,
il apparaît que la mise en place du contenseur CorCap
®
présente un risque opératoire modéré et des bénéfices en
terme de morbi-mortalité très encourageants. Les résultats à plus long terme permettront de positionner ce filet en
thérapeutique complémentaire et/ou alternative aux traitements usuels de l’insuffisance cardiaque chronique.
Mots clés :
contenseur cardiaque, CorCap
®
, insuffisance cardiaque chronique, dilatation ventriculaire, fraction
d’éjection ventriculaire gauche
Abstract
.The CorCap
®
Cardiac Support Device (CSD) is a passive permanent containment device placed around the
heart in order to decrease the wall stress, and reshape the dilated heart from a spherical to a more ellipsoidal shape in
patients with progressive heart failure. Its aim is to reduce the left ventricular dilatation, and optimize and/or improve
cardiac function. This device is made of biocompatible mesh-like polyester fabric with a knit construction and a
bidirectional compliance. Appropriate patients for CSD implantation are adults (18 years and over) with chronic
systolic heart failure of ischemic or idiopathic cause, with left ventricular dilatation, NYHA Class III or IV, under
permanent and optimal medical treatment. Between June 2002 and May 2006, 43 patients underwent implantations
of a CSD at the Bordeaux Heart University Hospital. Mean age of these patients at the time of operation was 56 ± 11
years (yrs), with an history of heart failure dating from 4 ± 2 yrs. The majority of these patients were NYHA Class III,
and all of them had a severely decreased left ventricular ejection fraction (mean 24 ± 4%). There were five early deaths
attributed to operative mortality having taken place during the first 30 days after surgery, or during the initial
hospitalization, and 4 late deaths over 3 months during the follow-up of 17 ± 5 months. In all survivors, hemodynami-
cal parameters improved, as well as the NYHA Class and the Quality of Life. Consequently, it appeared that the CSD
implantation involved a moderate operative risk, and that the benefits in terms of morbi-mortality were promising.
Longer-term results are needed which only will allow to define the interest of this device as a complementary or
alternative therapy to the current usual methods of treatment of the chronic heart failure.
Key words:
containment device, CorCap
®
, progressive heart failure, ventricular dilatation, left ventricular ejection
fraction
*Correspondance et tirés à part : C. Baudet Drouillard
ORIGINAL ARTICLE
J Pharm Clin 2007 ; 26 (2) : 123-30
J Pharm Clin, vol. 26, n° 2, juin 2007 123
doi: 10.1684/jpc.2007.0057
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

L’insuffisance cardiaque est un problème majeur de
santé publique. Malgré les nombreux progrès réa-
lisés dans la prise en charge médicamenteuse, la
morbidité et la mortalité restent encore élevées. On estime
que cette pathologie touche actuellement 500 000 à
1 000 000 de personnes en France et est à l’origine de
près de 30 000 décès chaque année. Les formes sévères
de la maladie (stade III et IV de la classification de la
NYHA) représenteraient environ 10 % de cette popula-
tion, soit 50 000 à 100 000 patients dont les deux tiers
sont âgés de plus de 70 ans.
Grâce aux mesures de prévention hygiéno-diététiques et
aux progrès thérapeutiques, le taux de mortalité par
insuffisance cardiaque a continuellement diminué ces 30
dernières années dans les pays occidentaux ; cependant
50 à 75 % des patients à un stade avancé de la maladie
décèdent dans les 5 ans qui suivent l’apparition des
premiers signes d’insuffisance cardiaque soit du fait de
son aggravation, soit par mort subite.
L'insuffisance cardiaque
L’insuffisance cardiaque [1-3] se définit comme l’incapa-
cité du cœur à assurer le débit sanguin nécessaire aux
besoins métaboliques et fonctionnels des différents orga-
nes (cerveau, reins et tissus musculaires périphériques).
Pour adapter au mieux le traitement de l’insuffisance
cardiaque et apprécier son efficacité, l’état fonctionnel
des malades doit être évalué en fonction d’une classifica-
tion, dont la plus utilisée est celle de la New York Heart
Association (NYHA).
Elle repose sur l’appréciation de la capacité du patient à
assurer une activité physique par rapport à sa propre
capacité physique avant le début de la maladie, ou à la
capacité considérée comme habituelle pour un individu
du même âge, du même sexe et de corpulence identique.
Un interrogatoire précis permet en général d’apprécier le
statut fonctionnel du malade par référence aux définitions
des 4 classes de la NYHA (figure 1).
Signes cliniques-diagnostic
Le diagnostic d’insuffisance cardiaque [1-4] repose sur la
mise en évidence de signes cardio-respiratoires et la
mesure de paramètres échocardiographiques.
L’auscultation cardiaque et respiratoire montre en
général :
– une dyspnée d’effort qui survient pour des efforts impor-
tants dans un premier temps puis pour des efforts de plus
en plus réduits au fur et à mesure de l’évolution de la
maladie avec un risque d’œdème aigu du poumon ;
– une dyspnée de décubitus ;
– des œdèmes au niveau des membres inférieurs ;
– un bruit de galop à l’auscultation cardiaque.
L’échocardiographie permet d’évaluer la taille, la fonction
ventriculaire gauche, le niveau des pressions de remplis-
sage et les pressions pulmonaires. Les principaux paramè-
tres échocardiographiques évalués sont :
– la fraction d’éjection ventriculaire gauche (FEVG) : c’est
un facteur pronostique majeur évalué de façon stable et
répétitive en échocardiographie. La relation entre FEVG et
mortalité est largement démontrée dans l’insuffisance car-
diaque. En cas d’insuffisance cardiaque prononcée la
FEVG est inférieure à la normale (67±8%);
– la mesure du volume télédiastolique ventriculaire gau-
che dont la valeur est largement supérieure à la normale
en cas d’insuffisance cardiaque (55 ± 10 mL/m
2
).
Deux tests complémentaires peuvent confirmer le diagnos-
tic d’insuffisance cardiaque : le test de marche pendant
6 minutes (distance parcourue < 500 m en cas d’insuffi-
sance cardiaque) et l’épreuve d’effort avec mesure
conjointe des gaz respiratoires (VO
2
max<75% des
valeurs théoriques rapportées au poids, au sexe et à l’âge
en cas d’insuffisance cardiaque).
Évolution et pronostic
Le pronostic de l’insuffisance cardiaque [1-4] est étroite-
ment lié au degré de sévérité de la maladie. Les patients
en classe IV de la NYHA ont un très mauvais pronostic à
court terme à l’opposé des patients asymptomatiques en
classe I. La mortalité des patients en classe II à III de la
NYHA est de l’ordre de 10 à 12 % par an, alors que celle
des patients en classe III à IV de la NYHA est de l’ordre de
35 %.
En cas d’insuffisance cardiaque aiguë, l’évolution tend
vers un œdème aigu du poumon qui peut s’associer à un
choc cardiogénique. L’évolution est le plus souvent rapide-
ment mortelle si on n’utilise pas des techniques de sup-
pléance (assistance circulatoire, transplantation ou cor-
rection chirurgicale de la fuite valvulaire). En cas
d’insuffisance cardiaque chronique, l’évolution se fait par
poussées, pouvant être signalées par une recrudescence
de la dyspnée d’effort ou par des accidents de dyspnée de
décubitus. Les complications pouvant survenir sont des
infections pulmonaires pouvant provoquer un œdème
pulmonaire, des accidents thrombo-emboliques veineux
ou artériels, des troubles du rythme tels qu’une fibrillation
auriculaire ou une mort subite par fibrillation ventriculaire.
Le passage en insuffisance cardiaque globale est une
modalité évolutive fréquente [5].
Traitements conventionnels
de l'insuffisance cardiaque chronique
La prise en charge thérapeutique de l’insuffisance cardia-
que chronique [4, 6] s’est considérablement améliorée
ces dernières décennies, notamment avec le développe-
ment de nouvelles techniques chirurgicales qui ont permis
d’améliorer l’espérance de vie des patients. Cependant,
un certain nombre de patients échappe aux traitements
conventionnels ou n’y répond pas.
Classification de la NYHA
Patient porteur d’une cardiopathie mais sans
aucune réduction de l’activité physique.
Légère limitation de l’activité physique.
Aucune gêne au repos mais l’activité quotidienne
ordinaire entraîne une fatigue, une dyspnée
ou des palpitations.
Limitation marquée des activités physiques.
Il n’y a pas de gêne au repos mais une activité
moins importante qu’à l’accoutumée provoque
des symptômes.
Classe I
Classe II
Classe III
Classe IV
Impossibilité de poursuivre une activité sans
gêne : les symptômes de l’insuffisance cardiaque
sont présents, même au repos, et la gêne est
accrue par toute activité physique.
Figure 1. Classification de la NYHA.
C. Baudet Drouillard, et al.
J Pharm Clin, vol. 26, n° 2, juin 2007
124
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Le traitement médicamenteux représente la thérapeutique
majeure au long cours de l’insuffisance cardiaque chroni-
que. Il a pour but d’améliorer la symptomatologie et de
limiter l’évolution de la maladie. Il est basé sur l’inactiva-
tion des systèmes de compensation neuro-hormonaux
responsables de l’aggravation de l’insuffisance cardia-
que. Actuellement, quatre grandes classes de médica-
ments ont leur place dans le traitement de l’insuffisance
cardiaque chronique : les diurétiques, les inhibiteurs de
l’enzyme de conversion (IEC), les bêtabloquants et les
antialdostérones. Ils permettent de réduire le nombre
d’hospitalisations et de réduire la mortalité.
En cas d’échappement au traitement médicamenteux ou
d’aggravation sous traitement, l’ultime recours reste la
transplantation cardiaque. Bien qu’elle représente le
meilleur traitement actuel (50 % de survie à 15 ans), elle
présente cependant de nombreuses limites, liées au man-
que de greffons (300 par an en France) et aux effets
indésirables qu’elle engendre.
Les alternatives thérapeutiques au traitement médicamen-
teux et à la transplantation cardiaque ont pour but d’amé-
liorer l’état clinique du patient et de retarder la transplan-
tation voire même de la suppléer. L’insuffisance cardiaque
est généralement le stade évolutif terminal d’une affection
valvulaire, coronaire, myocardique voire congénitale ou
acquise. Les interventions chirurgicales telles que la revas-
cularisation (pontage coronarien), le remodelage ventri-
culaire ou les valvuloplasties (réparation ou remplacement
valvulaire) permettent dans un premier temps de traiter la
ou les lésions causales de l’insuffisance cardiaque et de
ralentir son évolution.
La resynchronisation atrio-biventriculaire (stimulateur tri-
ple chambre) est une technique assez complexe nécessi-
tant une équipe médicale spécialisée et des locaux adap-
tés. L’une des voies d’avenir semble être l’association d’un
stimulateur triple chambre à un défibrillateur automatique
implantable pour pallier le risque de mort subite. Elle est
indiquée pour les patients en classe III ou IV de la NYHA
présentant un asynchronisme de contraction intraventricu-
laire ou une désynchronisation entre les deux ventricules
[6-8].
L’assistance mono- ou biventriculaire trouve sa place pour
les patients en stade terminal de l’insuffisance cardiaque
(classe IV de la NYHA) en attente ou en remplacement
d’une transplantation cardiaque. L’évolution tend vers des
systèmes totalement implantables facilitant ainsi le retour
à domicile et la reprise d’une activité quotidienne [8-10].
Nous avons ici choisi d’étudier une technique chirurgicale
basée sur la mise en place d’un dispositif de contention
passive : le contenseur cardiaque CorCap
®
et qui se pose
en alternative thérapeutique chez les patients en classe II
sévère, III ou IV de la NYHA, en association ou non à une
resynchronisation cardiaque ou une chirurgie mitrale.
Étude de l'efficacité clinique du CorCap®
au CHU de Bordeaux
Présentation du dispositif- base théorique
L’insuffisance cardiaque est un phénomène progressif
aboutissant à un remodelage ventriculaire qui inclut une
dilatation du cœur qui d’une forme elliptique devient
sphérique en s’élargissant. Il est associé à une augmenta-
tion de la tension pariétale.
Le contenseur cardiaque CorCap
®
est un implant perma-
nent placé autour du ventricule destiné à limiter la dilata-
tion ventriculaire associée à l’insuffisance cardiaque pro-
gressive. Cette action semble s’associer à une
amélioration de la fonction cardiaque (figure 2) [8, 11] .
Les traitements médicamenteux, tels que les bêtabloquants
et les inhibiteurs de l’enzyme de conversion agissent
essentiellement sur cette voie neurohormonale, mais ne
parviennent pas à stopper le processus de remodelage.
Le but du contenseur cardiaque est d’exercer une contre
pression sur la paroi ventriculaire en diastole, ce qui
diminue la tension pariétale. Il se positionne donc en
thérapeutique complémentaire des traitements médica-
menteux.
Les différentes études animales ont mis en évidence que :
– il réduisait l’étirement myocardique et la tension parié-
tale ;
– il fournissait un support diastolique ;
– il stoppait le remodelage ventriculaire et améliorait
l’index de sphéricité du ventricule.
De manière plus ou moins attendue, à ces phénomènes
s’associait une amélioration de la fonction cardiaque.
Les études cliniques ont confirmé ces différents résultats en
y associant une amélioration de la qualité de vie du
patient.
Le dispositif Acorn CorCap
®
est fabriqué par la société
Acorn Cardiovascular Inc (Minnesota, États-Unis). C’est
un dispositif médical de classe III (ses accessoires sont des
dispositifs médicaux de classe IIa) et commercialisé en
France au prix tarif de 5 600 euros HT.
Il est constitué de fibres de polyester tricoté en panneaux
rectilignes et de fils de suture non résorbables en polyester
(figures 3 et 4).
Les propriétés du tissage permettent à la maille de s’étirer
plus facilement dans le sens de la longueur que dans celui
de la largeur. Cette particularité de l’élasticité du tissage
favorise un remodelage du cœur en forme elliptique plutôt
qu’en forme sphérique. Le tissage a aussi été conçu pour
résister au démaillage, à l’effilochage et à l’effrangement.
Le dispositif est disponible en six tailles différentes afin de
convenir au mieux à la taille du cœur des patients.
Dégradation de la fonction cardiaque
Remodelage ventriculaire
Mort
Activation neurohormonale
(SRAA...)
Aggravation des symptômes de l’insuffisance cardiaque
(classification NYHA, hospitalisations)
CorCap
dilatation ventriculaire
et tension pariétale
Figure 2.Mécanisme d’action du contenseur cardiaque Cor-
Cap.
Contenseur cardiaque CorCap®
J Pharm Clin, vol. 26, n° 2, juin 2007 125
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Les principales caractéristiques du filet CorCap
®
sont :
– une biocompatibilité à long terme même si une réaction
fibreuse doit être envisageable ;
– une conformabilité optimale : il ne doit pas être trop
serré afin de ne pas réduire la fonction cardiaque ni trop
large afin de servir de soutien ;
– une conformabilité bidirectionnelle : il s’étire de façon
plus longitudinale que transversale afin de redonner au
cœur sa forme ellipsoïde initiale ;
– une nature multifilamentaire qui lui permet d’exercer sur
l’épicarde une pression uniforme et de ne pas comprimer
les vaisseaux sanguins.
Les critères actuels d’indication de ce dispositif incluent les
patients adultes (âgés de 18 ans ou plus) présentant une
cardiomyopathie dilatée, d’origine ischémique ou non,
en stade II avancé ; III ou IV de la NYHA. Les patients
doivent présenter une dilatation ventriculaire (dimension
télédiastolique ventriculaire gauche indexée ≥30 mm/m
2
ou dimension télédiastolique ventriculaire gauche
≥60 mm) diagnostiquée par échocardiographie et une
FEVG < 35 %. De plus, les patients doivent être sous
traitement médical optimal et stable depuis au moins
3 mois (IEC ou autre médiament si intolérance aux IEC,
diurétique au moins à la demande) et présenter des
fonctions rénale, hépatique et pulmonaire acceptables.
Le filet peut être implanté seul ou associé à d’autres gestes
chirurgicaux tels qu’une revascularisation coronarienne
(pontage coronarien) ou une annuloplastie de la valve
mitrale. Dans tous les cas, un consentement éclairé doit
être signé par le patient.
Les principales contre-indications ou critères d’exclusion
retenus sont :
– contre-indication à une intervention chirurgicale cardia-
que évaluée par le chirurgien (par exemple : lésion cor-
pusculaire importante ou réserve cardiaque insuffisante) ;
– cardiomégalie importante (diamètre cardiaque
externe > 14,6 cm) dépassant la plus grande taille dispo-
nible de CorCap
®
;
– présence d’adhérences péricardiques ou épicardiques
préexistantes rendant impossible l’accès au cœur ;
– pontages coronariens préexistants ;
– état fonctionnel de fin de classe IV de la NYHA nécessi-
tant l’administration intraveineuse de médicaments inotro-
pes ou un dispositif d’assistance ventriculaire gauche ;
– cardiomyopathie hypertrophique obstructive ;
– infection active ;
– dérèglement diastolique primaire.
Le dispositif est implanté par sternotomie. Après avoir
incisé le thorax, l’épicarde est exposé par péricardioto-
mie. Une technique mini-invasive qui permet de réduire
l’ouverture du thorax et d’apporter un meilleur confort
pour le patient est en cours de développement au CHU de
Bordeaux.
La sélection de la bonne taille du dispositif passe par la
mesure de la taille du cœur pendant l’intervention en
mesurant le périmètre au niveau du sillon auriculo-
ventriculaire et la longueur apex artère pulmonaire à
l’aide d’une cordelette graduée. Le dispositif est posi-
tionné autour du cœur et fixé par des sutures non résorba-
bles le long du sillon auriculo-ventriculaire. Les sutures
doivent être espacées de2à4cmetletissu ne doit pas se
froisser ni se plisser entre les sutures. Une fois les sutures
posées, le dispositif est ajusté en retirant l’excès de tissu.
Il est alors entièrement en contact avec les parois ventricu-
laires pendant tout le cycle cardiaque.
Cet ajustement final entraîne une légère diminution (au
maximum 10 %) du diamètre ventriculaire gauche. L’écho-
graphie transœsophagienne (ETO) permet de vérifier que
la diminution du volume télédiastolique ventriculaire gau-
che (VTDVG) reste inférieure à 10 % afin d’éviter un effet
néfaste constrictif (figure 5).
Pendant la pose du dispositif, les paramètres hémodyna-
miques du patient doivent être surveillés à l’aide d’une
sonde de Swan Ganz.
Les principaux évènements indésirables pouvant survenir
suite à l’implantation du dispositif sont : des infections,
une réduction du débit sanguin coronarien, une abrasion
ou une érosion du dispositif, une réaction allergique au
dispositif ou des complications arythmiques.
Les différentes études précliniques et cliniques ont montré
que l’implantation du CorCap
®
entraînait une réaction
fibreuse très limitée du fait de la structure aérée du produit
et qu’il n’y avait pas de relation directe entre l’implanta-
tion du CorCap
®
et la constriction physiologique obser-
vée. En effet, celle-ci peut être observée dès lors qu’un
geste chirurgical est réalisé [11-17].
Figure 3.Le contenseur cardiaque Acorn CorCap™.
Figure 4.Détail du tissage.
C. Baudet Drouillard, et al.
J Pharm Clin, vol. 26, n° 2, juin 2007
126
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Matériel et méthodes
Au CHU de Bordeaux, 43 patients ont bénéficié de la
pose d’un contenseur cardiaque CorCap
®
entre
juin 2002 et mai 2006. Les critères d’inclusion et d’exclu-
sion correspondaient aux indications et contre-indications
définies plus haut. Le but de cette étude prospective a été
d’évaluer les améliorations fonctionnelles et hémodynami-
ques ainsi que l’absence d’effets secondaires en postopé-
ratoire.
Nous avons donc étudié les dossiers cliniques de ces
patients et suivi les risques de morbi-mortalité.
Les principaux paramètres étudiés sont ceux caractéristi-
ques de l’insuffisance cardiaque :
– évaluation des caractéristiques échographiques : vo-
lume télédiastolique ventriculaire gauche (VTDVG) et frac-
tion d’éjection ventriculaire (FEV) gauche en pré et post
opératoire ;
– évolution de la classe NYHA ;
– test de marche pendant 6 minutes ;
– mesure de la VO
2
max ;
– morbidité et mortalité.
Ces évaluations ont été réalisées avant et après l’interven-
tion, puis à 3 mois, 6 mois, 12 mois, 18 mois et 24 mois.
Résultats
Patients
La moyenne d’âge des patients était de 56 ± 11 ans
(29-71 ans) et la majorité était de sexe masculin (34/9).
La cause de l’insuffisance cardiaque était d’origine idio-
pathique (70 %) et ischémique (30 %).
La durée moyenne de l’insuffisance cardiaque était d’envi-
ron 4 ans ± 2 ans avec entre 2 et 8 décompensations
l’année précédente. En pré-opératoire, 70 % des patients
étaient sous IEC et bêtabloquants et 44 % sous antialdo-
stérone.
Au niveau fonctionnel, la majorité des patients était en
classe III de la NYHA (72 %) et les autres patients se
répartissaient entre la classe II (13 %) et la classe IV
(15 %), sachant que tous les patients en classe II étaient à
un stade sévère susceptible de se dégrader rapidement.
La VO
2
max était de 13,3 mL/min/kg (8-22) et les résul-
tats du test de marche à 6 minutes ont été de 422 ± 120 m
(190-580 m).
Six des patients souffraient d’une insuffisance rénale sé-
vère et un patient était sous dialyse.
La FEVG moyenne était de 24±4%(17-35 %) et l’éva-
luation échographique a montré un VTDVG moyen de
71±8mm(55-86 mm).
Technique opératoire
La durée moyenne de l’implantation du contenseur cardia-
que a été de 43 ± 12 minutes (28-56 min) pour un temps
total d’intervention de 192 ± 31 minutes (86-268 min).
Les interventions ont eu lieu à cœur battant sans mise sous
circulation extracorporelle (CEC) pour 40 % des patients.
Pour les autres patients, la durée moyenne de la CEC a été
de 74 ± 16 minutes (46-102 min).
Le contenseur cardiaque a été posé seul sans geste
associé chez 20 patients.
Les 23 autres patients ont subi un geste chirurgical asso-
cié : 36 % ont subi une annuloplastie mitrale, 8 % une
annuloplastie tricuspidienne, 5 % un remplacement valvu-
laire aortique, 27 % un pontage coronarien et 24 % la
pose d’un stimulateur triple chambre (figure 6).
Morbi-mortalité
Pendant la période de suivi des patients 17 ± 5 mois
[6-38] neuf décès ont été rapportés (soit 20,9 %)
(tableau 1). Trois décès sont survenus précocement pen-
dant le séjour à l’hôpital (choc hémorragique, choc car-
diogénique et insuffisance surrénalienne). Deux patients
sont décédés après l’hospitalisation initiale (< 30 J) d’un
choc septique pour l’un et d’un bas débit cardiaque pour
l’autre. Enfin, quatre décès tardifs sont survenus après
trois mois (bas débit cardiaque), quatre mois (syndrome
1. Positionnement
du filet
2. Ajustement
4. Résection du matériel
en excès
3. Coupure longitudinale
5. Coupure longitudinale
de renforcement
6. Implantation terminée
Figure 5.Technique d’implantation.
Contenseur cardiaque CorCap®
J Pharm Clin, vol. 26, n° 2, juin 2007 127
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
 7
7
 8
8
1
/
8
100%