cancer invasif stroma metastases

CANCER INVASIFCANCER INVASIF
STROMASTROMA
METASTASESMETASTASES
METASTASESMETASTASES
M.D. DieboldM.D. Diebold
20112011

CELLULES CANCEREUSES
PROPRIETES
-
Invasion locale
-
Dissémination : formation de métastase

PHASE LOCALE
Etapes
1)
In situ = intra
-
épithélial
2)
Rupture de la membrane basale (uniquement pour les épithéliums)
3)
Invasion du tissu adjacent (= chorion pour une muqueuse)
4)
Invasion locale
de proche en proche
remplacement du tissu sain
conséquences fonctionnelles
volume tumoral
complications
ex. :
occlusion, obstruction d’un canal
douleurs par invasion nerveuse, par distension
ulcération (peau, sein)
brèche vasculaire
hémorragie

MECANISMES D’INVASION
Modulation de l’ancrage des cellules entre elles et à MEC : molécules
d’adhésion(CAM)
ex :
cadherines ,intégrines
(protéines liant le cytosquelette à
MEC),selectines,et mol apparentées aux Ig
mobilité
Rôle des protéases
Rôle des protéases
Cellules Kc
protéases :
ex :
MMP (métalloprotéases matricielles)
(constituants du système de plasmine : urokinases)
Migration des cellules Kc (par pseudopodes) sous l’influence de :
facteurs de mobilité
autocrines (facteurs de croissance et produits de
dégradation de MEC) et chimiotactiques

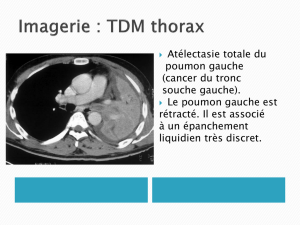
EN PRATIQUE
Le diagnostic d’invasion n’est possible que sur
prélèvements
tissulaires
Repose sur l’aspect de rupture
de la membrane basale de l’épithélium
de la membrane basale de l’épithélium
ou des structures (glandes…) qui constituent le tissu
Au début, étape de Kc micro
-
invasif
cancer intra
-
muqueux
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
1
/
26
100%