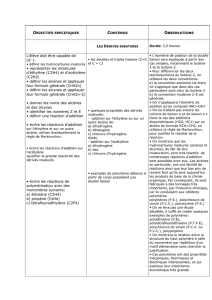
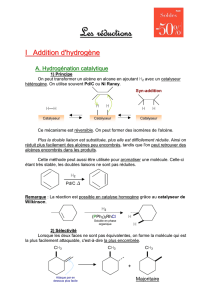
Additions sur les hydrocarbures insaturés

Chimie organique
Chapitre 1 : Additions sur les
hydrocarbures insaturés
I ) Les alcènes
1 ) Structure


2 ) Spectroscopie
Spectroscopie UV
Spectroscopie IR1650 cm-1
Spectroscopie RMN
● !"
#5 et 6 ppm
●Détermination des position cis ou trans#

3 ) Réactivité
●Nucléophilie"
●$redox%

II ) Hydratation des alcènes
1 ) Réaction.:
●&"' ()'*
+ (,)-.+#/0/0
.
●12alcool
●3%**
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
1
/
27
100%