2 Les réactions en chimie organique

UE5C vendredi 26 février 2010
1/7
Les réactions en chimie organique
Au cours d’une réaction il y a souvent rupture de liaisons et après d’autres liaisons se
forment. Mais initialement on trouve souvent des ruptures de liaisons
I – Rupture de liaison
2 catégories de ruptures
1 liaison σ avec 2 électrons, chaque partie de la molécule a apporté son électron, on a
une rupture dite homolytique, c’est à dire que chaque entité récupère l’électron qu’elle a
apporté pour formé la liaison, on a donc 2 entités porteuses chacune d’un électron
célibataires, ces entités sont des radicaux et souvent appelé radicaux libres
1 rupture hétérolytique au cours de laquelle
l’atome le plus électronégatif emporte avec lui
les 2 électrons de la simple liaison, il se voit
recevoir une charge négative, on observe alors
une partie anionique et une partie cationique.
Chimie organique = chimie du carbone, donc
les radicaux son appelés radicaux carbonés, les
entités positives sont les carbocations, les
entités négatives sont les carbanions.
II Intermédiaire réactionnels
A - les radicaux
Les radicaux sont des espèces électriquement neutres car ils n’ont pas acquis ni perdu
d’autres électrons, ils ont simplement récupéré ce qui leur appartenait, ils sont donc
neutre et ont un électron non apparié.
Les réactions qui impliquent des radicaux sont en général initiées par d’autres radicaux
provenant d’initiateurs.
Ces initiateurs possèdent une liaison σ de faible énergie, en général entre 2 atomes
identiques, et cette liaison peut être facilement rompue soit à l’aide de rayons lumineux
(hν) ou à l’aide de l’énergie thermique (apport de température positive)
On se servait comme initiateur des composés peroxydé (possédant 2 atomes d’oxygène
lié par une liaison σ de faible énergie, on a des restes carbonés de chaque côté de la
liaison O – O
L’hydropéroxyde on a 1 reste peroxyde et un atome d’hydrogène de chaque côté de la
liaison O – O

UE5C vendredi 26 février 2010
2/7
Ces peroxydes ont une structure pyramidale avec une orbitale très
dégagée (celle qui possède l’électron célibataire), rendant l’atome très
accessible à toutes sortes de réactifs d’où les radicaux sont des entités
chimiques extrêmement réactives. (Plus réactifs que les carbocation et
cabanions)
En général les radicaux carbonés sont considérés comme déficitaires en électrons et les
substituant qui tendent à renforcer structure
électronique vers lui le stabilisent, donc la
stabilité des radicaux croit avec le nombre de
groupements +I portés par le radical.
Inversement ils sont déstabilisé par des
groupements a effet –I
La stabilité est alors augmenté par
délocalisation.
B les carbocations
Un carbocation est une entité qui porte une charge
positive, il est hybridé sp2, donc un carbocation est plan,
comme précédemment les carbocations sont des entités
déficitaires en électrons donc ils sont stabilisés par des
substituant +I et ce d’autant plus que le nombre de
groupement +I augmente,
1 carbocation tertiaire sera plus stable qu’un II et qu’un I.
Ils sont stabilisé par délocalisation électronique, si on prend un carbocation allylique, il
existe 2 formes mésomères dans lesquels les charges positives sont portées par les
carbocations terminaux, on peut dire que ce carbocation est plus stable que le
carbocation éthyle ou même propylée de même nombre
d’atomes de carbones, on a un système conjugué.
Les hétéroatomes peuvent entrainé des délocalisations
de la charge positive, en particulier l’oxygène car ils sont
porteurs de doublets non liants qui vont être attirés par
le déficit électronique du carbone voisin. On a donc les
formules mésomères stabilisant le carbocation de
départ.
La délocalisation peut donc atteindre un hétéroatomes

UE5C vendredi 26 février 2010
3/7
ou un autre carbone.
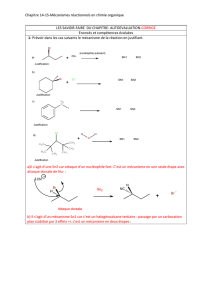
Les carbocations peuvent présenté des réactions de réarrangement qui consistent en la
formation d’un carbocation plus stable et nécessite un déplacement d’atomes ou de
groupement d’atomes
Ex : 1
On a un carbocation 1 aire on obtient un carbocation plus stable par migration d’un
atome d’hydrogène et formation d’un carbocation II aire, (isomérisation)
On peut aussi avoir déplacement d’un groupement d’électrons
Si ce carbocation primaire dérivé du diméthyle 2,2 propane, on obtient un carbocation
plus stable par migration d’un groupement CH3 sur le carbocation qui était porteur de la
charge positive, on obtient donc un carbocation tertiaire.
La stabilité est beaucoup plus importante, cette réaction se fera donc spontanément
Conséquence de la planéité d’un carbocation
Ajouter HCL formation de carbocation 2air
Addition de Cl-, mais le carbocation étant plan Cl- s’additionne d’un coté ou de l’autre de
la molécule
1er cas : au dessus, on obtient une configuration stéréochimique avec un carbone
asymétrique de configuration R
2e cas : au dessous, on obtient une configuration stéréochimique avec un carbone
asymétrique de configuration S
Le milieu réactionnel est il actif sur la lumière polarisé ? Non car c’est un mélange
racémique et qu’on a autant de R que de S puisque le carbocation est plan.
C les carbanions
Les carbanions peuvent être obtenus par arrachement d’un hydrogène
sous forme de protons à l’aide d’une base forte ces composés sont hybridé
sp3, donc il va avoir une structure tétraédrique, ils sont déjà porteur d’une
charge négative, donc les groupements +I vont déstabilisés en augmentant
la charge porté par ce carbone.

UE5C vendredi 26 février 2010
4/7
On peut dire que la stabilité d’un carbanion est lié à l’hybridation du carbone portant la
charge en effet un carbone hybridé sp est plus électronégatif qu’un carbone sp2 ou sp3,
il s’accommode mieux de la présence d’un doublet qu’un carbone sp2 ou sp3 donc un
carbanion sp est notamment plus stable qu’un carbanion sp2 analogue et sa formation
est donc plus aisée que celle d’un carbanion sp2 d’où l’acidité des acétyléniques vraies
III les réactifs
A réactifs électrophiles
Ils sont de 2 natures ce sont des espèces chargées positivement, le proton, le
carbocation, l’ion nitrosomium
Les espèces dont un atome porte une charge partielle positive et appartenant à une
liaison polarisée, c’est le cas de toutes les liaisons entre le carbone et les éléments plus
électronégatifs que le carbone
On verra surtout des liaisons CO, CN et CH(halogène), ces réactifs électrophiles
attaquent les sites riches au point de vue électronique
B les réactifs nucléophiles
Ils sont riches au point de vue électronique, on peut avoir des espèces chargées
négativement (ion hydroxide, ion alcoxyde, les halogènes on peut avoir aussi
l’hydrogène sous forme d’ion hydrure H-, on vient de parlé des acétyliures vraies qui
dérivent des acétyléniques vraies par perte d’un proton, les nitriles (qui dérivent de
l’acide cyanidrique par perte d’un proton), l’anion carboxylate, et tout ce qui est chargé
négativement.

UE5C vendredi 26 février 2010
5/7
Par contre on a également des espèces neutres et ce sont des entités qui possèdent des
doublets d’électrons non liants mais aussi des doublets d’électrons π, ce sont des
composé possédant à l’intérieur de la molécule, un atome d’oxygène doublement lié, un
atome de souffre doublement lié, les 2 sont porteurs de 2 doublets électroniques alors
que les dérivés de l’azote et du phosphore ne possèdent qu’un doublet électronique.
Il y des composés riches en électrons, ces structures tel que les éthyléniques et les
acétyléniques
L’acide de lewis est assimilable à une réactif électrophile puis qu’il possède une lacune
électronique
Et la base de lewis est assimilable à un réactif nucléophile
IV les principaux types de réactions
A réaction d’additions
On la rencontre en Chimie organique dans le cas des liaisons multiples carbones
carbones et avec 2 composé au départ on en
obtient 1.
Elles affectent la plupart du temps les liaisons
multiples : ex hydrolyse de l’éthylène éthanol
1 liaison a été rompue (en générale une π) et il
s’est formé 2 liaisons σ.
B substitution
Le réactif qui peut être un atome ou groupement va prend la place (substitué) un atome
ou groupement d’atomes du substrat.
Dérivé halogéné, substitution de l’halogène par OH- il s’agit d’une substitution
nucléophile
(2 types de SN)
 6
6
 7
7
1
/
7
100%